环戊二烯可用于制备二茂铁[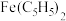 ,结构简式为
,结构简式为 ],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
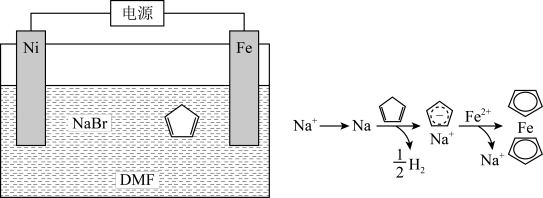
该电解池的阳极为___________ ,总反应为___________ 。电解制备需要在无水条件下进行,原因为___________ 。
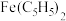 ,结构简式为
,结构简式为 ],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
该电解池的阳极为
21-22高二·全国·课时练习 查看更多[2]
更新时间:2022-09-04 20:15:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生产、生活密切相关,回答下列问题:
(1)如图为刻蚀在玻璃上的精美花纹图案,工人师傅常用_______ 刻蚀玻璃。

(2)金属钠着火时不能用水灭火,原因是_______ (用离子方程式表示)。
(3)下列物质:空气、氧气、食盐水、氢氧化钾、铜、蔗糖中,属于电解质的是_______ ,属于非电解质的是_______ 。
(4)已知某植物营养液配方为0.3 mol KCl、0.2 mol K2SO4、0.1 mol ZnSO4和1 L水。若以KCl、K2SO4、ZnCl2和1 L水为原料配得相同组成的营养液,则需K2SO4的物质的量为_______ mol。
(5)下列生产、生活中的事例中发生了氧化还原反应的是_______ (填字母)。
(6)“雷雨肥庄稼”涉及的化学方程式为_______ 、_______ 、_______ 。
(1)如图为刻蚀在玻璃上的精美花纹图案,工人师傅常用

(2)金属钠着火时不能用水灭火,原因是
(3)下列物质:空气、氧气、食盐水、氢氧化钾、铜、蔗糖中,属于电解质的是
(4)已知某植物营养液配方为0.3 mol KCl、0.2 mol K2SO4、0.1 mol ZnSO4和1 L水。若以KCl、K2SO4、ZnCl2和1 L水为原料配得相同组成的营养液,则需K2SO4的物质的量为
(5)下列生产、生活中的事例中发生了氧化还原反应的是
 |  |  |  |
| A.铁的冶炼 | B.早期的农业耕作 | C.简单机械织布 | D.祥云火炬燃烧 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据物质及其化合物的性质填空。
(1)为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末_______ (填试剂化学式);也可向煤油样品中加入一小块金属钠,若观察到_______ 现象,就可说明煤油中掺有水,写出相关的离子反应方程式_______ 。
(2)镁着火不能用二氧化碳来灭火,理由是_______ (用化学方程式表示)。
(3)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
①铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的离子反应方程式:_______ 。
②将7.8g过氧化钠投入500mL0.1mol/L氯化铝溶液中,可观察到的现象是_______ 。
A.放出无色无味的气体,生成大量白色沉淀
B.放出无色无味的气体,生成白色沉淀后恰好溶解
C.放出无色无味的气体,生成白色沉淀后部分溶解
D.无任何现象
(1)为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末
(2)镁着火不能用二氧化碳来灭火,理由是
(3)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
①铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的离子反应方程式:
②将7.8g过氧化钠投入500mL0.1mol/L氯化铝溶液中,可观察到的现象是
A.放出无色无味的气体,生成大量白色沉淀
B.放出无色无味的气体,生成白色沉淀后恰好溶解
C.放出无色无味的气体,生成白色沉淀后部分溶解
D.无任何现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠及其化合物是重要的化学物质。回答下列问题:
(1) 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为_________ (填化学式)。
(2)小块金属钠投入水中发生反应的离子方程式为_________ 。
(3) 、
、 都属于
都属于_________ (“碱性氧化物”或“氧化物”),可用蒸馏水检验 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:_________ 。
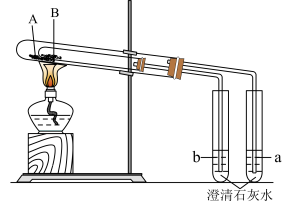
(4)如图装置可用于鉴别 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的_________ 性质加以鉴别。实验中可观察到b中澄清石灰水变浑浊,则物质A为_________ (填名称)。
(5) 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、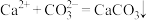 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
(1)
 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为(2)小块金属钠投入水中发生反应的离子方程式为
(3)
 、
、 都属于
都属于 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:(4)如图装置可用于鉴别
 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的
(5)
 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、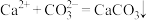 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:| 实验步骤 | 实验现象 |
ⅰ.取少量 溶液,向其中加入适量 溶液,向其中加入适量 溶液 溶液 | 无明显现象 |
| ⅱ.向上述溶液中滴加 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。
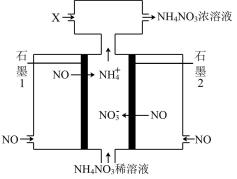
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____ (填1或2),该电极的反应式为_____________ 。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________ 。
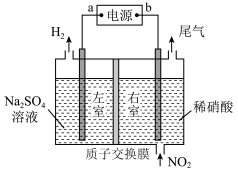
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______ 极,左室发生的电极反应式为_____________ 。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______ mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________ 。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。


(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烧, 电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2 = 3CO2+4H2O。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=________ (用△H1、△H2、△H3表示)
(2)写出该电池正极的电极反应式:_________ ,电池工作时CO32-移向_________ (填“正极”或“负极”);用该电池电解1000 mL lmol/L的AgNO3溶液(惰性电极),此电解池的反应方程式为_____________________________________ 。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=
(2)写出该电池正极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.载人航天工程对科学研究及太空资源开发具有重要意义,中国正逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次踏上飞向浩渺星辰的征途。
(1)氢氧燃料电池(构造如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。
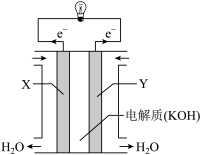
由此判断Y极为电池的___________ 极,OH-向___________ (填“正”或“负”)极作定向移动,Y极的电极反应式为___________ 。
Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲,已知肼反应生成N2)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。根据要求回答相关问题:
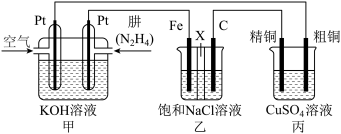
(2)甲装置中通入___________ 的一极为正极;乙装置中电解一段时间后溶液呈___________ 性,此时若将乙池中石墨(C)电极换成Mg电极,电极反应变为:___________ 。
(3)图中用丙装置模拟工业中的粗铜的精炼原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为___________ g。
(1)氢氧燃料电池(构造如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。

由此判断Y极为电池的
Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲,已知肼反应生成N2)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。根据要求回答相关问题:

(2)甲装置中通入
(3)图中用丙装置模拟工业中的粗铜的精炼原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国首创以铝组成的金属—海水—空气电池作为新型海水标志灯的能源,它以海水为电解质溶液,靠空气中的氧气使铝组成的金属不断氧化而产生电流。
(1)只要把灯放入海水中数分钟,就会发出耀眼的白光,则该电池的负极反应式为__________ ;
(2)电解法可制取碳的一种气态氢化物C2H4(如图所示)电极a接电源的__________ 极,该电极反应式为__________ ;
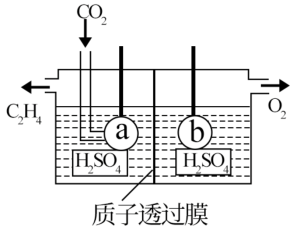
(3)将SO2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体NO,有关反应的离子方程式为__________ ;
(4)处理NOx的一种方法是利用甲烷催化还原NOx,
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ•mol-1;
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为__________ ;
(5)H2O2在工业、农业、医药上都有广泛的用途。用碱性氢氧燃料电池可合成H2O2,具有效率高、无污染等特点。电池总反应式为H2+O2+OH-=H2O+ ,写出正极反应式
,写出正极反应式__________ 。
(1)只要把灯放入海水中数分钟,就会发出耀眼的白光,则该电池的负极反应式为
(2)电解法可制取碳的一种气态氢化物C2H4(如图所示)电极a接电源的

(3)将SO2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体NO,有关反应的离子方程式为
(4)处理NOx的一种方法是利用甲烷催化还原NOx,
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ•mol-1;
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(5)H2O2在工业、农业、医药上都有广泛的用途。用碱性氢氧燃料电池可合成H2O2,具有效率高、无污染等特点。电池总反应式为H2+O2+OH-=H2O+
 ,写出正极反应式
,写出正极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用如图所示的装置进行电解,A中盛有NaOH溶液,B中盛有饱和Na2SO4溶液,通电一会儿,发现湿润的淀粉KI试纸的D端变为蓝色。回答下列问题:
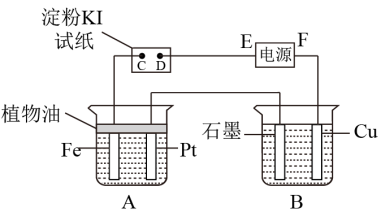
(1)电源的E端为__ (填“正”或“负”)极。
(2)A中Fe电极上的电极反应式为___ ;一段时间后,A中溶液pH__ (填“升高”、“降低”或“不变”)。
(3)B中发生反应的总化学方程式为___ 。
(4)电池工作tmin后,B装置中共收集到16.8L(折算为标准状况下)气体,此时电路中转移了__ mole-。
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸D端变为蓝色,下列做法可行的是__ (填标号)。
a. 将A中的溶液换成稀硫酸
b. 将A中的溶液换成浓硝酸
c. 将B中的溶液换成稀硫酸
d. 将B中的溶液换成浓硝酸

(1)电源的E端为
(2)A中Fe电极上的电极反应式为
(3)B中发生反应的总化学方程式为
(4)电池工作tmin后,B装置中共收集到16.8L(折算为标准状况下)气体,此时电路中转移了
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸D端变为蓝色,下列做法可行的是
a. 将A中的溶液换成稀硫酸
b. 将A中的溶液换成浓硝酸
c. 将B中的溶液换成稀硫酸
d. 将B中的溶液换成浓硝酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO3—还原为N2,一段时间后,溶液的碱性明显增强。则该反应离子方程式为____ 。
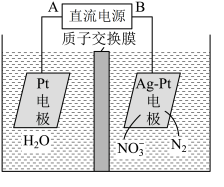
②电化学降解NO3—的原理如图所示,电源正极为________ (填“A”或 B”),若总反应4NO3-+4H+=5O2+2N2+2H2O,则阴极反应式为_______ 。
③能否把质子交换膜改为阴离子交换膜____________ (填“能“或”不能”)。
(2)研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
①CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为______ 。
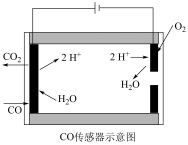
②测量汽车尾气中的CO浓度常用电化学气敏传感器,可用图简单表示,则阳极发生的电极反应为_____________________ 。
①催化硝化法中,用H2将NO3—还原为N2,一段时间后,溶液的碱性明显增强。则该反应离子方程式为
②电化学降解NO3—的原理如图所示,电源正极为
③能否把质子交换膜改为阴离子交换膜

(2)研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
①CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为
②测量汽车尾气中的CO浓度常用电化学气敏传感器,可用图简单表示,则阳极发生的电极反应为

您最近一年使用:0次



