利用下面两个装置进行钠及其化合物的性质验证实验(铁架台等辅助仪器已略去)。请回答下列问题:
(1)用图1装置做钠与水反应的实验:通过塑料瓶向U形管中加水使金属钠接触到水,同时挤压带玻璃珠的橡胶管,钠与水反应时U形管中液面的变化是___________ ;反应中钠熔化成一个闪亮的小球,说明的实验事实是___________ 。

(2)将 倒入图2装置的烧杯中,发现棉花能燃烧。实验中棉花包裹的淡黄色粉末物质为
倒入图2装置的烧杯中,发现棉花能燃烧。实验中棉花包裹的淡黄色粉末物质为____ (填化学式);烧杯底部垫细沙的目的是______ ;该淡黄色粉末与 反应的化学方程式为
反应的化学方程式为____ 。

(1)用图1装置做钠与水反应的实验:通过塑料瓶向U形管中加水使金属钠接触到水,同时挤压带玻璃珠的橡胶管,钠与水反应时U形管中液面的变化是

(2)将
 倒入图2装置的烧杯中,发现棉花能燃烧。实验中棉花包裹的淡黄色粉末物质为
倒入图2装置的烧杯中,发现棉花能燃烧。实验中棉花包裹的淡黄色粉末物质为 反应的化学方程式为
反应的化学方程式为
更新时间:2022/10/17 21:34:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠及其化合物是重要的化学物质。回答下列问题:
(1)Na、 、
、 、NaOH久置空气中最终都变为
、NaOH久置空气中最终都变为_______ (填化学式)。
(2)小块金属钠投入水中发生反应的离子方程式为_______ ;若4.6g金属钠完全与水反应,可产生 的质量是
的质量是_______ g。
(3) 、
、 都属于
都属于_______ (“碱性氧化物”或“氧化物”),可用蒸馏水检验 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:_______ 。
(4)如图装置可用于鉴别 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的_______ 性质加以鉴别。实验中可观察到b中澄清石灰水变浑浊,则物质A为_______ (填名称)。

(5) 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、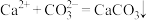 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
(1)Na、
 、
、 、NaOH久置空气中最终都变为
、NaOH久置空气中最终都变为(2)小块金属钠投入水中发生反应的离子方程式为
 的质量是
的质量是(3)
 、
、 都属于
都属于 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:(4)如图装置可用于鉴别
 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的
(5)
 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、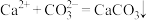 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:| 实验步骤 | 实验现象 |
i.取少量 溶液,向其中加入适量 溶液,向其中加入适量 溶液 溶液 | 无明显现象 |
| ii.向上述溶液中滴加 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】写化学方程式:
①钠和水反应___ 。
②铝和烧碱溶液反应___ 。
③铁和水蒸气反应___ 。
①钠和水反应
②铝和烧碱溶液反应
③铁和水蒸气反应
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据物质及其化合物的性质填空。
Ⅰ.为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末__ (填试剂化学式),若观察到___ 现象,就说明煤油中掺有水;也可向煤油样品中加入一小块金属钠,若观察到___ 现象,就可说明煤油中掺有水,反应的化学方程式是___ 。
Ⅱ.镁着火不能用二氧化碳来灭火,理由是___ (用化学方程式表示)。
Ⅲ.最近报纸上报导了有人混有洗涤剂发生中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(碱性含NaClO)进行杀菌。请写出涉及反应的离子方程式:___ 。
Ⅳ.除去下列物质中所混有少量的杂质,指明应加入的试剂,写出有关的离子反应方程式。
(1)Mg粉(Al粉):试剂___ ;离子方程式___ 。
(2)NaHCO3溶液(Na2CO3):试剂___ ;离子方程式___ 。
Ⅰ.为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末
Ⅱ.镁着火不能用二氧化碳来灭火,理由是
Ⅲ.最近报纸上报导了有人混有洗涤剂发生中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(碱性含NaClO)进行杀菌。请写出涉及反应的离子方程式:
Ⅳ.除去下列物质中所混有少量的杂质,指明应加入的试剂,写出有关的离子反应方程式。
(1)Mg粉(Al粉):试剂
(2)NaHCO3溶液(Na2CO3):试剂
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学与生活密切相关。回答下列问题:
(1)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度化学方程式表示为_______ 。
(2)NaHCO3的水溶液呈碱性,常用于处理食品生产中面粉过度发酵产生的有机酸(HA),又能使面食疏松多孔,有关反应的化学方程式为_______ 。
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为_______ ;漂白粉的有效成分是(填化学式)_______ 。
(4)漂白液的主要成分是NaClO和NaCl。其中的NaClO久置于空气中易失效的原因是_______ (用语言描述)。
(1)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度化学方程式表示为
(2)NaHCO3的水溶液呈碱性,常用于处理食品生产中面粉过度发酵产生的有机酸(HA),又能使面食疏松多孔,有关反应的化学方程式为
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(4)漂白液的主要成分是NaClO和NaCl。其中的NaClO久置于空气中易失效的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是___ (填序号,下同);属于电解质的是___ ;属于非电解质的是___ 。
(2)1.204×1024个H2SO4分子的物质的量为___ mol,共含___ 个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___ mol/L。
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为___ mol/L。
(4)写出铁在氯气中燃烧的化学方程式为___ ;过氧化钠与二氧化碳反应的化学方程式为___ 。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是
(2)1.204×1024个H2SO4分子的物质的量为
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO
 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为(4)写出铁在氯气中燃烧的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):

(1)若A是一种金属C是淡黄色固体,则B的化学式为______ ;A→C反应的化学方程式为______ ;写出C的一种用途______ (用化学方程式表示)。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为______ ,电子式为______ 。B→C反应的化学方程式为______ 。A和C是否能反应?______ (填“能”或“不能”),若能,写出反应的化学方程式:______ (若不能,此空不填)。

(1)若A是一种金属C是淡黄色固体,则B的化学式为
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据要求,写出化学方程式或者离子方程式;
(1)氯气和石灰乳反应制取漂白粉的化学方程式___________ ;
(2)过氧化钠和水反应的化学方程式___________ ;
(3)写出 和足量
和足量 反应的离子方程式
反应的离子方程式___________ ;
(4)碘盐中的 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式___________ ;
(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式___________ ;
(6)铜和浓硫酸加热反应的化学方程式___________ 。
(1)氯气和石灰乳反应制取漂白粉的化学方程式
(2)过氧化钠和水反应的化学方程式
(3)写出
 和足量
和足量 反应的离子方程式
反应的离子方程式(4)碘盐中的
 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式
(6)铜和浓硫酸加热反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾(① )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤ 。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥
。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥ 、⑦
、⑦ 等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
(1)在上述有标号的物质中,属于电解质的是___________ (填标号,下同),属于酸的是___________ ,属于盐的是___________ 。
(2)次氯酸盐氧化法: ___________
___________ ___________
___________ ___________
___________ ___________
___________ +___________
+___________ 。
。
①请配平上述离子方程式___________ 。
②上述反应中的还原剂为___________ ,氧化性:
___________ (填“大于”或“小于”) 。
。
(3)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:
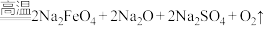 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。
。
①上述反应在熔融状态下进行,而不在水溶液中进行的原因是___________ (用化学方程式表示)。
②每生成3.2g ,理论上被氧化的
,理论上被氧化的 的质量为
的质量为___________ g。
 )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤ 。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥
。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥ 、⑦
、⑦ 等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。(1)在上述有标号的物质中,属于电解质的是
(2)次氯酸盐氧化法:
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ +___________
+___________ 。
。①请配平上述离子方程式
②上述反应中的还原剂为

 。
。(3)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:

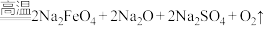 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。
。①上述反应在熔融状态下进行,而不在水溶液中进行的原因是
②每生成3.2g
 ,理论上被氧化的
,理论上被氧化的 的质量为
的质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学是一门以实验为基础的学科,研究小组需要经常做实验。
Ⅰ.某研究小组甲模仿侯德榜制备纯碱,原理为向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳。
(1)析出溶解度______ (填较小或较大)的碳酸氢钠,该反应离子方程式为______ 。
(2)欲得到纯碱,该研究小组将固体过滤、洗涤后,还需进行的操作是______(选装置)。
Ⅱ.某研究小组乙在探究 的性质实验时,发现
的性质实验时,发现 样品与过量水反应,待完全反应不再产生氧气后,得溶液
样品与过量水反应,待完全反应不再产生氧气后,得溶液 。溶液
。溶液 可使酸性
可使酸性 溶液褪色,同时放出氧气。小组成员查阅资料表明,
溶液褪色,同时放出氧气。小组成员查阅资料表明, 与水反应还可生成H2O2。
与水反应还可生成H2O2。
(3) 与水反应生成
与水反应生成 的反应是否属于氧化还原反应
的反应是否属于氧化还原反应______ (填是、否)。
(4)写出 与水反应的离子反应方程式:
与水反应的离子反应方程式:______ 。
(5)完成并配平该反应的离子方程式:__________ 。
 +H2O2+H+→Mn2++O2↑+□____
+H2O2+H+→Mn2++O2↑+□____
Ⅰ.某研究小组甲模仿侯德榜制备纯碱,原理为向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳。
(1)析出溶解度
(2)欲得到纯碱,该研究小组将固体过滤、洗涤后,还需进行的操作是______(选装置)。
A. | B. |
C. | D. |
Ⅱ.某研究小组乙在探究
 的性质实验时,发现
的性质实验时,发现 样品与过量水反应,待完全反应不再产生氧气后,得溶液
样品与过量水反应,待完全反应不再产生氧气后,得溶液 。溶液
。溶液 可使酸性
可使酸性 溶液褪色,同时放出氧气。小组成员查阅资料表明,
溶液褪色,同时放出氧气。小组成员查阅资料表明, 与水反应还可生成H2O2。
与水反应还可生成H2O2。(3)
 与水反应生成
与水反应生成 的反应是否属于氧化还原反应
的反应是否属于氧化还原反应(4)写出
 与水反应的离子反应方程式:
与水反应的离子反应方程式:(5)完成并配平该反应的离子方程式:
 +H2O2+H+→Mn2++O2↑+□____
+H2O2+H+→Mn2++O2↑+□____
您最近半年使用:0次



