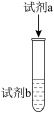
某化学兴趣小组同学利用下图所示装置(夹持及加热装置已略去,装置气密性良好)探究SO2的性质(实验前已事先除去装置中的空气)。请回答下列问题:
[查阅资料得知浓硫酸的沸点为338 ℃,酒精灯火焰的温度为400~500 ℃]
(1)仪器a的名称_______ 。
(2)装置D和F的作用是_______ 。
(3)加热时,装置A中反应的化学方程式为_______ 。
(4)打开K1,关闭K2,加热装置A一段时间后,B中的现象是_______ ,当装置C中溶液由蓝色变为无色,由此推测所得无色溶液中的离子主要是H+、I- 和_______ ;为了进一步实验证实了该过程中SO2已被氧化,该实验操作及现象是:_______ 。
(5)关闭K1,打开K2,用酒精灯加热装置A,观察到E中发生的现象是:有白色沉淀产生,白色沉淀的成分是_______ ,生成白色沉淀的原因可能是_______ (选填字母序号)。
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
c.SO2溶于水生成的H2SO3被装置内的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀

[查阅资料得知浓硫酸的沸点为338 ℃,酒精灯火焰的温度为400~500 ℃]
(1)仪器a的名称
(2)装置D和F的作用是
(3)加热时,装置A中反应的化学方程式为
(4)打开K1,关闭K2,加热装置A一段时间后,B中的现象是
(5)关闭K1,打开K2,用酒精灯加热装置A,观察到E中发生的现象是:有白色沉淀产生,白色沉淀的成分是
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
c.SO2溶于水生成的H2SO3被装置内的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀
更新时间:2022-10-01 23:00:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.为探究某盐X ( 含五种元素)的组成和性质, 设计并完成如下实验:
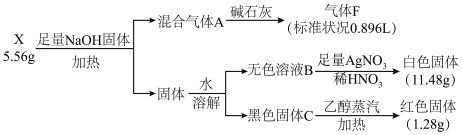
已知:气体F能使湿润的红色石蕊试纸变蓝。请回答:
(l)X含有的元素有 O、H、_____ ( 用元素符号表示), X 的化学式为_____ 。
(2)写出气体F 与黑色固体 C 在一定条件下发生的氧化还原反应, 产物中有一气体单质:______ 。
II.某学习小组设计制取 SO2并验证其部分性质的实验装置如图(夹持装置省略):

请回答:
(1)简述检查装置 A 气密性的方法:_________ 。
(2)写出C 中发生的离子反应方程式:_________ 。
(3)设计实验方案检验实验后 D 中的主要阴离子:________ .

已知:气体F能使湿润的红色石蕊试纸变蓝。请回答:
(l)X含有的元素有 O、H、
(2)写出气体F 与黑色固体 C 在一定条件下发生的氧化还原反应, 产物中有一气体单质:
II.某学习小组设计制取 SO2并验证其部分性质的实验装置如图(夹持装置省略):

请回答:
(1)简述检查装置 A 气密性的方法:
(2)写出C 中发生的离子反应方程式:
(3)设计实验方案检验实验后 D 中的主要阴离子:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知化合物A与B、丙与丁的元素组成相同,且四种物质中都含有同一种元素。A与B在常温下均呈液态。D为应用最广泛的金属,且D 与甲的浓溶液在常温作用无明显现象,加热时有大量气体产生。(相关转化部分反应条件和生成物未标出)。
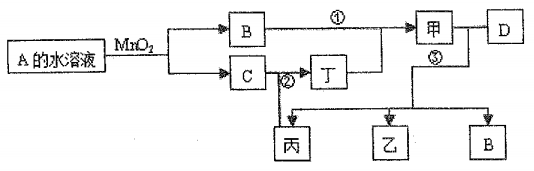
注: 转化关系中,②表示C 与丙反应生成丁。
(I)反应中MnO2的作用为_____ ,有1mol A 完全反应生成B、C转移____ mol 电子;
(II)若反应①除生成甲外,还生成丙,回答(1)、(2) 小题:
(1)反应②的化学方程式:_______________ 。
(2)写出过量D 与甲的稀溶液反应的离子方程式:____________ 。
(III)若丙为无色有刺激性气味的气体,可以使品红溶液褪色,回答(3)、(4) 小题:
(3)写出下列化学方程式②:__________________ ;③(甲足量):_________________ 。
(4)检验乙溶液中离子的实验方法为______________ 。

注: 转化关系中,②表示C 与丙反应生成丁。
(I)反应中MnO2的作用为
(II)若反应①除生成甲外,还生成丙,回答(1)、(2) 小题:
(1)反应②的化学方程式:
(2)写出过量D 与甲的稀溶液反应的离子方程式:
(III)若丙为无色有刺激性气味的气体,可以使品红溶液褪色,回答(3)、(4) 小题:
(3)写出下列化学方程式②:
(4)检验乙溶液中离子的实验方法为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】化学实验是研究和学习物质及其变化的基本方法,是科学探究的一种重要途径。某小组同学在实验室中用浓硫酸与铜反应制取二氧化硫,并对二氧化硫的性质进行探究,回答下列问题:

(1)仪器a的名称是________ ,装置A中制取SO2的化学方程式为________ 。
(2)配制100mL一定浓度的BaCl2溶液所需玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管和_______ 。
(3)欲用以上装置验证SO2的氧化性、还原性和漂白性,装置D中应盛放的试剂是_______ (填字母)。
(4)向溶解有SO2的BaCl2溶液中滴加下列溶液,能产生沉淀的有_______ (填字母)。
(5)国家规定葡萄酒中SO2最大含量为0.25g/L。该兴趣小组测某葡萄酒中SO2含量:测得 葡萄酒与20mL0.02mol/L碘水完全反应,则该葡萄酒中SO2的含量为
葡萄酒与20mL0.02mol/L碘水完全反应,则该葡萄酒中SO2的含量为_______ g/L(保留3位有效数字);若用酸性KMnO4溶液测定,测量结果会明显偏大,原因是KMnO4溶液除了与SO2反应,还会与葡萄酒中的________ 发生反应。

(1)仪器a的名称是
(2)配制100mL一定浓度的BaCl2溶液所需玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管和
(3)欲用以上装置验证SO2的氧化性、还原性和漂白性,装置D中应盛放的试剂是
| A.碘水 | B.石蕊溶液 | C.饱和NaCl溶液 | D.Na2S溶液 |
| A.NaCl溶液 | B.溴水 | C.氨水 | D.稀盐酸 |
 葡萄酒与20mL0.02mol/L碘水完全反应,则该葡萄酒中SO2的含量为
葡萄酒与20mL0.02mol/L碘水完全反应,则该葡萄酒中SO2的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有能看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生现象明显比通入CO2快。
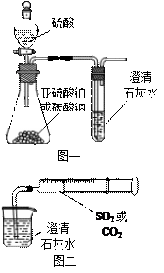
(1)对比分析两组实验,你认为用图一装置实验
时,通入SO2不能出现浑浊的原因可能是:
_________________ 。
(2)用图二装置实验时,以相同速率通入CO2或
SO2,SO2产生浑浊、澄清的现象比CO2
快的原因是______________________________________ 。
(3)用图一进行SO2与石灰水反应的实验时,从安全角度
考虑装置应做何改进?
_____________________________________________ 。
(4)有人提出上述实验现象“石灰水先变浑浊再澄清”可能与澄清石灰水的浓度有关。为了探究CO2通入澄清石灰水中的实验现象,查得下列数据:
Ⅰ 20℃时,Ca(OH)2的溶解度为:0.165g/100g水。
Ⅱ 不同浓度石灰水生成CaCO3的最大量
① 上表中A=___________________ g/100g水
Ⅲ 在1.01×105Pa CO2压力下,CaCO3的溶解度
Ⅳ 在不同压强(CO2)下,CaCO3溶解度(18℃)
认真分析以上数据回答下列问题:
②由表Ⅲ和表Ⅳ可知CaCO3溶解度的变化规律是:________________________________________________________________________________________________________________________
③由以上数据可以得出结论:欲观察到“石灰水先变浑浊再澄清的现象”,所需要的实验条件是:___________________________________________________________________________________

(1)对比分析两组实验,你认为用图一装置实验
时,通入SO2不能出现浑浊的原因可能是:
(2)用图二装置实验时,以相同速率通入CO2或
SO2,SO2产生浑浊、澄清的现象比CO2
快的原因是
(3)用图一进行SO2与石灰水反应的实验时,从安全角度
考虑装置应做何改进?
(4)有人提出上述实验现象“石灰水先变浑浊再澄清”可能与澄清石灰水的浓度有关。为了探究CO2通入澄清石灰水中的实验现象,查得下列数据:
Ⅰ 20℃时,Ca(OH)2的溶解度为:0.165g/100g水。
Ⅱ 不同浓度石灰水生成CaCO3的最大量
| 饱和石灰水与水的体积比 | 1:0 | 1:1 | 1:2 | 1:3 | 1:5 | 1:7 |
| 能生成CaCO3的最大量(g/100水) | A | 0.110 | 0.073 | 0.055 | 0.037 | 0.028 |
① 上表中A=
Ⅲ 在1.01×105Pa CO2压力下,CaCO3的溶解度
| 热力学温度/K | 282 | 298 | 308 |
| CaCO3溶解度(g/100水) | 0.130 | 0.094 | 0.076 5 |
Ⅳ 在不同压强(CO2)下,CaCO3溶解度(18℃)
| P(CO2)/Pa | 0 | 1.40×104 | 9.95×104 |
| CaCO3溶解度(g/100水) | 0.001 3 | 0.023 3 | 0.108 6 |
认真分析以上数据回答下列问题:
②由表Ⅲ和表Ⅳ可知CaCO3溶解度的变化规律是:
③由以上数据可以得出结论:欲观察到“石灰水先变浑浊再澄清的现象”,所需要的实验条件是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组取一定质量的FeSO4固体,利用下图装置进行实验。
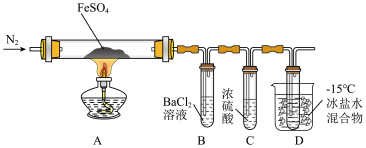
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8 ℃。
(1)实验③反应的离子方程式是_________________________ 。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有________ 气体,依据是________________________________ 。
(3)实验④反应的离子方程式是__________________________ 。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:____________ (用必要的文字和化学方程式解释)。

| 实验 | 实验过程 | 实验现象 |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色 B中有白色沉淀,D试 管中有无色液体 |
| ② | 用带有火星的木条靠近 装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热, 冷却后,取A中固体, 加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D 试管中 | 溶液变为浅绿色 |
(1)实验③反应的离子方程式是
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有
(3)实验④反应的离子方程式是
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】双氧水和含氯消毒剂是生活中常用的消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
①从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有还原性的实验是_______ (填序号),写出该过程的离子方程式_______ 。
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式_______ 。
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因_______ (用化学用语解释其原理)。
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为_______ 。
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为_______ mol。
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的_______ 倍。
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有还原性的实验是
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
提出问题: 、Br2哪个氧化性更强?
、Br2哪个氧化性更强?
(1)猜想:①甲同学认为氧化性: >Br2,故上述实验现象不是发生氧化还原反应所致,则溶液呈黄色是含
>Br2,故上述实验现象不是发生氧化还原反应所致,则溶液呈黄色是含___________ (填化学式,下同)所致。②乙同学认为氧化性:Br2> ,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含
,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含___________ 所致。
(2)设计实验并验证:丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点是正确的。
供选用的试剂:a.酚酞试液 b.CCl4 c.无水酒精 d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。
(3)结论:氧化性Br2> 。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为
。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为_______ 。
实验后的思考:根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是______ 。
某实验室用含少量铁的废铜渣为原料生产胆矾的流程如下:
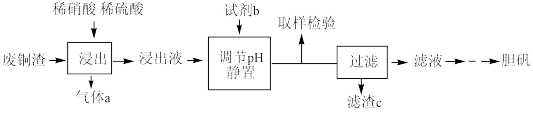
已知: 在pH为2.7时开始沉淀,到3.7时沉淀完全;
在pH为2.7时开始沉淀,到3.7时沉淀完全; 在pH为4.7时开始沉淀。
在pH为4.7时开始沉淀。
(4)“浸出”时,原料中的铜均转化为硫酸铜。写出相应的离子方程式:___________ 。
(5)试剂b是___________ (填物质名称),其反应的离子方程式:___________ 。
(6)调节pH的目的是___________ 。滤渣c是___________ 。
(7)将得到的胆矾与其他液体混合物分离的方法为___________ 。
提出问题:
 、Br2哪个氧化性更强?
、Br2哪个氧化性更强?(1)猜想:①甲同学认为氧化性:
 >Br2,故上述实验现象不是发生氧化还原反应所致,则溶液呈黄色是含
>Br2,故上述实验现象不是发生氧化还原反应所致,则溶液呈黄色是含 ,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含
,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含(2)设计实验并验证:丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点是正确的。
供选用的试剂:a.酚酞试液 b.CCl4 c.无水酒精 d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。
| 选用试剂(填序号) | 实验现象 | |
| 方案1 | ||
| 方案2 |
 。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为
。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为实验后的思考:根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是
某实验室用含少量铁的废铜渣为原料生产胆矾的流程如下:
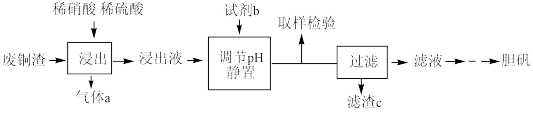
已知:
 在pH为2.7时开始沉淀,到3.7时沉淀完全;
在pH为2.7时开始沉淀,到3.7时沉淀完全; 在pH为4.7时开始沉淀。
在pH为4.7时开始沉淀。(4)“浸出”时,原料中的铜均转化为硫酸铜。写出相应的离子方程式:
(5)试剂b是
(6)调节pH的目的是
(7)将得到的胆矾与其他液体混合物分离的方法为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:

(1)图中D装置在实验中的作用是_______ 。
(2)若 A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S) 饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程为_______ 。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现是_______ ;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的离子反应方程式_______ 。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是_______ ,C中发生反应的离子方程式为_______ 。
(5)若B为块状大理石,C为 溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的
溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的_______ 。
A.HCl B.HNO3 C.H2SO4 D.CH3COOH

(1)图中D装置在实验中的作用是
(2)若 A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S) 饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程为
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现是
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是
(5)若B为块状大理石,C为
 溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的
溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的A.HCl B.HNO3 C.H2SO4 D.CH3COOH
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】无水FeCl2为黄绿色晶体,在空气中易被氧化、易吸水,不溶于氯仿等有机溶剂。
I.FeCl2的制备:
制备反应原理为2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl↑(C6H5Cl为氯苯,沸点132℃),制备装置如图所示(夹持及加热装置略去),收集的HCl气体可用于测定FeCl2的产率。
2FeCl2+C6H4Cl2+HCl↑(C6H5Cl为氯苯,沸点132℃),制备装置如图所示(夹持及加热装置略去),收集的HCl气体可用于测定FeCl2的产率。_______ ,作用是_______ 。
(2)装置C中的试剂是_______ (填化学式)。装置D的作用是_______ 。
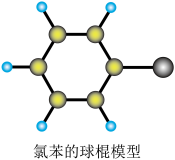
(3)氯苯(C6H5Cl)的球棍模型图,氯苯可由苯和氯气在催化剂条件下反应生成,其化学反应方程式为_______ ,反应类型是_______ 。
已知:Ba2+与SCN-可在溶液中大量共存;SCN-易被氧化为 。
。
(4)对实验ⅰ中溶液变为浅红色的原因,甲同学提出以下假设。
假设1:加入饱和氯水的量少,生成的 的浓度小;
的浓度小;
假设2:氯水氧化性强,_______ 。
取实验i中浅红色溶液,_____ (填实验操作),溶液浅红色消失,从而排除假设1;向2mL水中滴加5mL0.1mol·L−1KSCN溶液,滴加0.5mL饱和氯水,加入______ ,产生白色沉淀,说明假设2正确。
(5)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是_______ (用离子方程式表示,已知SCN-中C元素为+4价)。
I.FeCl2的制备:
制备反应原理为2FeCl3+C6H5Cl
 2FeCl2+C6H4Cl2+HCl↑(C6H5Cl为氯苯,沸点132℃),制备装置如图所示(夹持及加热装置略去),收集的HCl气体可用于测定FeCl2的产率。
2FeCl2+C6H4Cl2+HCl↑(C6H5Cl为氯苯,沸点132℃),制备装置如图所示(夹持及加热装置略去),收集的HCl气体可用于测定FeCl2的产率。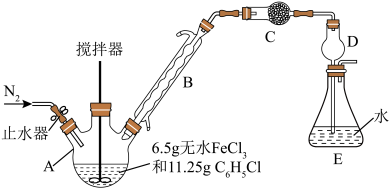
(2)装置C中的试剂是
(3)氯苯(C6H5Cl)的球棍模型图,氯苯可由苯和氯气在催化剂条件下反应生成,其化学反应方程式为
| 序号 | 装置 | 试剂b | 试剂a | 实验现象 |
| 实验i |
| 5mL0.1mol·L−1KSCN溶液、1mL0.1mol·L−1FeCl2(pH=1)溶液 | 0.5mL饱和氯水 | 溶液立即变为浅红色 |
| 实验ii | 1mL15mol·L−1HNO3溶液 | 溶液变为红色,一段时间后,溶液褪为无色,且溶液中产生无色气泡,试管上方呈红棕色 |
 。
。(4)对实验ⅰ中溶液变为浅红色的原因,甲同学提出以下假设。
假设1:加入饱和氯水的量少,生成的
 的浓度小;
的浓度小;假设2:氯水氧化性强,
取实验i中浅红色溶液,
(5)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是
您最近一年使用:0次