根据元素周期律回答:
(1)比较原子半径的大小(填“>”或“<”,下同):K_______ Ca,Si_______ N;
(2)比较酸碱性的强弱:HNO3_______ H3PO4,Mg(OH)2_______ Al(OH)3;
(3)比较氢化物的热稳定性:H2S_______ H2O,NH3_______ HF。
(4)①N2 ②MgCl2 ③NH3 ④Na2O2 ⑤Ne,这些物质中,只含有非极性键的是_______ ;只含有离子键的是_______ ;既含有共价键又含有离子键的是_______ ;只含有极性键的是_______ 。写出②的形成过程:_______
(1)比较原子半径的大小(填“>”或“<”,下同):K
(2)比较酸碱性的强弱:HNO3
(3)比较氢化物的热稳定性:H2S
(4)①N2 ②MgCl2 ③NH3 ④Na2O2 ⑤Ne,这些物质中,只含有非极性键的是
更新时间:2022-10-20 18:20:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下列各题中有关物质的比较,请用“>”、“<”、“=”填空:
(1)酸性:H3PO4____ HNO3,H2SO4___ HClO4;
(2)氧化性:F2____ S,N2___ O2;
(3)热稳定性:CH4____ NH3,HCl____ HI。
(1)酸性:H3PO4
(2)氧化性:F2
(3)热稳定性:CH4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请利用元素周期律和元素周期表的有关知识回答下列问题。
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
(2)A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层电子数是最外层电子数的2倍,则A、B元素。______
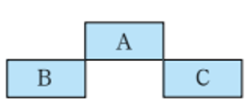
(3)短周期元素A、B、C在元素周期表中的位置如图所示。已知B、C两元素的原子序数之和是A元素的原子序数的4倍,则A、B、C分别是______
(4)X、Y、Z是相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z分别是_________
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
| A.Li、Be、B原子的最外层电子数依次增多 |
| B.P、S、Cl元素的最高正化合价依次升高 |
| C.N、O、F原子的半径依次增大 |
| D.Na、K、Rb原子核外的电子层数依次增多 |
| A.一定是第2周期元素 | B.一定是同一周期元素 |
| C.一定分别位于第2、3周期 | D.可以相互化合形成化合物 |

| A.Be、Na、Al | B.B、Mg、Si | C.O、P、Cl | D.C、Al、P |
| A.Mg、Al、Si | B.Li、Be、Mg | C.N、O、S | D.P、S、O |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表反映了元素性质的变化规律,是学习、研究和应用化学的重要工具。下表为元素周期表的一部分,回答下列问题:

(1)Mg和Al都是制造飞机和宇宙飞船的重要材料。Mg和Al属于同周期_______ (填“金属”或“非金属”)元素,但Mg的原子半径比Al的_______ 。
(2)C的非金属性比同主族Si的非金属性_______ 。
(3)Cl的最高价氧化物对应的水化物属于_______ (填“酸”或“碱”)。
(4)Mg在 中燃烧生成
中燃烧生成_______ (填化学式),该产物中所含化学键的类型为_______ 。
(5)各种物质中均储存着化学能,化学能可使物质中的电子保持_______ (填“静止”或“运动”)状态。在氢气-氧气燃料电池中,化学能转化为电能时,还原剂是_______ (填化学式)。与普通锌锰干电池相比,该电池的优势是_______ (任填一项)。假如该燃料电池工作时每消耗1 g  可释放143 kJ的能量,其中80%可转化为电能,则该电池消耗1 mol
可释放143 kJ的能量,其中80%可转化为电能,则该电池消耗1 mol  时输出的电能应为
时输出的电能应为_______ kJ。

(1)Mg和Al都是制造飞机和宇宙飞船的重要材料。Mg和Al属于同周期
(2)C的非金属性比同主族Si的非金属性
(3)Cl的最高价氧化物对应的水化物属于
(4)Mg在
 中燃烧生成
中燃烧生成(5)各种物质中均储存着化学能,化学能可使物质中的电子保持
 可释放143 kJ的能量,其中80%可转化为电能,则该电池消耗1 mol
可释放143 kJ的能量,其中80%可转化为电能,则该电池消耗1 mol  时输出的电能应为
时输出的电能应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。流程如下图所示:

(1)用电子式表示Br2的形成过程________ 。提取Br2 时,第一次通入Cl2 后发生反应的离子方程式是_______ ;ⅦA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐______ (填“增大”或“减小”),得电子能力逐渐减弱。②中SO2表现 _________ (填“氧化”“还原”“酸”“碱”)性;
(2)镁在元素周期表中的位置是________ ;为了实现对镁离子的富集,①中分离提纯的实验操作名称是__________ ;
(3)用MgCl2溶液制成无水MgCl2,加热溶液过程中,会生成Mg(OH)Cl溶液和一种酸性气体。写出该反应的化学方程式______ 。

(1)用电子式表示Br2的形成过程
(2)镁在元素周期表中的位置是
(3)用MgCl2溶液制成无水MgCl2,加热溶液过程中,会生成Mg(OH)Cl溶液和一种酸性气体。写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】卤族元素:
①物理性质
相似性:_______ 。
递变性:_______ 。
②化学性质
相似性:_______ 。
递变性:_______ 。
①物理性质
相似性:
递变性:
②化学性质
相似性:
递变性:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】短周期元素A、B、D、E、G、J在周期表中的位置如下:
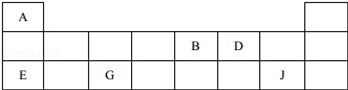
(1)根据上表回答问题:
①D在周期表中的位置是__ .
②A、B、E、G的原子半径由大到小的顺序是__ (填元素符号).
③B、D的气态氢化物的稳定性关系为__ (填化学式).
④34Se与D同主族,其非金属性比D__ (填“强”或“弱”),从原子结构的角度解释其原因为__ .
⑤E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为ⅰ.H++OH﹣=H2O、ⅱ._________ 、ⅲ.________ .
(2)如图所示转化关系中的各物质由以上六种元素的一种或多种组成,其中甲、乙、丙、丁为两种元素组成的化合物,甲、丙的分子属于10电子微粒,丙为常见溶剂.(图中部分产物已略)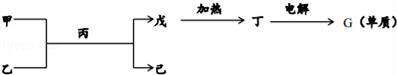
①物质己中含有的化学键的类型为__ .
②用电子式表示丙分子的形成过程为__ .
③由丁电解制得G单质的化学反应方程式为__ .

(1)根据上表回答问题:
①D在周期表中的位置是
②A、B、E、G的原子半径由大到小的顺序是
③B、D的气态氢化物的稳定性关系为
④34Se与D同主族,其非金属性比D
⑤E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为ⅰ.H++OH﹣=H2O、ⅱ.
(2)如图所示转化关系中的各物质由以上六种元素的一种或多种组成,其中甲、乙、丙、丁为两种元素组成的化合物,甲、丙的分子属于10电子微粒,丙为常见溶剂.(图中部分产物已略)

①物质己中含有的化学键的类型为
②用电子式表示丙分子的形成过程为
③由丁电解制得G单质的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(一)硫及其化合物在生产、生中有广泛应用。
(1)硫原子最外层有_________ 种不同运动状态的电子,能量最高的电子其电子云形状是________ 。
(2)硫与同主族的短周期元素相比,形成气态氢化物稳定性的大小为_________ ,从化学键角度解释其原 因____________ 。
(3)棉织物用氯气漂白后,加入 Na2S2O3 除去余氯,反应中___________ 被氧化;若反应中生成 0.2 mol SO42-则转移电子________ mol。
(4)同温同浓度的 Na2SO3、(NH4)2SO3、NaHSO3 三种溶液中c(SO32-)最大的是___________ 。
(5)经测定 NaHSO3 溶液中 c(H2SO3)<c(SO32-),则 NaHSO3溶液呈_____ (填“酸或碱”)性,请结合相关方程式解释原因_______________ 。
(1)硫原子最外层有
(2)硫与同主族的短周期元素相比,形成气态氢化物稳定性的大小为
(3)棉织物用氯气漂白后,加入 Na2S2O3 除去余氯,反应中
(4)同温同浓度的 Na2SO3、(NH4)2SO3、NaHSO3 三种溶液中c(SO32-)最大的是
(5)经测定 NaHSO3 溶液中 c(H2SO3)<c(SO32-),则 NaHSO3溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置。请回答下列问题:

(1)铁元素位于元素周期表中第四周期__________ 族。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是氢原子的最外层电子“饱和缺一”。请写出LiH的电子式_____________ ,而且Li+的离子半径比H-_______ (填“大”或“小”)。
(3)d的某化合物呈淡黄色,可与硫酸亚铁溶液反应生成红褐色沉淀和能使带火星的木条复燃的气体,d的该化合物中含有的化学键类型为__________________ 。
(4)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带______ (填“正”或“负”) 电荷。
(5)下列叙述正确的是______
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.氢化物的酸性:f弱于g

(1)铁元素位于元素周期表中第四周期
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是氢原子的最外层电子“饱和缺一”。请写出LiH的电子式
(3)d的某化合物呈淡黄色,可与硫酸亚铁溶液反应生成红褐色沉淀和能使带火星的木条复燃的气体,d的该化合物中含有的化学键类型为
(4)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带
(5)下列叙述正确的是
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.氢化物的酸性:f弱于g
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】五种短周期元素的部分性质数据如下:
(1)Z离子的结构示意图为_______________ 。
(2)关于Y、Z两种元素,下列叙述正确的是__________ (填序号)。
a 简单离子的半径Y>Z
b 气态氢化物的稳定性Y比Z强
c 最高价氧化物对应水化物的酸性Z比Y强
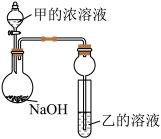
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物。某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是____________________________ 。一段时间后,观察到试管中的现象是_________________________ ,发生反应的离子方程式是___________________________ 。
(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被氢氧化钠溶液吸收的化学方程式是: 2XO2+2NaOH=M+NaXO3+H2O (已配平),产物M中元素X的化合价为__________ 。
| 元素 | T | X | Y | Z | W |
| 原子半径(mm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
(2)关于Y、Z两种元素,下列叙述正确的是
a 简单离子的半径Y>Z
b 气态氢化物的稳定性Y比Z强
c 最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物。某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是

(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被氢氧化钠溶液吸收的化学方程式是: 2XO2+2NaOH=M+NaXO3+H2O (已配平),产物M中元素X的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H除外):____ ,所含元素的原子半径由小到大的顺序:_____ ,Mg在元素周期表中的位置:_______ ,Mg(OH)2的电子式:_____
(2)在NaCl、NaOH、N2、H2S中,只含有离子键的是____ ,仅含有共价键的化合物是_______
(3)用电子式表示MgCl2的形成过程___________
(4)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净,干燥后称重,总质量为47g,则产生氢气的体积___ mL(标准状况)
(2)在NaCl、NaOH、N2、H2S中,只含有离子键的是
(3)用电子式表示MgCl2的形成过程
(4)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净,干燥后称重,总质量为47g,则产生氢气的体积
您最近一年使用:0次



