汽车的方向盘和前排乘客座位前的仪表板内都有折叠安全气囊,该安全气囊中含有叠氮化钠(NaN3)、硝酸钾(KNO3)、二氧化硅(SiO2)粉等。完成下列填空:
(1)关于KNO3,下列分析正确的是_______。(单选,选填选项)
(2)行驶的汽车发生有足够强度的意外碰撞时,碰撞传感器将激活特定的电路,放电使NaN3迅速分解,生成Na并放出N2,写出NaN3分解的化学方程式_______ 。
(3)生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑,标出该反应电子转移的方向和数目:____________ ,该反应的还原剂是_______ ,发生还原反应的物质是_______ ,生成14g氮气,转移电子的物质的量为_______ 。
(1)关于KNO3,下列分析正确的是_______。(单选,选填选项)
| A.KNO3电离需要通电 |
| B.KNO3是强电解质,其水溶液的导电性一定强 |
C.熔融状态的KNO3中含自由移动的K+和NO |
D.固态KNO3不导电,因其中不含K+和NO |
(3)生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑,标出该反应电子转移的方向和数目:
更新时间:2022-10-13 23:17:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:①石灰石;②Cu;③Ba(OH)2晶体;④盐酸;⑤CH4;⑥NH3;⑦NaCl固体;⑧硫酸;⑨Na2SO4溶液;⑩NaHSO4晶体
(1)能导电的是__ (填序号,下同);
(2)属于电解质的有__ ;
(3)属于非电解质的有__ ;
(4)既不是电解质,也不是非电解质的是__ 。
(1)能导电的是
(2)属于电解质的有
(3)属于非电解质的有
(4)既不是电解质,也不是非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列物质:①Na②H2O③酒精④CO2⑤NH3⑥熔融NaCl⑦Ba(OH)2⑧冰醋酸(纯净的醋酸)⑨蔗糖⑩NaHCO3溶液。属于电解质的是___________ ,属于非电解质的是___________ 。(填序号)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列10种物质: ①硫酸 ②CO2 ③Ba(OH)2固体 ④NH4Al(SO4)2固体 ⑤葡萄糖 ⑥Al ⑦氢氧化铁胶体 ⑧CH3COOH ⑨熔融氯化钾 ⑩氯水
请回答下列问题:
(1)上述物质中属于电解质的是______ (填序号),属于非电解质的是___________ (填序号),能导电的是___________ (填序号)。
(2)将①的稀溶液加入⑦中,实验现象为___________ 。
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:_____ 。
(4)久置的氯水酸性增强的原因:(化学方程式表示)___________ 。
请回答下列问题:
(1)上述物质中属于电解质的是
(2)将①的稀溶液加入⑦中,实验现象为
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:
(4)久置的氯水酸性增强的原因:(化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
⑴该反应中氧化剂是______________ ,被氧化的是________ 元素。
⑵该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为_____________
⑶用双线桥法标出电子转移的方向与数目_________________ 。
⑴该反应中氧化剂是
⑵该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为
⑶用双线桥法标出电子转移的方向与数目
您最近一年使用:0次
【推荐2】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂___________ ,还原剂___________ ;
(2)氧化产物___________ ,还原产物___________ ;
(3)用单线桥的方法表示该反应的电子转移情况___________ 。
(4)用双线桥的方法表示该反应的电子转移情况。___________ 。
(5)当有8个NH3分子参加反时,转移的电子个数为___________ 。
(1)氧化剂
(2)氧化产物
(3)用单线桥的方法表示该反应的电子转移情况
(4)用双线桥的方法表示该反应的电子转移情况。
(5)当有8个NH3分子参加反时,转移的电子个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。请回答下列问题:
(1)此反应的氧化剂是_______ ,氧化产物是_______ 。
(2)已知碳与浓硫酸在加热条件下反应生成CO2、SO2和H2O,写出该反应的化学方程式:_______ 。
Ⅱ.饮用水中的NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(3)上述反应中,被氧化的元素_______ ,还原产物是_______ 。
(4)用双线桥法表示反应中电子转移的方向和数目:_______
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(5)请配平下列离子方程式。_______
_______Fe2++_______H++_______NO =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
(1)此反应的氧化剂是
(2)已知碳与浓硫酸在加热条件下反应生成CO2、SO2和H2O,写出该反应的化学方程式:
Ⅱ.饮用水中的NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:(3)上述反应中,被氧化的元素
(4)用双线桥法表示反应中电子转移的方向和数目:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(5)请配平下列离子方程式。
_______Fe2++_______H++_______NO
 =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请你根据所学习与掌握的知识,按下列要求填空:
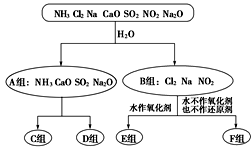
(1)上述第一级分类标准(分成A、B组的依据)是_________________________________ 。
(2)F组中物质除了Cl2外还有____________ (填化学式)。
(3)D组中的氨水呈弱碱性,用电离方程式表示其呈弱碱性的原因:___________________ 。
(4)用Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,说明理由:____________________ 。
Ⅱ.某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内:(不要求配平)_______________

(2)反应中,被还原的元素是__________ ,还原剂是_______________ 。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目:_________________


(1)上述第一级分类标准(分成A、B组的依据)是
(2)F组中物质除了Cl2外还有
(3)D组中的氨水呈弱碱性,用电离方程式表示其呈弱碱性的原因:
(4)用Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,说明理由:
Ⅱ.某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内:(不要求配平)

(2)反应中,被还原的元素是
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知硝酸与金属反应时,在不同条件下有不同的还原产物,甚至在同一反应中可同时得到多种还原产物。现有HNO3、NH4NO3、N2O、H2O、Zn、Zn(NO3)2六种物质。
(1)请利用其中五种物质组成一个完整的化学反应,写出该化学反应方程式______________ ;
(2)上述所写反应中,硝酸表现出的化学性质是_______ ,被还原的元素是_______ 。
(3)若六种物质组成一个完整的化学反应,则反应中的还原产物是_______ (填化学式),若该反应中NH4NO3与N2O物质的量之比为1︰1,那么该反应中氧化剂与还原剂的物质的量之比为________ 。
(1)请利用其中五种物质组成一个完整的化学反应,写出该化学反应方程式
(2)上述所写反应中,硝酸表现出的化学性质是
(3)若六种物质组成一个完整的化学反应,则反应中的还原产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】K2CO3有广泛的用途。
(1)钾肥草木灰中含有K2CO3、K2SO4、KCl等。将草木灰用水浸取,过滤、蒸发得浓缩液。
①该浓缩液呈碱性的原因用离子方程式表示为______ 。
②检验该浓缩液中Cl-所用的试剂有________ 。
A.AgNO3溶液 B.硝酸 C.盐酸 D.Ba(NO3)2溶液 E.BaCl2溶液
(2)工业上曾利用如下反应生产碳酸钾:K2SO4 + C + CaCO3 → K2CO3+ X+ CO2↑(未配平)
已知X为两种元素组成的化合物,则X的化学式为__________ ;反应中氧化剂与还原剂物质的量之比为________ 。
(3)离子膜电解-炭化法是目前生产碳酸钾的常用的方法。
第一步:精制KCl溶液
粗KCl中含有Ca2+、Mg2+等离子,按以下流程精制:
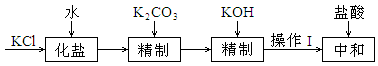
已知:加入K2CO3后,溶液中部分Mg2+转化为MgCO3沉淀。
Ksp[Mg(OH)2]=5.6×10-12,Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6。
①操作Ⅰ的名称是_________ 。
②当加入KOH后,溶液中n(CO32-)增大,主要原因是____ 。
第二步:电解精制后的KCl溶液制取KOH,其它产物制取盐酸。
第三步:将KOH与CO2反应转化为KHCO3,再将KHCO3分解得到产品。
③离子膜电解-炭化法的整个过程中,可以循环利用的物质有____ 。
(1)钾肥草木灰中含有K2CO3、K2SO4、KCl等。将草木灰用水浸取,过滤、蒸发得浓缩液。
①该浓缩液呈碱性的原因用离子方程式表示为
②检验该浓缩液中Cl-所用的试剂有
A.AgNO3溶液 B.硝酸 C.盐酸 D.Ba(NO3)2溶液 E.BaCl2溶液
(2)工业上曾利用如下反应生产碳酸钾:K2SO4 + C + CaCO3 → K2CO3+ X+ CO2↑(未配平)
已知X为两种元素组成的化合物,则X的化学式为
(3)离子膜电解-炭化法是目前生产碳酸钾的常用的方法。
第一步:精制KCl溶液
粗KCl中含有Ca2+、Mg2+等离子,按以下流程精制:

已知:加入K2CO3后,溶液中部分Mg2+转化为MgCO3沉淀。
Ksp[Mg(OH)2]=5.6×10-12,Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6。
①操作Ⅰ的名称是
②当加入KOH后,溶液中n(CO32-)增大,主要原因是
第二步:电解精制后的KCl溶液制取KOH,其它产物制取盐酸。
第三步:将KOH与CO2反应转化为KHCO3,再将KHCO3分解得到产品。
③离子膜电解-炭化法的整个过程中,可以循环利用的物质有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的KIO3,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,是电解质的是___________ ,是非电解质的是___________ 。(填序号)
(2)写出④在水中的电离方程式___________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:___________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为 。
。
(4)反应中氧化剂与还原剂的物质的量之比为___________ ,其中HNO3反应中显示出来的性质是___________ 。
(5)该反应中的氧化产物为___________ ,每生成11.2L(标准状况下)的NO,转移的电子个数为___________ 。
(6)请用双线桥标出电子转移的情况___________ 。
| 名称 | 天然气 | 白酒 | 醋酸 | 小苏打 | 熟石灰 | 铜线 | 加碘盐 |
| 主要成分 | ①CH4 | ②C2H5OH | ③CH3COOH | ④NaHCO3 | ⑤Ca(OH)2 | ⑥Cu | ⑦NaCl和KIO3混合 |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
 。
。(4)反应中氧化剂与还原剂的物质的量之比为
(5)该反应中的氧化产物为
(6)请用双线桥标出电子转移的情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO+2CO=N2+2CO2。
(1)碳元素的化合价___________ (填“升高”或“降低”),被___________ (填“氧化”或“还原”),CO是___________ 剂(填“氧化”或“还原”),NO是___________ 剂(填“氧化”或“还原”),发生___________ 反应(填“氧化”或“还原”)。
(2)用单线桥表示此反应中的电子转移情况2NO+2CO=N2+2CO2:___________ 。
(3)若反应中消耗了2molCO,则生成N2的物质的量为___________ mol,转移电子的物质的量为___________ mol。
(4)H2S与CO2在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为___________ 。
(1)碳元素的化合价
(2)用单线桥表示此反应中的电子转移情况2NO+2CO=N2+2CO2:
(3)若反应中消耗了2molCO,则生成N2的物质的量为
(4)H2S与CO2在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为
您最近一年使用:0次
【推荐3】高锰酸盐具有强氧化性,常用于杀菌消毒。
(1)已知 是一种不稳定的物质,具有强氧化性。可发生反应:
是一种不稳定的物质,具有强氧化性。可发生反应: 。
。
①配平该反应的离子方程式:_______ 。
②该反应的实验现象为_______ 。
③上述反应中,发生还原反应的粒子是_______ (写化学式),每消耗3个 ,反应转移电子的个数为
,反应转移电子的个数为_______ 。
(2)已知某容器中发生了一个化学反应,反应过程中存在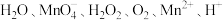 六种粒子。在反应过程中测得
六种粒子。在反应过程中测得 和
和 的粒子数目随时间变化的曲线如图所示。
的粒子数目随时间变化的曲线如图所示。
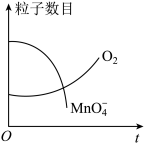
①写出该反应的离子方程式:_______ *。
②该反应中,氧化剂与还原剂的粒子数目之比为_______ 。
③若消耗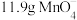 ,则生成氧气的质量为
,则生成氧气的质量为_______ 。
(3)水中的溶解氧 是水生生物生存不可缺少的条件。将水样与
是水生生物生存不可缺少的条件。将水样与 碱性悬浊液混合,反应生成
碱性悬浊液混合,反应生成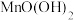 ,实现氧的固定。“氧的固定”中发生反应的化学方程式为
,实现氧的固定。“氧的固定”中发生反应的化学方程式为_______ 。
(1)已知
 是一种不稳定的物质,具有强氧化性。可发生反应:
是一种不稳定的物质,具有强氧化性。可发生反应: 。
。①配平该反应的离子方程式:
②该反应的实验现象为
③上述反应中,发生还原反应的粒子是
 ,反应转移电子的个数为
,反应转移电子的个数为(2)已知某容器中发生了一个化学反应,反应过程中存在
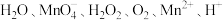 六种粒子。在反应过程中测得
六种粒子。在反应过程中测得 和
和 的粒子数目随时间变化的曲线如图所示。
的粒子数目随时间变化的曲线如图所示。
①写出该反应的离子方程式:
②该反应中,氧化剂与还原剂的粒子数目之比为
③若消耗
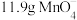 ,则生成氧气的质量为
,则生成氧气的质量为(3)水中的溶解氧
 是水生生物生存不可缺少的条件。将水样与
是水生生物生存不可缺少的条件。将水样与 碱性悬浊液混合,反应生成
碱性悬浊液混合,反应生成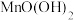 ,实现氧的固定。“氧的固定”中发生反应的化学方程式为
,实现氧的固定。“氧的固定”中发生反应的化学方程式为
您最近一年使用:0次



