某温度下,HNO2和CH3COOH的电离常数分别为 和
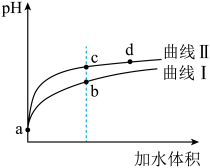
和 。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
 和
和 。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
| A.曲线Ⅰ代表HNO2溶液 |
| B.取相同体积b、c两点的溶液,分别与NaOH恰好中和后,b点对应溶液中n(Na+)更大 |
| C.取等体积a点的两种溶液,稀释到相同的pH值,CH3COOH所需水的体积更小 |
| D.相应酸的电离程度:d点>c点,溶液导电性:d点>c点 |
更新时间:2022-11-05 20:24:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随加水体积变化的曲线如图所示。下列说法正确的是


| A.HB的酸性强于HA |
| B.加水稀释到pH相同时,酸HA、HB用到的水V(A)小于V(B) |
| C.a点溶液的导电性大于b点溶液 |
| D.同浓度的NaA与NaB溶液中,c(A-)=c(B-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
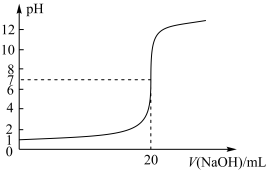

| A.用石墨电极电解熔融 Al2O3时,阳极须定期更换 |
| B.如上图所示为向10 mL一定浓度的HCl溶液中滴加NaOH溶液时,所得室温下溶液pH随NaOH溶液体积的变化,由图可知c(NaOH)=0.1 mol·L−1 |
| C.由方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol−1可知甲烷的燃烧热为890.3 kJ·mol−1 |
D.C(s)+H2O(g)  CO(g)+H2(g)在一定条件下能自发进行的原因是ΔH>0 CO(g)+H2(g)在一定条件下能自发进行的原因是ΔH>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列图示与对应的叙述相符的是( )
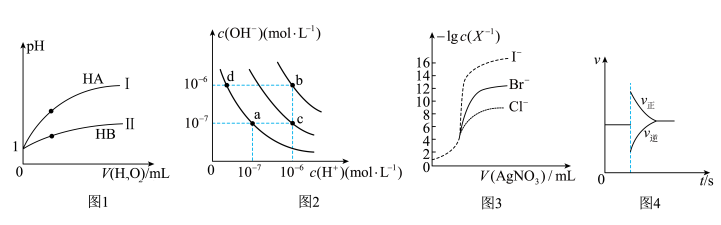

| A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+) |
| B.图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性 |
| C.用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
D.图4表示在N2(g)+3H2(g)  2NH3(g)达到平衡后,减小NH3浓度时速率的变化 2NH3(g)达到平衡后,减小NH3浓度时速率的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】稀释0.1 mol/L的醋酸溶液,其中随水的增加而增大的有
⑴H+的物质的量 ⑵ c(H+) ⑶ c(OH—) ⑷ c(H+)/c(HAc) ⑸ c(HAc)/c(Ac—)
⑴H+的物质的量 ⑵ c(H+) ⑶ c(OH—) ⑷ c(H+)/c(HAc) ⑸ c(HAc)/c(Ac—)
| A.⑴⑶⑷ | B.⑴⑶⑸ | C.⑵⑷ | D.⑶⑷ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图示与对应的叙述相符的是
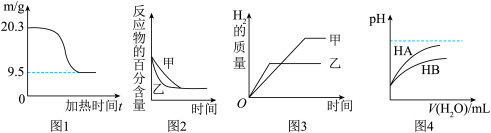

A.图1表示0.1 mol 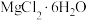 在空气中充分加热时固体质量随时间的变化 在空气中充分加热时固体质量随时间的变化 |
B.图2表示压强对可逆反应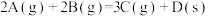 的影响,乙的压强比甲的压强大 的影响,乙的压强比甲的压强大 |
| C.若图3表示等质量的钾、钠分别与足量水反应,则甲代表钠 |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列事实能证明HCOOH为弱酸的是
A.可与 反应生成 反应生成 |
| B.导电能力低于同浓度的硫酸 |
C. 溶液可以使甲基橙变红 溶液可以使甲基橙变红 |
| D.室温时HCOONa溶液的pH大于7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】从植物花汁中提取的一种有机物HIn,可做酸碱指示剂,在水溶液中存在电离平衡:HIn(红色)  H++In-(黄色),对上述平衡解释不正确的是
H++In-(黄色),对上述平衡解释不正确的是
 H++In-(黄色),对上述平衡解释不正确的是
H++In-(黄色),对上述平衡解释不正确的是| A.升高温度平衡向正方向移动 |
| B.加入盐酸后平衡向逆方向移动,溶液显红色 |
| C.加入NaOH溶液后平衡向正方向移动,溶液显黄色 |
| D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】羟胺( )稀溶液中
)稀溶液中 的电离方程式为
的电离方程式为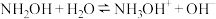 ,设
,设 的电离平衡常数为K。下列说法正确的是
的电离平衡常数为K。下列说法正确的是
 )稀溶液中
)稀溶液中 的电离方程式为
的电离方程式为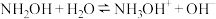 ,设
,设 的电离平衡常数为K。下列说法正确的是
的电离平衡常数为K。下列说法正确的是| A.常温下,加入少量NaOH固体,平衡向左移动,K减小 |
B.常温下,加入少量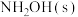 ,平衡向右移动, ,平衡向右移动, 的电离度增大 的电离度增大 |
| C.常温下,加少量水稀释,溶液中所有离子浓度都减小 |
D.常温下,通入少量HCl气体,平衡向右移动, 增大 增大 |
您最近一年使用:0次

 用于金属精制、农药、医药、催化剂再生等。室温下,关于
用于金属精制、农药、医药、催化剂再生等。室温下,关于 溶液中,下列说法正确的是
溶液中,下列说法正确的是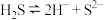
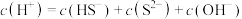
 的
的 溶液等体积混合,混合液呈碱性
溶液等体积混合,混合液呈碱性 减小
减小

