硫是一种黄色晶体。硫元素有多种化合价。仔细观察下列物质中硫的化合价及排列顺序:H2S(Na2S)、S、SO2(X、Na2SO3)、Y(H2SO4、Na2SO4)。回答下列问题:
(1)在Na2S中,硫元素的化合价是____ 。
(2)参考Y后边的表述,X是一种含氧酸,X的化学式为____ 。
(3)Y+____ =H2SO4。
(4)在反应2H2S+SO2=3S+2H2O中,氧化产物和还原产物都是S,则氧化产物和还原产物的个数比是____ 。
(5)SO2能使酸性高锰酸钾溶液紫色褪去。发生的反应如下:5SO2+2 +2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
+2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是____ 。
(1)在Na2S中,硫元素的化合价是
(2)参考Y后边的表述,X是一种含氧酸,X的化学式为
(3)Y+
(4)在反应2H2S+SO2=3S+2H2O中,氧化产物和还原产物都是S,则氧化产物和还原产物的个数比是
(5)SO2能使酸性高锰酸钾溶液紫色褪去。发生的反应如下:5SO2+2
 +2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
+2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
更新时间:2022-11-04 08:01:37
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)用双线桥表示该反应中电子转移的情况___________ 。
(2)浓盐酸在反应中显示出来的性质是___________ 。
(3)若产生标况下4.48 L Cl2,则被氧化的HCl的物质的量为__________ mol。
(1)用双线桥表示该反应中电子转移的情况
(2)浓盐酸在反应中显示出来的性质是
(3)若产生标况下4.48 L Cl2,则被氧化的HCl的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在Cl2+2NaOH=NaCl+NaClO+H2O反应中被氧化的Cl2与被还原的Cl2的分子个数之比为___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】硫循环在自然界和人类生活生产中均起到重要作用。
(1)如图是自然界中硫的循环图,下列关于这两种循环的说法正确的是_______(填字母)。
(2)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:
①SO2催化歧化反应的化学方程式是_______ ,该反应中生成1molS,转移的电子数约为_______ 。
②反应III中检验生成的二氧化硫的方法是_______ 。
③硫酸的工业生产是利用硫铁矿经沸腾炉燃烧,再经接触室转化,最后用98.3%的浓硫酸吸收而制得。写出接触室中发生反应的化学方程式:_______ ;用98.3%的浓硫酸吸收而不用水吸收的原因是_______ 。
(1)如图是自然界中硫的循环图,下列关于这两种循环的说法正确的是_______(填字母)。

| A.火山喷口附近容易见到单质硫 |
| B.硫循环过程无生物圈参与 |
| C.人类对化石燃料的过度开采对硫循环造成巨大影响 |
| D.硫循环对环境的影响是导致酸雨的产生 |
(2)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:

①SO2催化歧化反应的化学方程式是
②反应III中检验生成的二氧化硫的方法是
③硫酸的工业生产是利用硫铁矿经沸腾炉燃烧,再经接触室转化,最后用98.3%的浓硫酸吸收而制得。写出接触室中发生反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】研究表明,氮氧化物和二氧化硫等气体与雾霾的形成有关(如图所示)。

(1)过程①中NOx(x=1或2)发生_______ (填“氧化”或“还原”)反应。
(2)气体A的化学式是________ 。
(3)过程②的化学方程式是________ 。
(4)已知:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H1= -a kJ/mol
S(s)+O2(g)=SO2(g) △H2= -b kJ/mol
家庭常用燃料液化石油气中含有微量H2S,在燃烧过程中会产生SO2。该反应的热化学方程式是____________ 。

(1)过程①中NOx(x=1或2)发生
(2)气体A的化学式是
(3)过程②的化学方程式是
(4)已知:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H1= -a kJ/mol
S(s)+O2(g)=SO2(g) △H2= -b kJ/mol
家庭常用燃料液化石油气中含有微量H2S,在燃烧过程中会产生SO2。该反应的热化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】硫酸工业中热能的合理利用及三废处理
硫酸生产过程中的三个反应都是_____ ,为了充分利用这些热量,在生产过程中,沸腾炉外设置____ 回收高温废热,把__ 和转化器合为一体,将二氧化硫转化为三氧化硫时放出的热量及时导出用来__ 。
(1)废气:硫酸工业的尾气中含有的有毒气体是___ ,用___ 处理尾气的化学方程式分别为:_______________________ 、_________________________ 、_________________ 。
(2)废水:没有被污染的冷却水可以被____ ;若排出的是酸性废水,一般使用石灰乳等中和处理,反应的离子方程式为_____ 。
(3)废渣:以硫铁矿为原料生产硫酸,废渣的主要成分是____ 、硫化亚铁及少量有害物质。用废渣可以炼制的金属是____ 。
硫酸生产过程中的三个反应都是
(1)废气:硫酸工业的尾气中含有的有毒气体是
(2)废水:没有被污染的冷却水可以被
(3)废渣:以硫铁矿为原料生产硫酸,废渣的主要成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】 、氮的氧化物和
、氮的氧化物和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
(1)二氧化硫被雨水吸收后就形成了酸雨。某兴趣小组同学收集热电厂附近的雨水进行实验,测得该雨水样品的pH为4.73,且每隔1h,通过pH计测定雨水样品的pH,测得的结果如表所示。
正常雨水的pH为5.6,偏酸性,这是因为_______ 。分析上述数据变化,你认为形成这一变化的原因是_______ (用化学方程式表示)。
(2)研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如图所示。

各室中发生的反应如下:
氧化室: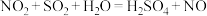
清除室:
分解室:
物质X和Y分别为_______ 、_______ (填化学式)。写出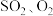 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:_______ 。
(3)生物脱 的方法除去
的方法除去 的原理如图所示。
的原理如图所示。

消耗标准状况下11.2L ,转移的电子数为
,转移的电子数为_______ 。
 、氮的氧化物和
、氮的氧化物和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:(1)二氧化硫被雨水吸收后就形成了酸雨。某兴趣小组同学收集热电厂附近的雨水进行实验,测得该雨水样品的pH为4.73,且每隔1h,通过pH计测定雨水样品的pH,测得的结果如表所示。
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(2)研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如图所示。

各室中发生的反应如下:
氧化室:
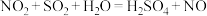
清除室:

分解室:

物质X和Y分别为
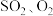 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:(3)生物脱
 的方法除去
的方法除去 的原理如图所示。
的原理如图所示。
消耗标准状况下11.2L
 ,转移的电子数为
,转移的电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】I.如图所示:在B水槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B水槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL。
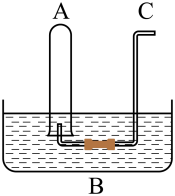
(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是___________ 。
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为___________ mol/L(设溶液的体积仍为500 mL,答案用分数表示)。
Ⅱ.向 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:
(3)沉淀A的化学式为___________ ,该沉淀能否溶于稀盐酸?___________ (填“能”或“不能”)。
(4)写出通入少量 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:___________ ,生成2.33 g沉淀B,理论上需要消耗标准状况下的
___________  。
。
(5)若将 溶液换成
溶液换成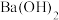 溶液,少量
溶液,少量 通入
通入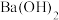 溶液中的离子方程式为
溶液中的离子方程式为___________ 。
Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为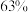 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为___________ ,加入NaOH溶液的体积为___________ mL。
(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。
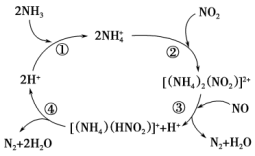
按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是___________ 。
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是___________ 。
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为___________ (忽略溶质扩散)。
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是___________ 。

(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为
Ⅱ.向
 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:(3)沉淀A的化学式为
(4)写出通入少量
 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:
 。
。(5)若将
 溶液换成
溶液换成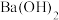 溶液,少量
溶液,少量 通入
通入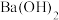 溶液中的离子方程式为
溶液中的离子方程式为Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为
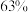 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。

按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的
 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某研究性学习小组计划研究当地酸雨的形成过程,于是取来雨水作水样进行测定,随着时间的推移,多次测定该样品的pH,得到如下数据:
(1)雨水样品放置时pH变化的主要原因是________ (用化学方程式表示)。由此可以得出酸雨的形成过程可能是_________ 。
(2)如果将刚取样的上述雨水和自来水混合,pH降低了,推测其原因是______ ,二氧化硫表现______ 性。
(3)酸雨对环境造成的危害有______ 。
A.腐蚀桥梁、雕塑等建筑物 B.污染水源 C.损害庄稼
(4)为减少酸雨的产生,可采取的措施有_______ 。
①少用煤作燃料②把工厂的烟囱造高③化石燃料脱硫④在已酸化的土壤中加石灰⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
| 时间(h) | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)雨水样品放置时pH变化的主要原因是
(2)如果将刚取样的上述雨水和自来水混合,pH降低了,推测其原因是
(3)酸雨对环境造成的危害有
A.腐蚀桥梁、雕塑等建筑物 B.污染水源 C.损害庄稼
(4)为减少酸雨的产生,可采取的措施有
①少用煤作燃料②把工厂的烟囱造高③化石燃料脱硫④在已酸化的土壤中加石灰⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】用化学用语填空
(1)氨气_______ 。
(2)氢氧化铝_______ 。
(3)乙醇_______ 。
(4)硫酸铁_______ 。
(1)氨气
(2)氢氧化铝
(3)乙醇
(4)硫酸铁
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(MgxFe2-xSiO4)。回答下列问题:基态Fe原子的价电子排布式为_______ 。橄榄石中,各元素电负性大小顺序为_______ ,铁的化合价为_______ 。
您最近一年使用:0次
【推荐3】根据题目要求回答问题:
(1)请用化学用语填空:
①氯离子的结构示意图_______
②一水合氨水溶液呈碱性的原因:_______ 。
(2)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此回答下列问题:
①该反应_______ (选填“属于”或“不属于”)氧化还原反应。
②H3PO2属于_______ (选填“一”、“二”或“三”)元酸。NaH2PO2属于____ (选填“正盐”或“酸式盐”)。
(3)火箭发射时可用肼(N2H4)作燃料,NO2作氧化剂,生成N2和H2O。写出该反应的化学方程式_______ 。
(4)在一定条件下,RO 和氟气可发生如下反应:RO
和氟气可发生如下反应:RO +F2+2OH-=RO
+F2+2OH-=RO +2F-+H2O从而可知在RO
+2F-+H2O从而可知在RO 中,元素R的化合价为
中,元素R的化合价为_______
(5)下图是在一定温度下向不同电解质溶液中加入新物质时溶液的导电性发生的变化,其电流强度(I)随新物质加入量(m)的变化曲线,若澄清石灰水中通入CO2至过量,则符合变化趋势的图为_______ 。
a. b.
b.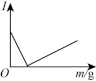 c.
c.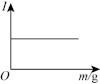
(1)请用化学用语填空:
①氯离子的结构示意图
②一水合氨水溶液呈碱性的原因:
(2)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此回答下列问题:
①该反应
②H3PO2属于
(3)火箭发射时可用肼(N2H4)作燃料,NO2作氧化剂,生成N2和H2O。写出该反应的化学方程式
(4)在一定条件下,RO
 和氟气可发生如下反应:RO
和氟气可发生如下反应:RO +F2+2OH-=RO
+F2+2OH-=RO +2F-+H2O从而可知在RO
+2F-+H2O从而可知在RO 中,元素R的化合价为
中,元素R的化合价为(5)下图是在一定温度下向不同电解质溶液中加入新物质时溶液的导电性发生的变化,其电流强度(I)随新物质加入量(m)的变化曲线,若澄清石灰水中通入CO2至过量,则符合变化趋势的图为
a.
 b.
b. c.
c.
您最近一年使用:0次

 通入浓氨水中,发生如下反应:
通入浓氨水中,发生如下反应:
 与
与

