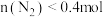向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)  2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示

下列说法正确的是
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物起始量 | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |

下列说法正确的是
| A.由图可知:T1<T2,且该反应为吸热反应 |
| B.T2时该反应的平衡常数K=0.8 |
| C.l0min内甲容器中反应的平均速率v(B)=0.025mol·(L·min)-1 |
| D.T1℃,若起始时甲容器中充入1.5molA、0.5molB,平衡时B的转化率为25% |
13-14高三上·江苏无锡·期末 查看更多[5]
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下,在三个容积相同的恒容密闭容器中按不同的方式投入反应物,发生反应 N2(g)+3H2(g) 2NH3(g) △H= -92.4kJ/mol, 测得反应的相关数据如下表:
2NH3(g) △H= -92.4kJ/mol, 测得反应的相关数据如下表:
则下列关系正确的是
 2NH3(g) △H= -92.4kJ/mol, 测得反应的相关数据如下表:
2NH3(g) △H= -92.4kJ/mol, 测得反应的相关数据如下表:| 容器甲 | 容器乙 | 容器丙 | |
| 反应温度/℃ | 400 | 400 | 500 |
| 反应物投入量 | 1molN2,3molH2 | 4molNH3 | 1molN2,3molH2 |
| 平衡时v(正)(H2)/mol/(L·s) | v1 | v2 | v3 |
| 平衡时c(NH3)/(mol/L) | c1 | c2 | c3 |
| 平衡时总压强P/Pa | P1 | P2 | P3 |
| 物质的平衡转化率a | a1(N2) | a2(NH3) | a3(N2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c1<2c2 | B.c2>2c3,a2(NH3)+a3(N2)<1 |
| C.K1>K3, P2>2P3 | D.v1<v3,a1(N2)<a3(N2) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在某温度下,向三个初始体积均为 的密闭容器中按下表所示投料,发生反应:
的密闭容器中按下表所示投料,发生反应: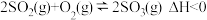 。下列说法不正确的是
。下列说法不正确的是
 的密闭容器中按下表所示投料,发生反应:
的密闭容器中按下表所示投料,发生反应: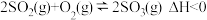 。下列说法不正确的是
。下列说法不正确的是容器编号 | 容器类型 | 起始物质的量/ | 平衡时 | ||
|
|
| |||
Ⅰ | 恒温恒容 | 2 | 1 | 0 | 1.8 |
Ⅱ | 绝热恒容 | 0 | 0 | 2 | a |
Ⅲ | 恒温恒压 | 2 | 1 | 0 | b |
A.容器Ⅰ中 转化率小于容器Ⅲ中 转化率小于容器Ⅲ中 的转化率 的转化率 |
B.容器Ⅲ平衡体系中保持容器压强不变,充入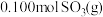 ,新平衡后 ,新平衡后 浓度未变 浓度未变 |
C.平衡时 的物质的量: 的物质的量: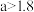 、 、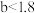 |
D.若容器Ⅰ中有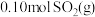 、 、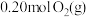 和 和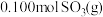 ,则此时 ,则此时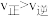 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
下列说法正确的是
| 容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
| CO(g) | SO2(g) | S(g) | CO2(g) | ||
| 甲 | 1 | 0.5 | 0.5 | 1 | a |
| 乙 | 1 | 0.5 | 0 | 0 | 0.2 |
| 丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
| A.平衡常数:K甲>K乙 |
| B.a=0.4 |
| C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005mol•L-1•min-1 |
| D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知 是煤液化的一个反应,在温度
是煤液化的一个反应,在温度 和
和 时将
时将 和
和 充入
充入 密闭容器中测得
密闭容器中测得 随时间(s)的变化如下表
随时间(s)的变化如下表
下列说法正确的是
 是煤液化的一个反应,在温度
是煤液化的一个反应,在温度 和
和 时将
时将 和
和 充入
充入 密闭容器中测得
密闭容器中测得 随时间(s)的变化如下表
随时间(s)的变化如下表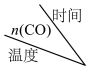 | 0 | 10 | 20 | …… | 40 | 50 |
 | 1.0 | 0.7 | 0.5 | …… | 0.25 | 0.25 |
 | 1.0 | 0.65 | 0.4 | …… | 0.28 | 0.28 |
A. 温度下平衡后恒容再充入 温度下平衡后恒容再充入 ,重新平衡后 ,重新平衡后 总的转化率与 总的转化率与 的相等 的相等 |
B. 温度下 温度下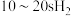 的反应速率为 的反应速率为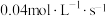 |
C.恒温,恒容条件下,通入等物质的量的反应物,当 的体积分数不变时,该反应达到了平衡状态。 的体积分数不变时,该反应达到了平衡状态。 |
D. 温度下平衡后恒定压强不变充入 温度下平衡后恒定压强不变充入 的体积分数不变 的体积分数不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】相同温度下,体积均为1 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
下列叙述不正确的是
 2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| (1) | 2 | 3 | 0 | 27.78 kJ |
| (2) | 1.6 | 1.8 | 0.8 | Q |
| A.容器(1)(2)中反应达平衡时压强相等 |
| B.容器(2)中反应开始时v(正)>v(逆) |
| C.容器(2)中反应达平衡时,吸收的热量Q为9.26 kJ |
| D.容器(1)中反应达平衡时若移走1 mol N2和1.5 mol H2,再次达到新平衡时n(NH3)<0.3 mol |
您最近一年使用:0次



 与
与 。
。 ,向
,向 和
和 ,一定条件下测得
,一定条件下测得 的物质的量随时间变化关系如表所示:
的物质的量随时间变化关系如表所示:
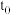




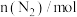

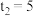 ,则
,则 内
内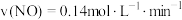
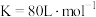
 和
和