某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
下列说法正确的是
| 容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
| CO(g) | SO2(g) | S(g) | CO2(g) | ||
| 甲 | 1 | 0.5 | 0.5 | 1 | a |
| 乙 | 1 | 0.5 | 0 | 0 | 0.2 |
| 丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
| A.平衡常数:K甲>K乙 |
| B.a=0.4 |
| C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005mol•L-1•min-1 |
| D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2 |
更新时间:2020-03-27 20:17:04
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa,已知:分压=总压×该组分物质的量分数),各物质的分压随时间的变化曲线如图所示。下列说法不正确的是
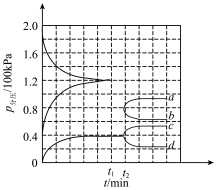

| A.若保持容器体积不变,氨气分压不变可说明反应已达平衡状态 |
B.若保持容器体积不变,用H2浓度变化表示0~t1时间内的反应速率v(H2)= 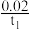 mol·L-1·min-1 mol·L-1·min-1 |
| C.t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是d |
| D.若保持容器体积不变,t2时充入He,反应仍处于平衡状态,氨气的分压保持不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在T℃时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g)⇌HCHO(g)+H2O(g) ;∆H<0,若起始时容器内气体压强为1.2 kPa,达到平衡时,HCHO的分压与起始的 关系如图所示:下列说法不正确的是
关系如图所示:下列说法不正确的是
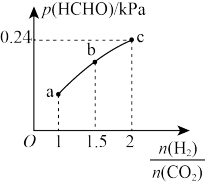
 关系如图所示:下列说法不正确的是
关系如图所示:下列说法不正确的是
| A.b点的化学平衡常数KP≈3.5 |
| B.容器内H2O的体积分数保持不变,说明达到平衡状态 |
C.若5min到达c点,则v(H2)= 0.24mol L-1 L-1 min-1 min-1 |
| D.c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,α(H2)增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知反应:2NO(g)+2H2(g)  N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
下列说法中不正确的是
 N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。| 实验数据 | 初始浓度(mol·L-1) | 生成N2的初始速率(mol·L-1·s-1) | |
| c(NO) | c(H2) | ||
| 1 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
| 2 | 1.00×10-3 | 6.00×10-3 | 4.80×10-4 |
| 3 | 2.00×10-3 | 3.00×10-3 | 9.60×10-4 |
| A.关系式中x=2、y=1 |
| B.800℃时,k的值为8×104 |
| C.反应体系的二种物质中,H2(g)的浓度对反应速率影响更大 |
| D.当其他条件不变时,升高温度,速率常数将增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】某温度下,H2 (g) + CO2 (g)⇌H2O(g) + CO(g) (ΔH>0)的平衡常数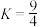 ,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:
,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:
下列判断有错的是
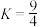 ,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:
,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:| 起始浓度(mol/L) | 甲 | 乙 | 丙 | 丁 |
| c(H2) | 0.01 | 0.02 | 0.02 | 0.005 |
| c(CO2) | 0.01 | 0.01 | 0.02 | 0.005 |
| c(H2O) | 0 | 0 | 0 | 0.005 |
| c(CO) | 0 | 0 | 0 | 0.005 |
| A.平衡时,乙中CO2的转化率>60% |
B.平衡时,四容器中甲的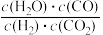 值最小 值最小 |
| C.起始时丁向正反应方向进行 |
| D.反应开始时,丙中反应速率最快 |
您最近一年使用:0次
【推荐2】一定温度下,在一个容积为1 L的密闭容器中,充入1 mol X(g)和1 mol Y(g),发生反应X(g)+Y(g)  2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
 X(g)+
X(g)+ Y(g),则下列判断正确的是
Y(g),则下列判断正确的是
 2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
 X(g)+
X(g)+ Y(g),则下列判断正确的是
Y(g),则下列判断正确的是| A.后一反应的平衡常数为1 |
| B.后一反应的平衡常数为0.5 |
| C.后一反应达到平衡时,X的平衡浓度为0.25 mol·L-1 |
| D.后一反应达到平衡时,Z的分解率为25% |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】T℃时,CaCO3(s) CaO(s)+CO2(g)在密闭容器中达到平衡时的体积为100mL,已知CaO(s)和CaCO3(s)的密度分别为:3.35g•cm-3、2.93g•cm-3,下列有关说法正确的是
CaO(s)+CO2(g)在密闭容器中达到平衡时的体积为100mL,已知CaO(s)和CaCO3(s)的密度分别为:3.35g•cm-3、2.93g•cm-3,下列有关说法正确的是
 CaO(s)+CO2(g)在密闭容器中达到平衡时的体积为100mL,已知CaO(s)和CaCO3(s)的密度分别为:3.35g•cm-3、2.93g•cm-3,下列有关说法正确的是
CaO(s)+CO2(g)在密闭容器中达到平衡时的体积为100mL,已知CaO(s)和CaCO3(s)的密度分别为:3.35g•cm-3、2.93g•cm-3,下列有关说法正确的是| A.恒温、恒容,体系中再加入56gCaO(s),平衡不移动 |
| B.恒温,压缩容器体积,达到平衡后,化学反应速率加快 |
| C.恒温、恒压,体系中再加入100gCaCO3(s),平衡常数不变 |
| D.恒温、恒压,体系中通入一定量N2,平衡正向移动,建立新的平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】异丁醇催化脱水制备异丁烯主要涉及以下2个反应。研究一定压强下不同含水量的异丁醇在恒压反应器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如图。
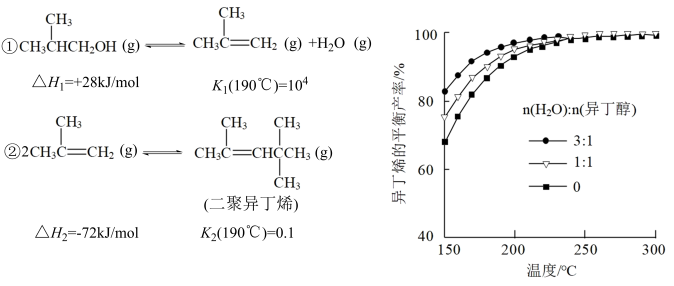
| A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备 |
B.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是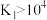 、 、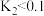 |
C.190℃时,增大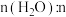 (异丁醇),不利于反应②的进行 (异丁醇),不利于反应②的进行 |
D.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度 与流出物质浓度c之间存在: 与流出物质浓度c之间存在: (异丁醇)=c(异丁烯)+2c(二聚异丁烯) (异丁醇)=c(异丁烯)+2c(二聚异丁烯) |
您最近一年使用:0次

 进行投料,发生反应
进行投料,发生反应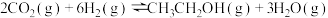
 ,在
,在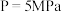 时测得不同温度下平衡体系中各种物质的体积分数(V/%)如图所示,下列说法中正确的是
时测得不同温度下平衡体系中各种物质的体积分数(V/%)如图所示,下列说法中正确的是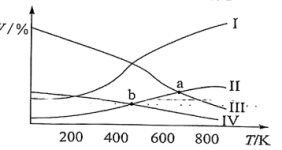
 组分的曲线是Ⅱ
组分的曲线是Ⅱ 转化率为40%
转化率为40%
 I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是
I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是


