已知反应:2NO(g)+2H2(g)  N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
下列说法中不正确的是
 N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。
N2(g)+2H2O(g)生成N2的速率与NO、H2的初始浓度的关系为v=kcx(NO)•cy(H2),k为速率常数。在800℃时测得的相关数据如表所示。| 实验数据 | 初始浓度(mol·L-1) | 生成N2的初始速率(mol·L-1·s-1) | |
| c(NO) | c(H2) | ||
| 1 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
| 2 | 1.00×10-3 | 6.00×10-3 | 4.80×10-4 |
| 3 | 2.00×10-3 | 3.00×10-3 | 9.60×10-4 |
| A.关系式中x=2、y=1 |
| B.800℃时,k的值为8×104 |
| C.反应体系的二种物质中,H2(g)的浓度对反应速率影响更大 |
| D.当其他条件不变时,升高温度,速率常数将增大 |
更新时间:2023-11-04 09:26:48
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】α—萘磺酸(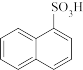 )和β—萘磺酸(
)和β—萘磺酸(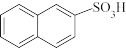 )是重要的化工原料,合成时往往得到两者的混合物,工业上相关的合成反应如图。有关说法错误的是
)是重要的化工原料,合成时往往得到两者的混合物,工业上相关的合成反应如图。有关说法错误的是
反应①: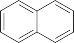 +H2SO4=
+H2SO4=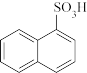 +H2O ΔH1<0 K1
+H2O ΔH1<0 K1
反应②: +H2SO4=
+H2SO4=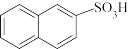 +H2O △H2<0 K2
+H2O △H2<0 K2
 )和β—萘磺酸(
)和β—萘磺酸( )是重要的化工原料,合成时往往得到两者的混合物,工业上相关的合成反应如图。有关说法错误的是
)是重要的化工原料,合成时往往得到两者的混合物,工业上相关的合成反应如图。有关说法错误的是反应①:
 +H2SO4=
+H2SO4= +H2O ΔH1<0 K1
+H2O ΔH1<0 K1反应②:
 +H2SO4=
+H2SO4= +H2O △H2<0 K2
+H2O △H2<0 K2| A.若主要产物是α—萘磺酸,说明反应①活化能比②小 |
B.平衡时α—萘磺酸和β—萘磺酸的物质的量浓度关系为 = = |
C.在密闭容器中加入萘与硫酸,tmin后反应达到平衡,用萘磺酸表示的反应速率为 |
| D.α—萘磺酸与β—萘磺酸能相互转化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】研究发现燃煤脱硫过程中生成的 CaSO₄(s) 与 CO(g) 在密闭体系中将发生如下反应:
Ⅰ.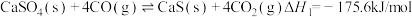
Ⅱ.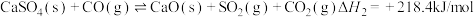
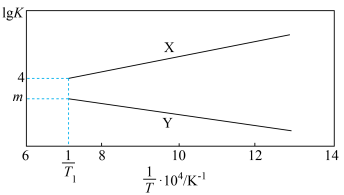
已知图为反应Ⅰ和反应Ⅱ的平衡常数(K) 与温度(T) 的变化关系。现维持温度为 T1,往某2L刚性密闭反应器中投入足量的CaSO4(s) 和1mol CO(g),经t小时反应体系达到平衡,此时体系压强为原来的1.4倍。下列说法正确的是
Ⅰ.
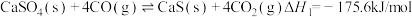
Ⅱ.
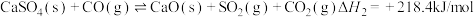
已知图为反应Ⅰ和反应Ⅱ的平衡常数(K) 与温度(T) 的变化关系。现维持温度为 T1,往某2L刚性密闭反应器中投入足量的CaSO4(s) 和1mol CO(g),经t小时反应体系达到平衡,此时体系压强为原来的1.4倍。下列说法正确的是

A.若用生石灰固硫的反应为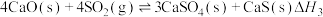 ,则 ,则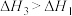 |
B.提高反应体系的温度能降低反应体系中 的生成量 的生成量 |
C.反应体系中 CO 的消耗速率为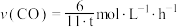 |
| D.m≈0.3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
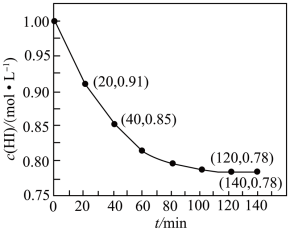
【推荐3】HI常用作有机反应中的还原剂,受热会发生分解反应。已知443℃时:2HI(g) H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
 H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
| A.0~20min内的平均反应速率可表示为v(H2)=0.0045mol·L-1·min-1 |
| B.升高温度,再次平衡时,c(HI)>0.78mol·L-1 |
C.该反应的化学平衡常数计算式为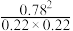 |
| D.反应进行40 min时,体系吸收的热量约为0.94kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列操作能达到相应实验目的的是
| 实验操作 | 实验目的 | |
| A | 向等体积、等pH的两种酸溶液HA和HB中分别加入足量锌粉,充分反应后,HA溶液产生更多的氢气 | 说明Ka(HA)>Ka(HB) |
| B | 向5mL0.1mol/LCuSO4溶液中先加入2mL0.4mol/LNaOH溶液,再加入1mL0.1mol/LNa2S溶液 | 探究常温下Ksp[Cu(OH)2]>Ksp(CuS) |
| C | 向滴有酚酞的碳酸钠溶液中加入适量BaCl2固体,溶液颜色变浅 | 说明碳酸钠溶液中存在水解平衡 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验能达到预期目的是
| 实验内容 | 实验目的 | |
| A | 将0.2mol·L-1的KI溶液和0.05mol·L-1的FeCl3溶液等体积混合,充分反应后,取少许混合液滴加AgNO3溶液 | 验证Fe3+与I−的反应有一定限度 |
| B | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴入几滴K3[Fe(CN)6]溶液 | 验证该过程是否发生原电池反应 |
| C | 相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 | 探究FeCl3对H2O2分解速率的影响 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下述实验不能达到预期实验目的的是
序号 | 实验内容 | 实验目的 |
A | 将2.5g CuSO4•5H2O溶解在97.5g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 室温下,用pH试纸测定浓度为0.1mol•L-1 NaClO溶液和0.1mol•L-1 CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



