设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.34g 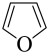 中含有的极性键数目为2 中含有的极性键数目为2 |
B.通常条件下,46g二氧化氮与四氧化二氮的混合气体中的原子数为3 |
C.50mL 18.4 浓硫酸与足量铜微热反应,生成 浓硫酸与足量铜微热反应,生成 分子的数目为0.46 分子的数目为0.46 |
D.在含4mol Si-O键的石英晶体中,氧原子的数目为4 |
22-23高三上·辽宁·期中 查看更多[8]
四川省绵阳南山中学2023-2024学年高三上学期12月月考理综试题江苏省盐城市响水中学2023-2024学年高二上学期期中考试化学(选修)试题(已下线)第03练 阿伏加德罗常数(NA)及其应用-2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题03 突破阿伏加德罗常数正误判断(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)辽宁省沈阳市第十中学2022-2023学年高二上学期期末综合测评化学试题(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷山东省曹县第一中学2023届高三上学期12月月考化学试题辽宁省六校2022-2023学年高三上学期期中联考化学试题
更新时间:2022/11/16 19:33:00
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】设NA为阿伏伽德罗常数值。下列有关叙述正确的是
| A.标准状况下,22.4LCCl4中含有的共价键数为4NA |
| B.0.2mol SO2和0.lmolO2在一定条件下充分反应后,混合物的分子数为0.2NA |
| C.常温下,3.2g由S2、S4、S8组成的混合物中含硫原子数为0.1NA |
| D.1mol/L Na2CO3溶液中含有CO32-的数目一定小于NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.标准状况下,22.4 L二氯甲烷的分子数约为NA个 |
| B.在常温常压下,2.24LSO2与O2混合气体中所含氧原子数为0.2NA |
| C.17.6 g丙烷中所含的共价键为4NA个 |
| D.将标况下11.2L的Cl2通入水中转移的电子数目为0.5NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.6gSiO2晶体中所含硅氧键数目约为0.2NA |
| B.0.5molC2H4和C3H4O2的混合物完全燃烧,消耗O2分子数目为1.5NA |
| C.将0.1mol甲烷和0.1molCl2混合光照,生成一氯甲烷的分子数为0.1NA |
| D.标准状况下,22.4L氯气通入水中,n(HClO)+n(Cl-)+n(ClO-)=2NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1 L 0.1 mol/L乙醇溶液中存在的共价键总数为0.8 |
B.5 g  和 和 的混合物发生热核聚变反应: 的混合物发生热核聚变反应: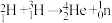 ,净产生的中子( ,净产生的中子( )数为 )数为 |
C.1 L 1 mol/L的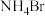 溶液中通入适量氨气后呈中性,此时溶液中 溶液中通入适量氨气后呈中性,此时溶液中 的数目为 的数目为 |
D.将0.1 mol  完全溶于水中,所得到溶液中 完全溶于水中,所得到溶液中 、 、 、HClO、ClO的粒子数之和为0.2 、HClO、ClO的粒子数之和为0.2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】用NA表示阿伏伽德罗常数的值,下列叙述中正确的是
① 31g白磷中含有1.5NA个P-P
② 1L0.1 mol/L的Na2CO3溶液中含阴离子总数为0.1NA个
③ 标准状况下,22.4L HF含NA个分子
④ 电解精炼铜时转移了NA个电子,阳极溶解32g铜
⑤ 标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA
⑥ 常温下,含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数小于0.1 NA
⑦ 142g Na2SO4 和Na2HPO4 固体混合物中,阴、阳离子总数为3NA
⑧ NA个Fe(OH)3胶体粒子的质量为107g
① 31g白磷中含有1.5NA个P-P
② 1L0.1 mol/L的Na2CO3溶液中含阴离子总数为0.1NA个
③ 标准状况下,22.4L HF含NA个分子
④ 电解精炼铜时转移了NA个电子,阳极溶解32g铜
⑤ 标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA
⑥ 常温下,含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数小于0.1 NA
⑦ 142g Na2SO4 和Na2HPO4 固体混合物中,阴、阳离子总数为3NA
⑧ NA个Fe(OH)3胶体粒子的质量为107g
| A.①④⑧ | B.①⑥⑦ | C.③⑤⑦ | D.①⑥⑧ |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】向 和
和 的混合物中加入某浓度的稀硫酸
的混合物中加入某浓度的稀硫酸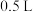 ,固体物质完全反应,生成
,固体物质完全反应,生成 和
和 。在所得溶液中加入
。在所得溶液中加入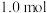
 的
的 溶液
溶液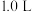 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是
 和
和 的混合物中加入某浓度的稀硫酸
的混合物中加入某浓度的稀硫酸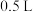 ,固体物质完全反应,生成
,固体物质完全反应,生成 和
和 。在所得溶液中加入
。在所得溶液中加入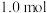
 的
的 溶液
溶液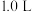 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是A. 与 与 的物质的量之比为 的物质的量之比为 |
B.硝酸的物质的量浓度为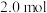  |
C.产生的 在标准状况下的体积为 在标准状况下的体积为 |
D. 、 、 与硝酸反应后剩余 与硝酸反应后剩余 为 为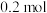 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知有下列三个反应:① 、②
、② 、③
、③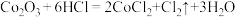 。下列有关说法正确的是
。下列有关说法正确的是
 、②
、② 、③
、③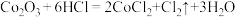 。下列有关说法正确的是
。下列有关说法正确的是A.反应①②③中的氧化产物分别是 、 、 、 、 |
B.根据以上化学方程式可以得到氧化性的强弱是 |
C.由上推理可得: |
D.在反应③中有1mol 生成,则被还原的HCl为2mol 生成,则被还原的HCl为2mol |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列物质中,既有离子键又有非极性键的化合物是
| A.NH4Cl | B.Na2O2 | C.CO2 | D.MgCl2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列说法中错误的是
① 键与
键与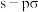 键的对称性不同;②
键的对称性不同;②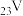 电子排布式
电子排布式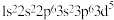 违反了洪特规则;③原子最外层电子排布为
违反了洪特规则;③原子最外层电子排布为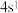 的元素一定是s区元素;④霓虹灯光、激光、荧光都与原子核外电子跃迁吸收能量有关;⑤
的元素一定是s区元素;④霓虹灯光、激光、荧光都与原子核外电子跃迁吸收能量有关;⑤ 和
和 分子中心原子的杂化轨道类型相同;⑥1个N原子最多只能与3个H原子结合形成
分子中心原子的杂化轨道类型相同;⑥1个N原子最多只能与3个H原子结合形成 分子,是由共价键的饱和性决定的
分子,是由共价键的饱和性决定的
①
 键与
键与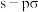 键的对称性不同;②
键的对称性不同;②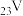 电子排布式
电子排布式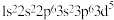 违反了洪特规则;③原子最外层电子排布为
违反了洪特规则;③原子最外层电子排布为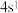 的元素一定是s区元素;④霓虹灯光、激光、荧光都与原子核外电子跃迁吸收能量有关;⑤
的元素一定是s区元素;④霓虹灯光、激光、荧光都与原子核外电子跃迁吸收能量有关;⑤ 和
和 分子中心原子的杂化轨道类型相同;⑥1个N原子最多只能与3个H原子结合形成
分子中心原子的杂化轨道类型相同;⑥1个N原子最多只能与3个H原子结合形成 分子,是由共价键的饱和性决定的
分子,是由共价键的饱和性决定的| A.3个 | B.4个 | C.5个 | D.6个 |
您最近半年使用:0次


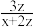

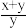
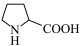 )催化某羟醛缩合反应的机理如图所示。下列说法错误的是
)催化某羟醛缩合反应的机理如图所示。下列说法错误的是
 键和π键的断裂和形成
键和π键的断裂和形成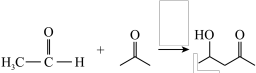
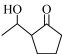
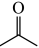 )替换环戊酮(
)替换环戊酮( ),反应可得到
),反应可得到