下图是实验室制备氯气并进行一系列相关实验的装置(加热和夹持仪器已省略)。
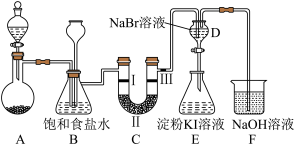
(1)用来盛放浓盐酸的仪器的名称是_______ ,装置A选用二氧化锰固体和浓盐酸在加热条件下制备氯气,反应的化学方程式为_______ 。
(2)装置C可验证干燥的氯气没有漂白性,则装置C中II的作用是_______ ,I与III是干燥的有色布条,描述I、III处的现象:_______ 。
(3)E 中实验现象为_______ 。

(1)用来盛放浓盐酸的仪器的名称是
(2)装置C可验证干燥的氯气没有漂白性,则装置C中II的作用是
(3)E 中实验现象为
更新时间:2022/11/19 08:46:01
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为了更深刻地认识卤素的性质,某化学小组对卤素的制备和性质进行如下探究实验,根据实验回答问题。
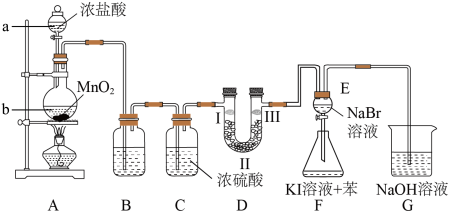
(1)仪器b的名称是__________ ,装置A制取氯气的化学方程式为________________ 。
(2)浓盐酸在反应中显示出来的性质是______________ ,若产生0.5 mol Cl2则被氧化的HCl____ mol,转移电子数约为____ 个(NA表示阿伏加德罗常数)
(3)装置D的作用是验证氯气是否具有漂白性,为此D中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是_____ (填字母编号)。
(4)装置F的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开E中活塞,将装置E中少量溶液加入装置F中,振荡,观察到的现象是_______________________ ,该现象______ (填“能”或“不能”)说明溴单质的氧化性强于碘单质,原因是_____________ 。
(5)实验室也可以用高锰酸钾和浓盐酸反应来制备氯气,将反应的化学方程式配平:__________ 。
KMnO4+ HCl(浓)= KCl + MnCl2+ Cl2↑ + H2O,有126. 4 g的KMnO4参加反应,若将生成的氯气全部通入足量的石灰乳中,理论上可得到次氯酸钙的质量为_____ g;制得的漂白粉应密封保存否则容易失效,其失效的原因是_______________ 。(用化学方程式表示)

(1)仪器b的名称是
(2)浓盐酸在反应中显示出来的性质是
(3)装置D的作用是验证氯气是否具有漂白性,为此D中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水氯化钙 | 湿润的有色布条 |
| c | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)装置F的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开E中活塞,将装置E中少量溶液加入装置F中,振荡,观察到的现象是
(5)实验室也可以用高锰酸钾和浓盐酸反应来制备氯气,将反应的化学方程式配平:
KMnO4+ HCl(浓)= KCl + MnCl2+ Cl2↑ + H2O,有126. 4 g的KMnO4参加反应,若将生成的氯气全部通入足量的石灰乳中,理论上可得到次氯酸钙的质量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某小组使用如图装置制取并收集干燥、纯净的氯气,反应的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,请回答问题:
MnCl2+Cl2↑+2H2O,请回答问题:
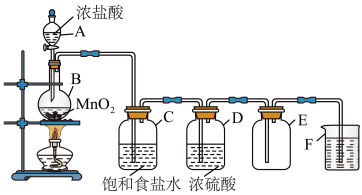
(1)装置中仪器A的名称是__ 。
(2)反应中MnO2为__ (填“氧化剂”或“还原剂”),1molMnO2中含__ molMn原子,__ 个氧原子(用NA表示阿伏加德罗常数的值)。
(3)F中盛放的是NaOH溶液,写出F装置中反应的离子方程式:__ 。
(4)装置C的作用是___ ,装置D的作用是___ 。
 MnCl2+Cl2↑+2H2O,请回答问题:
MnCl2+Cl2↑+2H2O,请回答问题:
(1)装置中仪器A的名称是
(2)反应中MnO2为
(3)F中盛放的是NaOH溶液,写出F装置中反应的离子方程式:
(4)装置C的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某实验活动小组设计了如下反应装置制备无水氯化铝,已知无水氯化铝易潮解,遇水蒸气产生大量白雾,在标压下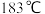 升华,经冷却后可凝华为固体。
升华,经冷却后可凝华为固体。
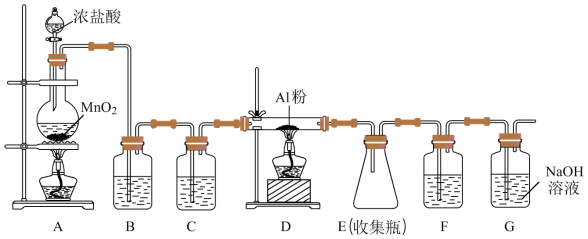
请回答:
(1)盛装浓盐酸的仪器的名称是:___________ ,向其中加入如图所示的浓盐酸,其物质的量浓度是___________  。
。
(2)装置B的作用是___________ ,装置F中盛放___________ 。
(3)请写出装置A中发生的化学方程式___________ ,D中反应的化学方程式___________ G中反应的离子方程式___________ 。
(4)某学习小组用下图装置研究气体X的性质,气体X的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:
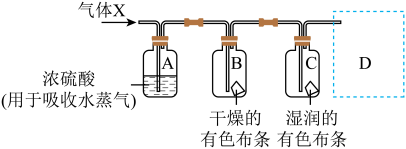
分别描述B、C装置中的现象:B___________ ,C___________ ,从物质性质说明B、C装置中现象不同的原因:___________ 。
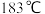 升华,经冷却后可凝华为固体。
升华,经冷却后可凝华为固体。
请回答:
(1)盛装浓盐酸的仪器的名称是:
 。
。| 盐酸 化学式:  相对分子质量:36.5 外观:合格 密度:   的质量分数:36.5% 的质量分数:36.5%符合  |
(2)装置B的作用是
(3)请写出装置A中发生的化学方程式
(4)某学习小组用下图装置研究气体X的性质,气体X的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:

分别描述B、C装置中的现象:B
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。某同学利用高浓度的NaClO溶液和(CNO)3H3固体,在10 ℃时反应制备二氯异氰尿酸钠,实验装置如下图所示(部分夹持装置略)。
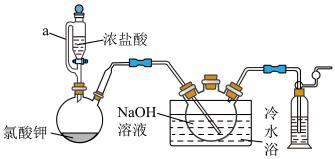
已知:2NaClO+(CNO)3H3=(CNO)3Cl2Na+NaOH+H2O。
回答下列问题:
(1)仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是___________ 。
(2)待装置B中液面上方有黄绿色气体时,可从三颈烧瓶上口加入(CNO)3H3固体,反应过程中仍需不断通入Cl2的理由是___________ 。
(3)反应结束后,装置B中的浊液经过滤、___________ 、干燥得粗产品。上述装置存在一处缺陷会导致装置B中NaOH利用率降低,改进的方法是___________ 。
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,I2+2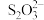 =
=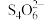 +2I-。
+2I-。
实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为V mL。
①滴定终点现象为___________ 。
②该样品的有效氯含量表达式为___________ 。
(该样品的有效氯= )
)

已知:2NaClO+(CNO)3H3=(CNO)3Cl2Na+NaOH+H2O。
回答下列问题:
(1)仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是
(2)待装置B中液面上方有黄绿色气体时,可从三颈烧瓶上口加入(CNO)3H3固体,反应过程中仍需不断通入Cl2的理由是
(3)反应结束后,装置B中的浊液经过滤、
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,I2+2
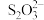 =
=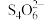 +2I-。
+2I-。实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为V mL。
①滴定终点现象为
②该样品的有效氯含量表达式为
(该样品的有效氯=
 )
)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】 是安全高效的灭菌消毒剂,下图是实验室制备较纯净的
是安全高效的灭菌消毒剂,下图是实验室制备较纯净的 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。

已知:①通常情况下, 是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
②氯气和二氧化氯的沸点。
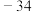 ℃
℃  11℃。
11℃。
(1)导管a的作用是___________ 。装置b的名称为___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)为制得纯净的氯气,B、C中试剂依次为___________ 、___________ 。(填名称)
(4)D为 的发生装置。化学方程式为
的发生装置。化学方程式为___________ 。
(5)E中装置选择___________ (填“G”或“H”)。

 是安全高效的灭菌消毒剂,下图是实验室制备较纯净的
是安全高效的灭菌消毒剂,下图是实验室制备较纯净的 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。
已知:①通常情况下,
 是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。②氯气和二氧化氯的沸点。

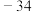 ℃
℃  11℃。
11℃。(1)导管a的作用是
(2)A中发生反应的离子方程式为
(3)为制得纯净的氯气,B、C中试剂依次为
(4)D为
 的发生装置。化学方程式为
的发生装置。化学方程式为(5)E中装置选择

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置。
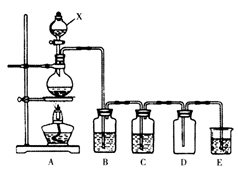
请按要求回答下列问题:
(1)仪器X的名称为_________________ 。
(2)已知装置B中选用的试剂为饱和食盐水,其作用为___________________ 。
(3)将氯气通入紫色石蕊试液C中可以观察到的现象是________________________ 。
(4)装置E中装有NaOH溶液,该装置中反应的化学方程式_________________________ 。

请按要求回答下列问题:
(1)仪器X的名称为
(2)已知装置B中选用的试剂为饱和食盐水,其作用为
(3)将氯气通入紫色石蕊试液C中可以观察到的现象是
(4)装置E中装有NaOH溶液,该装置中反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】I、实验室常用二氧化锰和浓盐酸反应制备氯气,用如图装置可制备纯净、干燥的氯气,并验证其部分性质。
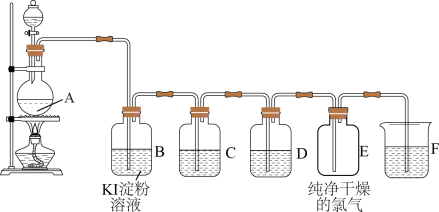
(1)A中发生反应的离子方程式是___________ 。
(2)C、D中所用试剂分别是:___________ 。
(3)B中出现的现象是___________ 。
(4)请用离子方程式表示F中 溶液的作用
溶液的作用___________ 。
Ⅱ、某兴趣小组拟利用如图装置探究验证干燥的 和潮湿的
和潮湿的 有无漂白性。
有无漂白性。
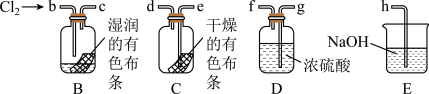
(5)按气体从左向右流向将各装置依次连接起来(填接口标号): 接b
接b___________ 。
(6)通入 后,集气瓶B、C中红色布条的现象分别是
后,集气瓶B、C中红色布条的现象分别是___________ 。

(1)A中发生反应的离子方程式是
(2)C、D中所用试剂分别是:
(3)B中出现的现象是
(4)请用离子方程式表示F中
 溶液的作用
溶液的作用Ⅱ、某兴趣小组拟利用如图装置探究验证干燥的
 和潮湿的
和潮湿的 有无漂白性。
有无漂白性。
(5)按气体从左向右流向将各装置依次连接起来(填接口标号):
 接b
接b(6)通入
 后,集气瓶B、C中红色布条的现象分别是
后,集气瓶B、C中红色布条的现象分别是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】“速力菲”(主要成分:琥珀酸亚铁)是一种常见的补铁药物。某兴趣小组为了测定“速力菲”药片中铁元素的含量,设计如下实验(假设反应过程无铁元素损耗):

请回答下列问题:
(1)研细的目的是_______ 。
(2)加入盐酸后溶液为淡黄色,说明“速力菲”中的 已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有
已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)设计实验证明淡黄色溶液中是否含有
_______ 。
(4)淡黄色溶液中加入氯水,发生反应的离子方程式为_______ 。
(5)“速力菲”药片中铁元素的含量力_______ (用含有a、b的式子表示)。

请回答下列问题:
(1)研细的目的是
(2)加入盐酸后溶液为淡黄色,说明“速力菲”中的
 已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有
已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有(3)设计实验证明淡黄色溶液中是否含有

(4)淡黄色溶液中加入氯水,发生反应的离子方程式为
(5)“速力菲”药片中铁元素的含量力
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氨气在工农业生产中有重要应用。某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。
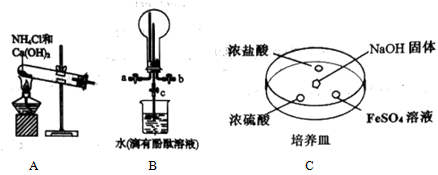
(1)实验室用装置A制备氨气的化学方程式为___________ 。
(2)用装置B收集氨气时,进气口是___________ (选填“a”或“b”)。打开装置B中的活塞c,烧瓶内产生了红色喷泉,则说明氨具有的性质是___________ ,___________ 。
(3)向C中 固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ ,检验白烟中阴离子的方法是___________ 。 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有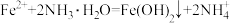 和
和___________ 。

(1)实验室用装置A制备氨气的化学方程式为
(2)用装置B收集氨气时,进气口是
(3)向C中
 固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有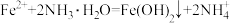 和
和
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(内置有铁粉)。请回答下列问题:
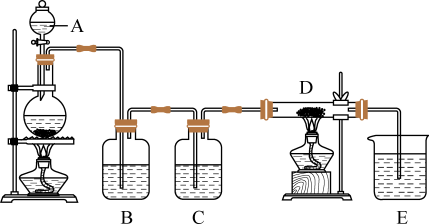
(1)仪器A的名称是_______________ 。
(2)装置B中盛放的液体是______ ,气体通过装置B的目的是_________ 。
装置C中盛放的液体是_________ ,气体通过装置C的目的是____________ 。
(3)D中反应的化学方程式是_____________________________ 。
(4)烧杯E中盛放的液体是______ ,反应的离子方程式是______________ 。

(1)仪器A的名称是
(2)装置B中盛放的液体是
装置C中盛放的液体是
(3)D中反应的化学方程式是
(4)烧杯E中盛放的液体是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】下列是实验室制取乙炔、洗气和性质实验所需的装置及试剂,按要求回答下列问题:

1)请选出制取乙炔气体所需的装置________ (填字母,选错扣分)
2)如果将产生的气体按照发生、洗气、性质实验装置的顺序从左到右连接起来,请写出接口连接的数字顺序:发生装置出口____ 接 ____ 接____ 接_____ 或_____ 。(填数字)
3)写出制取乙炔的化学方程式:____________________________________________ 。
4)装置C的作用 是________________________________________________________ 。
5)如果要进行乙炔的可燃性实验,首先应该__________________________________ 。

1)请选出制取乙炔气体所需的装置
2)如果将产生的气体按照发生、洗气、性质实验装置的顺序从左到右连接起来,请写出接口连接的数字顺序:发生装置出口
3)写出制取乙炔的化学方程式:
4)装置C的作用 是
5)如果要进行乙炔的可燃性实验,首先应该
您最近一年使用:0次





