氨气在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式_______ ;
②NH3的稳定性比PH3_______ (填写“强”或“弱”)。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
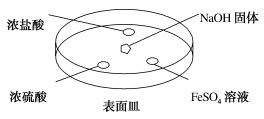
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是_______ (写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH 和
和_______ 。
(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为_______ 。当反应中有0.3mol电子发生转移时,生成亚硝酸的质量为_______ g(小数点后保留两位有效数字)。
(1)①氮气用于工业合成氨,写出氮气的电子式
②NH3的稳定性比PH3
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH
 和
和(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
更新时间:2022-11-11 22:17:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】黑火药是我国四大发明之一,它爆炸时发生多种化学反应,其中主要的化学反应方程式为:
(1)反应物中被称为“中国盐”的化学式是_______ 。生成物中属于非电解质的电子式是_______ 。收集黑火药爆炸后的烟尘与酸性高锰酸钾溶液反应,能使溶液紫红色褪去,烟尘中能使酸性高锰酸钾溶液褪色的物质名称是_______ 。
(2)反应中,还原剂是_______ ,被还原的元素是_______ 。每生成 氧化产物,转移的电子数是
氧化产物,转移的电子数是_______  ,消耗
,消耗 的质量为
的质量为_______ g(保留1位小数)。
(3)有人提出将 通过管道输送到海底,可减缓空气中
通过管道输送到海底,可减缓空气中 浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。结合必要的化学用语,简要分析海水酸性增强的原因
浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。结合必要的化学用语,简要分析海水酸性增强的原因_______ 。

(1)反应物中被称为“中国盐”的化学式是
(2)反应中,还原剂是
 氧化产物,转移的电子数是
氧化产物,转移的电子数是 ,消耗
,消耗 的质量为
的质量为(3)有人提出将
 通过管道输送到海底,可减缓空气中
通过管道输送到海底,可减缓空气中 浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。结合必要的化学用语,简要分析海水酸性增强的原因
浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。结合必要的化学用语,简要分析海水酸性增强的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】NaCl是一种重要的化工原料,可以制备一系列物质如图,回答有关问题:

(1)写出图中体现的两种重要工业生产是_______ 、_______ ;用阳离子交换膜法电解饱和食盐水时,阴极得到_______ 、_______ 。
(2)工业上制取 时,向饱和食盐水中先通入
时,向饱和食盐水中先通入_______ 、后通入_______ ;过滤得到 沉淀后的母液,经吸氨、降温冷析后,加氯化钠细粒可得到一种沉淀,该沉淀的电子式
沉淀后的母液,经吸氨、降温冷析后,加氯化钠细粒可得到一种沉淀,该沉淀的电子式_______ 。
(3)氯离子最外层电子排布式_______ ;氢氧化钠碱性比氢氧化锂碱性强,请用元素周期律知识说明理由_______ 。
(4)图中NaCl是来自粗盐,请简要概括一下制备系列物质的前期要做的主要工作有哪些?_______ 。
(5)氮元素的另一种气态氢化物肼可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为:
(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为:_______ 。


(1)写出图中体现的两种重要工业生产是
(2)工业上制取
 时,向饱和食盐水中先通入
时,向饱和食盐水中先通入 沉淀后的母液,经吸氨、降温冷析后,加氯化钠细粒可得到一种沉淀,该沉淀的电子式
沉淀后的母液,经吸氨、降温冷析后,加氯化钠细粒可得到一种沉淀,该沉淀的电子式(3)氯离子最外层电子排布式
(4)图中NaCl是来自粗盐,请简要概括一下制备系列物质的前期要做的主要工作有哪些?
(5)氮元素的另一种气态氢化物肼可视为
 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为:
(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___ 。
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
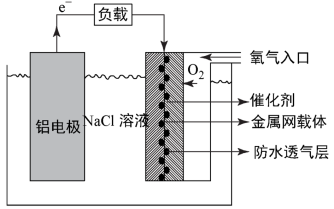
该电池的正极反应方程式为___ ,当铝电极质量减少9克,则另一极通入的氧气的体积在标准状况下为___ 。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为___ 。
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为___ ,相同压强下,AsH3的沸点___ NH3(填“大于”或“小于”)。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

该电池的正极反应方程式为
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列4种物质:①浓H2SO4、②NO2、③NH4Cl、④NaHCO3。其中,可以使蔗糖变黑的是______ (填序号);与水发生反应由红棕变为无色的是______ (填序号);加热分解,遇冷又化合的是______ (填序号);加热分解生产无色无味气体的反应方程式是______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NH3与NO2是常见的氮的化合物,研究它们的综合利用有重要意义
(1)NO2产生的环境问题有_______ (填一种)
(2)热电厂通常用NH3消除燃煤烟气中NO2,写出该反应化学方程式_______
(3)氨气与氯化氢气体混合的现象是_______ ,该反应可用于_______
(4)若将少量氨气与过量氯气混合,则生成一种酸性气体和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式_______ ,A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式_______
(1)NO2产生的环境问题有
(2)热电厂通常用NH3消除燃煤烟气中NO2,写出该反应化学方程式
(3)氨气与氯化氢气体混合的现象是
(4)若将少量氨气与过量氯气混合,则生成一种酸性气体和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硅、硫、氮是重要的非金属元素。回答下列问题:
(1) 属于
属于________ (填“酸性”“碱性”或“两性”)氧化物。 的用途有
的用途有________ (任写一个)。
(2)玻璃也属于典型的硅酸盐材料,其制备原料除了石灰石还有________ ;盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因为________ (用化学方程式表示)。
(3)实验室利用含 的溶液吸收
的溶液吸收 ,从而实现
,从而实现 的回收利用。写出
的回收利用。写出 与
与 在水溶液中发生反应的离子方程式:
在水溶液中发生反应的离子方程式:________ ;每消耗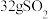 转移电子的物质的量为
转移电子的物质的量为________ mol。
(4)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:________ 。
(1)
 属于
属于 的用途有
的用途有(2)玻璃也属于典型的硅酸盐材料,其制备原料除了石灰石还有
(3)实验室利用含
 的溶液吸收
的溶液吸收 ,从而实现
,从而实现 的回收利用。写出
的回收利用。写出 与
与 在水溶液中发生反应的离子方程式:
在水溶液中发生反应的离子方程式: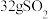 转移电子的物质的量为
转移电子的物质的量为(4)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
您最近一年使用:0次
【推荐1】铁及其化合物与生产、生活关系密切:
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
(2) 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式_______ 。向反应后的溶液加入_______ (填名称),可回收Cu,并得到 溶液。
溶液。
(3)用废铁皮制取( )的部分流程示意图如下:
)的部分流程示意图如下:_______ 。
(4) 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为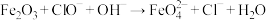 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5) 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。当该反应转移1.2mol电子时,能产生_______ mol 。
。
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
A. | B. | C. | D. |
(2)
 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式 溶液。
溶液。(3)用废铁皮制取(
 )的部分流程示意图如下:
)的部分流程示意图如下: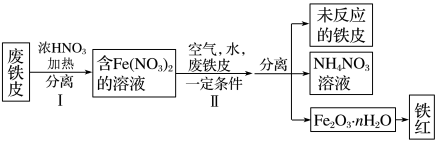
(4)
 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为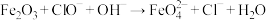 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(5)
 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】油画的白色燃料中曾含二价铅盐,二价铅盐经过长时间空气(含有微量H2S)的侵蚀,生成PbS而变黑。可用一定量的H2O2溶液擦铁修复。完成下列填空:
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式___________ 。
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为___________ 。当PbSO4和CH3COONH4恰好完全反应时,溶液显___________ 性(选填“酸性”、“中性”或“碱性”)。
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为___________ ;该物质在空气中很快变为红褐色,原因是___________ 。
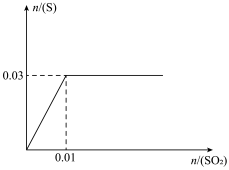
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为___________ 。从开始通SO2至饱和,再继续通一段时间,整个过程中c(H+)的变化情况为___________ 。
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S
 +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
您最近一年使用:0次
【推荐1】铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等,Na2FeO4 可用作净水剂等。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为_______ 。
(2)氯化铁还可以充当双氧水分解的催化剂, 1molH2O2发生分解时转移的电子数是_______ 。
(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得: Fe (NO3) 3+NaOH+Cl2→Na2FeO4+NaNO3+ NaCl +H2O(未配平)。上述反应中氧化产物为_______ 。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为
(2)氯化铁还可以充当双氧水分解的催化剂, 1molH2O2发生分解时转移的电子数是
(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得: Fe (NO3) 3+NaOH+Cl2→Na2FeO4+NaNO3+ NaCl +H2O(未配平)。上述反应中氧化产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)过氧化氢俗名双氧水,有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。配平下列反应方程式:______
______H2O2+______Cr2(SO4)3+______KOH—______K2CrO4+______K2SO4+______H2O
(2)消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑(已配平)。试指出A的化学式______ ,如此反应中有6.72L(标准状况)气体生成,转移电子数目为______
______H2O2+______Cr2(SO4)3+______KOH—______K2CrO4+______K2SO4+______H2O
(2)消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑(已配平)。试指出A的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
 是强氧化性的盐
是强氧化性的盐
 固体保存需要防潮
固体保存需要防潮
 其消毒和净化水的原理相同
其消毒和净化水的原理相同
 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______
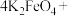 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈 的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附 性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5 mg K2FeO4即可达到卫生标准 ... ... |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是 是强氧化性的盐
是强氧化性的盐 固体保存需要防潮
固体保存需要防潮 其消毒和净化水的原理相同
其消毒和净化水的原理相同 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: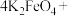 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。
您最近一年使用:0次



