某化学兴趣小组为了探究 的相关性质,设计了如图一的一系列实验。
的相关性质,设计了如图一的一系列实验。

查阅资料:① 与
与 不反应;
不反应;
②氯元素形成物质的二维价类图如下所示:
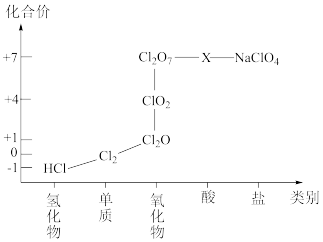
(1)根据二维图中信息,写出氯的最高价含氧酸的化学式_______ 。
(2)将 通入水中,其离子方程式为
通入水中,其离子方程式为_______ 。
(3)实验室可用该反应 制备
制备 ,该反应中盐酸体现
,该反应中盐酸体现_______ (填字母),其中氧化剂与还原剂的微粒个数之比为_______ 。
A.酸性 B.氧化性 C.还原性 D.挥发性
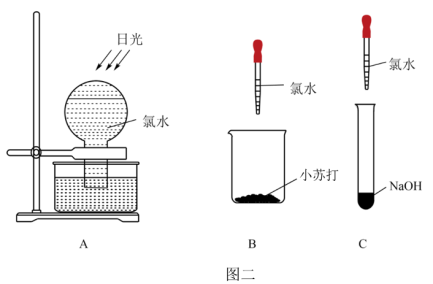
(4)图一中,通入_______ 后,从集气瓶A、B的现象可得出的结论是_______ 。
(5)图二中三组实验,不会产生气体的是_______ ﹔请用一个离子方程式表示图二B装置中发生的反应_______ 。
 的相关性质,设计了如图一的一系列实验。
的相关性质,设计了如图一的一系列实验。
查阅资料:①
 与
与 不反应;
不反应;②氯元素形成物质的二维价类图如下所示:

(1)根据二维图中信息,写出氯的最高价含氧酸的化学式
(2)将
 通入水中,其离子方程式为
通入水中,其离子方程式为(3)实验室可用该反应
 制备
制备 ,该反应中盐酸体现
,该反应中盐酸体现A.酸性 B.氧化性 C.还原性 D.挥发性
(4)图一中,通入
(5)图二中三组实验,不会产生气体的是

更新时间:2022-11-13 00:21:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用硫铁矿烧渣(主要成分为 、FeO、
、FeO、 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为 、
、 、FeO等),制备高效水处理剂聚合硫酸铁铝的流程如下:
、FeO等),制备高效水处理剂聚合硫酸铁铝的流程如下:
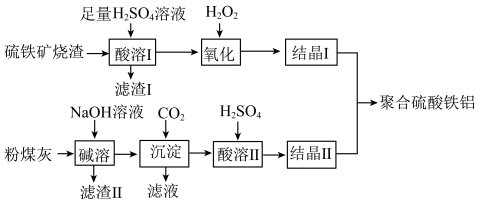
已知: 既不溶于
既不溶于 溶液,也不和
溶液,也不和 溶液反应。
溶液反应。
(1)如何检验“酸溶I”得到的溶液中含有阳离子 的实验方法
的实验方法___________ 。
(2)“氧化”时,若用氯水代替 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(3)流程图中通入过量 反应生成沉淀化学方程式为
反应生成沉淀化学方程式为___________ 。
(4)实验室若以 、
、 、
、 的混合物制备纯净
的混合物制备纯净 溶液,请补充完整的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量该混合物中加入足量的稀硫酸充分反应,过滤,
溶液,请补充完整的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量该混合物中加入足量的稀硫酸充分反应,过滤,___________ ,过滤,得到较纯净的 溶液。
溶液。
(5)向 、FeO的固体混合物中,加入足量
、FeO的固体混合物中,加入足量 溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中
溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中 ,则固体混合物中
,则固体混合物中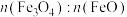 =
=___________ (写出计算过程)。
 、FeO、
、FeO、 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为 、
、 、FeO等),制备高效水处理剂聚合硫酸铁铝的流程如下:
、FeO等),制备高效水处理剂聚合硫酸铁铝的流程如下:
已知:
 既不溶于
既不溶于 溶液,也不和
溶液,也不和 溶液反应。
溶液反应。(1)如何检验“酸溶I”得到的溶液中含有阳离子
 的实验方法
的实验方法(2)“氧化”时,若用氯水代替
 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)流程图中通入过量
 反应生成沉淀化学方程式为
反应生成沉淀化学方程式为(4)实验室若以
 、
、 、
、 的混合物制备纯净
的混合物制备纯净 溶液,请补充完整的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量该混合物中加入足量的稀硫酸充分反应,过滤,
溶液,请补充完整的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量该混合物中加入足量的稀硫酸充分反应,过滤, 溶液。
溶液。(5)向
 、FeO的固体混合物中,加入足量
、FeO的固体混合物中,加入足量 溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中
溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中 ,则固体混合物中
,则固体混合物中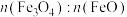 =
=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】碱金属广泛应用于电池、陶瓷、玻璃、润滑剂、制冷液、核工业以及光电等领域,它们的化学性质显示出十分明显的同系行为,根据所学知识回答下列问题:
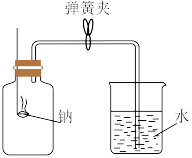
(1)如图所示,先用弹簧夹夹住橡胶管,点燃钠(足量),迅速伸入瓶中并塞上瓶塞,发生反应的化学方程式为___________ ,产物的颜色是___________ ,待反应完全并冷却至原温度后,打开弹簧夹,则观察到的现象是___________ (假设装置的气密性良好)。
(2)按照实验研究和元素周期律推理,元素锂和水反应与钠和水反应比较,反应更剧烈的元素是___________ (填元素符号),锂与水反应的离子方程式是___________ ,锂还是一种重要的储氢材料,其吸氢原理如下: ,则该反应中还原剂是
,则该反应中还原剂是___________ ,每消耗 28g锂相当于可以储存氢气体积为___________ L(H2)密度 0.089g/L,保留到小数点后一位)。
(1)如图所示,先用弹簧夹夹住橡胶管,点燃钠(足量),迅速伸入瓶中并塞上瓶塞,发生反应的化学方程式为

(2)按照实验研究和元素周期律推理,元素锂和水反应与钠和水反应比较,反应更剧烈的元素是
 ,则该反应中还原剂是
,则该反应中还原剂是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
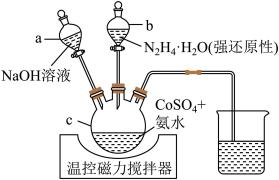
【推荐3】同济大学程传伟教授发现了一种高效的氮杂碳纳米片阵列负载的超薄Co(OH)2纳米片自支撑空气正极材料。实验室可用如图所示装置制得微米级Co(OH)2。
已知:①Co的化合价有+2价和+3价, 、
、 易与
易与 形成络合物,
形成络合物, 的还原性强于
的还原性强于 和
和 。
。
②沉淀的生成速率越快,颗粒越小,呈凝乳状或胶体,不易过滤。请回答下列问题:
(1)仪器 的名称是
的名称是_______ ;使用仪器 的第一步操作名称是
的第一步操作名称是_______ 。
(2) 时,先在不断搅拌下,向
时,先在不断搅拌下,向 中
中 溶液中加入氨水,调节
溶液中加入氨水,调节 至6,加入氨水的作用是
至6,加入氨水的作用是_______ 。
(3)加入氨水后,应先打开滴液漏斗_______ (填“a”或“b”);其理由是_______ 。
(4)将实验所得沉淀过滤、用热水洗涤、干燥,检验产品是否洗净的实验操作是_______ 。
(5)实验室还可以用废旧锂电池正极材料(含 ,以及少量
,以及少量 )为原料制备微米级
)为原料制备微米级 。已知:酸性条件下的氧化性强弱顺序为
。已知:酸性条件下的氧化性强弱顺序为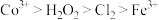 ;
; 可溶于水;下表是部分金属离子生成氢氧化物沉淀的
可溶于水;下表是部分金属离子生成氢氧化物沉淀的 。
。
请补充完整实验方案:取一定量废旧锂电池正极材料,粉碎后与 溶液配成悬浊液;在搅拌下,先加入
溶液配成悬浊液;在搅拌下,先加入_______ 到固体完全溶解;_______ 到溶液的颜色不再加深(或开始产生大量气泡),再向其中加入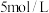 氮水调整溶液
氮水调整溶液 ,使
,使 形成
形成 沉淀,然后过滤,除去难溶性杂质
沉淀,然后过滤,除去难溶性杂质 ;
;_______ ,调节 至9.5,过滤、洗涤,真空㤨干得到微米级
至9.5,过滤、洗涤,真空㤨干得到微米级 。[实验中可选用的试剂:
。[实验中可选用的试剂: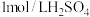 溶液、
溶液、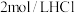 溶液、
溶液、 溶液、30%
溶液、30% 溶液]。
溶液]。
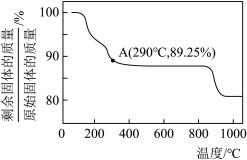
(6) 在空气中加热时,固体残留率随温度的变化如图所示,则在A点时,剩余固体的成分为
在空气中加热时,固体残留率随温度的变化如图所示,则在A点时,剩余固体的成分为_______ (填化学式)。

已知:①Co的化合价有+2价和+3价,
 、
、 易与
易与 形成络合物,
形成络合物, 的还原性强于
的还原性强于 和
和 。
。②沉淀的生成速率越快,颗粒越小,呈凝乳状或胶体,不易过滤。请回答下列问题:
(1)仪器
 的名称是
的名称是 的第一步操作名称是
的第一步操作名称是(2)
 时,先在不断搅拌下,向
时,先在不断搅拌下,向 中
中 溶液中加入氨水,调节
溶液中加入氨水,调节 至6,加入氨水的作用是
至6,加入氨水的作用是(3)加入氨水后,应先打开滴液漏斗
(4)将实验所得沉淀过滤、用热水洗涤、干燥,检验产品是否洗净的实验操作是
(5)实验室还可以用废旧锂电池正极材料(含
 ,以及少量
,以及少量 )为原料制备微米级
)为原料制备微米级 。已知:酸性条件下的氧化性强弱顺序为
。已知:酸性条件下的氧化性强弱顺序为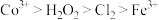 ;
; 可溶于水;下表是部分金属离子生成氢氧化物沉淀的
可溶于水;下表是部分金属离子生成氢氧化物沉淀的 。
。| 金属离子 |  |  |  |
开始沉淀的 | 7.6 | 7.6 | 2.7 |
沉淀完全的 | 9.2 | 9.6 | 3.7 |
 溶液配成悬浊液;在搅拌下,先加入
溶液配成悬浊液;在搅拌下,先加入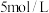 氮水调整溶液
氮水调整溶液 ,使
,使 形成
形成 沉淀,然后过滤,除去难溶性杂质
沉淀,然后过滤,除去难溶性杂质 ;
; 至9.5,过滤、洗涤,真空㤨干得到微米级
至9.5,过滤、洗涤,真空㤨干得到微米级 。[实验中可选用的试剂:
。[实验中可选用的试剂: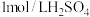 溶液、
溶液、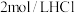 溶液、
溶液、 溶液、30%
溶液、30% 溶液]。
溶液]。(6)
 在空气中加热时,固体残留率随温度的变化如图所示,则在A点时,剩余固体的成分为
在空气中加热时,固体残留率随温度的变化如图所示,则在A点时,剩余固体的成分为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】锰(Mn)最早是由瑞典化学家伯格曼的助手甘恩从软锰矿中分离得到的,锰常用于制造合金锰钢。某化工厂以软锰矿(主要成分是 ,含有
,含有 、
、 、CaO等少量杂质)为主要原料制取金属锰的工艺流程如下所示。
、CaO等少量杂质)为主要原料制取金属锰的工艺流程如下所示。
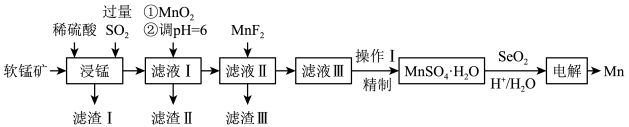
(1)“浸锰”步骤中往往有副产物 生成,温度对“浸锰”反应的影响如图所示。为减少
生成,温度对“浸锰”反应的影响如图所示。为减少 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是_______ ,“滤渣I”的成分有 和
和_______ (填化学式)。该步骤中可以再加入 ,以促进“滤渣I”析出,结合平衡移动原理分析其原因:
,以促进“滤渣I”析出,结合平衡移动原理分析其原因:_______ 。

(2)“滤液I”中需要先加入 ,充分反应后再调pH,写出加入
,充分反应后再调pH,写出加入 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
(3)“滤液II”中加入 的目的是进一步除去溶液中的
的目的是进一步除去溶液中的 ,已知25℃时
,已知25℃时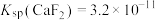 ,则常温下
,则常温下 在纯水中的溶解度为
在纯水中的溶解度为_______ 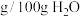 。
。
(4)由“滤液III”可制得 ,已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液III”中获得较高纯度
,已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液III”中获得较高纯度 的“操作I”为控制温度在80~90℃蒸发结晶、
的“操作I”为控制温度在80~90℃蒸发结晶、_______ 、用80~90℃蒸馏水洗涤2~3次、真空干燥。

(5)电解时加入适量的 有利于Mn在电极上析出,
有利于Mn在电极上析出, 与水反应生成的
与水反应生成的 (二元弱酸)在阴极放电生成Se单质(对
(二元弱酸)在阴极放电生成Se单质(对 有特殊的吸附能力,有利于
有特殊的吸附能力,有利于 电还原沉积),该电极反应为
电还原沉积),该电极反应为____ 。
 ,含有
,含有 、
、 、CaO等少量杂质)为主要原料制取金属锰的工艺流程如下所示。
、CaO等少量杂质)为主要原料制取金属锰的工艺流程如下所示。
(1)“浸锰”步骤中往往有副产物
 生成,温度对“浸锰”反应的影响如图所示。为减少
生成,温度对“浸锰”反应的影响如图所示。为减少 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是 和
和 ,以促进“滤渣I”析出,结合平衡移动原理分析其原因:
,以促进“滤渣I”析出,结合平衡移动原理分析其原因:
(2)“滤液I”中需要先加入
 ,充分反应后再调pH,写出加入
,充分反应后再调pH,写出加入 时发生反应的离子方程式:
时发生反应的离子方程式:(3)“滤液II”中加入
 的目的是进一步除去溶液中的
的目的是进一步除去溶液中的 ,已知25℃时
,已知25℃时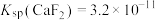 ,则常温下
,则常温下 在纯水中的溶解度为
在纯水中的溶解度为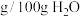 。
。(4)由“滤液III”可制得
 ,已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液III”中获得较高纯度
,已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液III”中获得较高纯度 的“操作I”为控制温度在80~90℃蒸发结晶、
的“操作I”为控制温度在80~90℃蒸发结晶、
(5)电解时加入适量的
 有利于Mn在电极上析出,
有利于Mn在电极上析出, 与水反应生成的
与水反应生成的 (二元弱酸)在阴极放电生成Se单质(对
(二元弱酸)在阴极放电生成Se单质(对 有特殊的吸附能力,有利于
有特殊的吸附能力,有利于 电还原沉积),该电极反应为
电还原沉积),该电极反应为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】从废钼催化剂(主要成分为MoS2,含少量SiO2、CuFeS2、As2O3)中回收钼酸铵晶体的工艺流程如图所示:

注:酸浸后钼元素以MoO 形式存在。
形式存在。
回答下列问题:
(1)高温焙烧时,废钼催化剂中的金属元素转化为金属氧化物,则“焙烧”过程中MoS2发生反应的化学方程式为______ 。
(2)“调pH”中,加入MoO3调节溶液的pH略大于______ 时,可除去目标杂质离子。
已知:溶液中某离子浓度≤10-5mol•L-1时,认为沉淀完全;常温下Ksp[Fe(OH)3]=10-38.5,Ksp[Cu(OH)2]=10-19.6。
(3)若反萃取剂A是氨水,则反萃取过程中MoO 发生的离子方程式为
发生的离子方程式为______ 。
(4)已知“除砷”过程中,pH对As去除率的影响如图所示。当pH>10后,随着pH的增大,去除率呈下降趋势的原因可能是_______ 。

(5)钼酸铵溶液可用于测定磷肥含磷量,步骤如下:准确称量磷肥2.84g,用硫酸和高氯酸在高温下使之分解,磷转化为磷酸。过滤、洗涤、弃去残渣。以硫酸—硝酸为介质,加入过量钼酸铵溶液生成钼磷酸铵沉淀(NH4)3H4PMo12O42•H2O,将过滤、洗涤后的沉淀溶于50.00mL6.00mol•L-1NaOH溶液后,定容至250mL。取25mL溶液,以酚酞为指示剂,用0.40mol•L-1盐酸溶液滴定其中过量的NaOH,消耗盐酸23.00mL。计算磷肥中磷的百分含量_______ (以P2O5计)(写出计算过程)。
已知:(NH4)3H4PMo12O42•H2O+26NaOH=12Na2MoO4+Na2HPO4+3NH3↑+17H2O。

注:酸浸后钼元素以MoO
 形式存在。
形式存在。回答下列问题:
(1)高温焙烧时,废钼催化剂中的金属元素转化为金属氧化物,则“焙烧”过程中MoS2发生反应的化学方程式为
(2)“调pH”中,加入MoO3调节溶液的pH略大于
已知:溶液中某离子浓度≤10-5mol•L-1时,认为沉淀完全;常温下Ksp[Fe(OH)3]=10-38.5,Ksp[Cu(OH)2]=10-19.6。
(3)若反萃取剂A是氨水,则反萃取过程中MoO
 发生的离子方程式为
发生的离子方程式为(4)已知“除砷”过程中,pH对As去除率的影响如图所示。当pH>10后,随着pH的增大,去除率呈下降趋势的原因可能是

(5)钼酸铵溶液可用于测定磷肥含磷量,步骤如下:准确称量磷肥2.84g,用硫酸和高氯酸在高温下使之分解,磷转化为磷酸。过滤、洗涤、弃去残渣。以硫酸—硝酸为介质,加入过量钼酸铵溶液生成钼磷酸铵沉淀(NH4)3H4PMo12O42•H2O,将过滤、洗涤后的沉淀溶于50.00mL6.00mol•L-1NaOH溶液后,定容至250mL。取25mL溶液,以酚酞为指示剂,用0.40mol•L-1盐酸溶液滴定其中过量的NaOH,消耗盐酸23.00mL。计算磷肥中磷的百分含量
已知:(NH4)3H4PMo12O42•H2O+26NaOH=12Na2MoO4+Na2HPO4+3NH3↑+17H2O。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。回答下列问题:
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。回答下列问题:

(1)煅烧前需粉碎黄铁矿并且煅烧时通入足量空气,这些做法的原因是_______ ,写出“煅烧”过程的化学方程式_______ 。
(2)此流程中 炉渣用
炉渣用 高温还原法制得还原铁粉,在实际中还可采用
高温还原法制得还原铁粉,在实际中还可采用_______ 反应制得铁水,用于焊接钢轨,此反应是_______ (填“放热反应”或“吸热反应”)。
(3)流程中用 制硫酸的过程在实际硫酸工业中在接触室和吸收塔中进行。接触室中的反应为
制硫酸的过程在实际硫酸工业中在接触室和吸收塔中进行。接触室中的反应为 。
。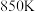 时,在一恒容密闭反应器中充入一定量的
时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得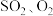 和
和 的浓度分别为
的浓度分别为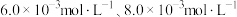 和
和 。
。
①该温度下反应的平衡常数为_______ (保留两位有效数字)。
②平衡时 的转化率为
的转化率为_______ 。
(4)因为 具有
具有_______ 性,导致 产品中不可避免地存在
产品中不可避免地存在 。检验其中含有
。检验其中含有 的操作是
的操作是_______ 。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。回答下列问题:
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。回答下列问题:
(1)煅烧前需粉碎黄铁矿并且煅烧时通入足量空气,这些做法的原因是
(2)此流程中
 炉渣用
炉渣用 高温还原法制得还原铁粉,在实际中还可采用
高温还原法制得还原铁粉,在实际中还可采用(3)流程中用
 制硫酸的过程在实际硫酸工业中在接触室和吸收塔中进行。接触室中的反应为
制硫酸的过程在实际硫酸工业中在接触室和吸收塔中进行。接触室中的反应为 。
。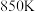 时,在一恒容密闭反应器中充入一定量的
时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得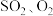 和
和 的浓度分别为
的浓度分别为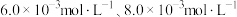 和
和 。
。①该温度下反应的平衡常数为
②平衡时
 的转化率为
的转化率为(4)因为
 具有
具有 产品中不可避免地存在
产品中不可避免地存在 。检验其中含有
。检验其中含有 的操作是
的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用如图装置制取氯气,并用氯气进行实验。回答下列问题:
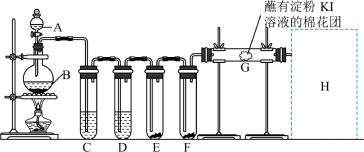
(1)A中盛有浓盐酸,B中盛有 ,该反应的化学方程式为:
,该反应的化学方程式为:___________ ,如果生成1mol的氯气,则被还原的HCl为___________ mol。
(2)D中放入浓 的目的是
的目的是___________ 。
(3)E中为干燥的有色布条,F中为湿润的有色布条,可观察到的现象是___________ ,解释E、F装置中现象不同的原因:___________ 。
(4)G处的现象是___________ 。
(5)用离子方程式写出H处尾气吸收装置中的反应原理___________ 。

(1)A中盛有浓盐酸,B中盛有
 ,该反应的化学方程式为:
,该反应的化学方程式为:(2)D中放入浓
 的目的是
的目的是(3)E中为干燥的有色布条,F中为湿润的有色布条,可观察到的现象是
(4)G处的现象是
(5)用离子方程式写出H处尾气吸收装置中的反应原理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
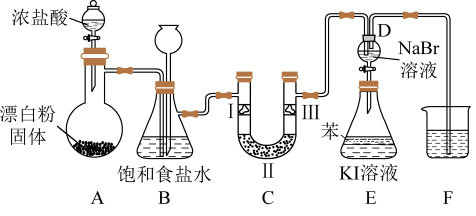
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是___________ ,请写出该反应相应的化学方程式___________ 。
(2)装置B中饱和食盐水的作用是___________ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是___________ ,该现象___________ (填“能”或“不能")说明溴单质的氧化性强于碘,原因是___________ 。
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为___________ 。

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是
(2)装置B中饱和食盐水的作用是
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有
 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下。
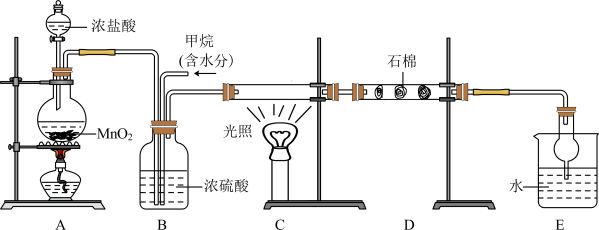
根据要求回答下列问题:
(1)A装置中装浓盐酸的实验仪器_______ (填名称),A装置烧瓶中发生反应的化学方程式为_______ ,足量MnO2与一定量的浓盐酸通过该反应生成标准状况下11.2L气体,理论上反应中消耗的溶质n(HCl)=_______ mol。
(2)B装置有三种功能:①控制气流速度,②均匀混合气体,③_______ 。
(3)C装置中生成一氯甲烷的化学方程式为_______ ,若在C装置中生成了1mol一氯甲烷,则反应的Cl2物质的量_______ 1mol(填“>”、“=”或“<”)。
(4)D装置的石棉中均匀混有KI粉末,其作用是_______ 。
A.吸收有机化合物 B.吸收氯气 C.吸收氯化氢
(5)E装置中干燥管的作用是_______ 。
A.吸收氯气 B.吸收氯化氢 C.防止倒吸
(6)该装置还有缺陷,原因是没有进行尾气处理,其尾气中主要的含氯有机化合物为_______。

根据要求回答下列问题:
(1)A装置中装浓盐酸的实验仪器
(2)B装置有三种功能:①控制气流速度,②均匀混合气体,③
(3)C装置中生成一氯甲烷的化学方程式为
(4)D装置的石棉中均匀混有KI粉末,其作用是
A.吸收有机化合物 B.吸收氯气 C.吸收氯化氢
(5)E装置中干燥管的作用是
A.吸收氯气 B.吸收氯化氢 C.防止倒吸
(6)该装置还有缺陷,原因是没有进行尾气处理,其尾气中主要的含氯有机化合物为_______。
| A.CH3Cl | B.CH2Cl2 | C.CHCl3 | D.CCl4 |
您最近一年使用:0次



