自舍勒发现氯气可以作为消毒剂以来,人们陆续发现和使用了形形色色的消毒剂。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移_________ 。反应中盐酸表现出的性质有_________ 。
(2)根据世界环保联盟的要求,二氧化氯( )消毒剂将逐渐取代
)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:_________ 。
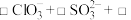 _________
_________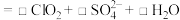
(3)高铁酸钾 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。
①湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式_________ 。
②如下图所示,用 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: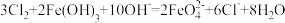 。
。

反应后取出三口瓶中的溶液于试管中,加入稀 后产生黄绿色气体
后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 。制备高铁酸钾的实验中,氧化性:
。制备高铁酸钾的实验中,氧化性:
_________  (填写>,<或=)。试管中发生反应再次产生
(填写>,<或=)。试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
_________  (填写>,<或=)。试说明影响
(填写>,<或=)。试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素_________ 。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用
 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移(2)根据世界环保联盟的要求,二氧化氯(
 )消毒剂将逐渐取代
)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为: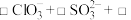 _________
_________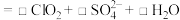
(3)高铁酸钾
 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。①湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式②如下图所示,用
 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: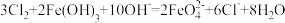 。
。
反应后取出三口瓶中的溶液于试管中,加入稀
 后产生黄绿色气体
后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 。制备高铁酸钾的实验中,氧化性:
。制备高铁酸钾的实验中,氧化性:
 (填写>,<或=)。试管中发生反应再次产生
(填写>,<或=)。试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
 (填写>,<或=)。试说明影响
(填写>,<或=)。试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素
更新时间:2022-11-13 20:54:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知NaHSO4晶体易溶于水,它溶于水时,电离出三种不同的离子,因此NaHSO4溶液显强酸性,类似盐酸。
(1)下列说法中正确的是________ (填序号)
A.NaHSO4属于酸 B.NaHSO4属于正盐
C.NaHSO4属于酸式盐 D.NaHSO4溶液能与Zn反应生成氢气
(2)向一定量的Ba(OH)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的化学方程式为:_________________________________________ , 沉淀完全后,继续滴加NaHSO4溶液,此时发生反应的化学方程式为:____________________ 。
(3)NaHCO3与NaHSO4类似,NaHCO3分别与过量的Ca(OH)2溶液、少量的Ca(OH)2溶液反应时,除共同的两种产物CaCO3、H2O外,还有产物的化学式依次为____________ 、___________ 。
(1)下列说法中正确的是
A.NaHSO4属于酸 B.NaHSO4属于正盐
C.NaHSO4属于酸式盐 D.NaHSO4溶液能与Zn反应生成氢气
(2)向一定量的Ba(OH)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的化学方程式为:
(3)NaHCO3与NaHSO4类似,NaHCO3分别与过量的Ca(OH)2溶液、少量的Ca(OH)2溶液反应时,除共同的两种产物CaCO3、H2O外,还有产物的化学式依次为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列反应的离子方程式不正确 的是_______ 。
A.(2021年1月·浙江选考真题)石灰石与醋酸反应:CO +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2O
B.(2022·湖南省等级考)用醋酸和淀粉-KI溶液检验加碘盐中的IO :IO
:IO +5I-+6H+=3I2+3H2O
+5I-+6H+=3I2+3H2O
C.(2022·广东省等级考)钠的过氧化物转化为碱:2O +2H2O=4Na++4OH-+O2↑
+2H2O=4Na++4OH-+O2↑
D.(2022·广东省等级考)钠的盐转化为另一种盐:Na2SiO3+2H+=H2SiO3↓+2Na+
E.(2021·浙江高考)碳酸镁与稀盐酸反应:CO +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
F.(2021·全国乙卷)氯化铜溶液中通入硫化氢:S2-+Cu2+=CuS↓
G.(2021·浙江7月学考真题)氯酸钾的电离方程式:KClO3=K++Cl-+3O2-
H.(2020·天津等级考)CaCO3与稀硝酸反应:CO +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
I.(2020·江苏高考)Cl2通入水中制氯水:Cl2+H2O 2H++Cl-+ClO-
2H++Cl-+ClO-
J.(2020·浙江7月选考)CuSO4溶液中滴加稀氨水:Cu2++2OH-=Cu(OH)2↓
K.(2018·浙江6月学考真题)MnO2与浓盐酸反应的离子方程式:MnO2+4HCl Mn2++Cl2↑+2Cl-+2H2O
Mn2++Cl2↑+2Cl-+2H2O
L.(2019·江苏高考)向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
M.(2019·北京高考)H2C2O4有还原性:2MnO +5C2O
+5C2O +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
A.(2021年1月·浙江选考真题)石灰石与醋酸反应:CO
 +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2OB.(2022·湖南省等级考)用醋酸和淀粉-KI溶液检验加碘盐中的IO
 :IO
:IO +5I-+6H+=3I2+3H2O
+5I-+6H+=3I2+3H2OC.(2022·广东省等级考)钠的过氧化物转化为碱:2O
 +2H2O=4Na++4OH-+O2↑
+2H2O=4Na++4OH-+O2↑D.(2022·广东省等级考)钠的盐转化为另一种盐:Na2SiO3+2H+=H2SiO3↓+2Na+
E.(2021·浙江高考)碳酸镁与稀盐酸反应:CO
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2OF.(2021·全国乙卷)氯化铜溶液中通入硫化氢:S2-+Cu2+=CuS↓
G.(2021·浙江7月学考真题)氯酸钾的电离方程式:KClO3=K++Cl-+3O2-
H.(2020·天津等级考)CaCO3与稀硝酸反应:CO
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2OI.(2020·江苏高考)Cl2通入水中制氯水:Cl2+H2O
 2H++Cl-+ClO-
2H++Cl-+ClO-J.(2020·浙江7月选考)CuSO4溶液中滴加稀氨水:Cu2++2OH-=Cu(OH)2↓
K.(2018·浙江6月学考真题)MnO2与浓盐酸反应的离子方程式:MnO2+4HCl
 Mn2++Cl2↑+2Cl-+2H2O
Mn2++Cl2↑+2Cl-+2H2OL.(2019·江苏高考)向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
M.(2019·北京高考)H2C2O4有还原性:2MnO
 +5C2O
+5C2O +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】判断下列离子方程式是否正确(填“对”或“错”),并将错误的离子方程式修改正确。
(1)铁粉溶于稀硫酸:2Fe2++6H+=2Fe3++H2 ↑_________ ,_____________________ 。
(2)用饱和氯化铁溶液制备氢氧化铁胶体:Fe3++3OH-=Fe(OH)3↓_________ ,_________________ 。
(3)氧化钙溶于盐酸反应:CaO+2H+=Ca2++H2O_________ ,____________________ 。
(4)BaCO3与稀硫酸反应:Ba2++ =BaSO4↓
=BaSO4↓_________ ,___________________ 。
(5)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-= Mg(OH)2↓_________ ,__________________ 。
(6)硝酸钙溶液和碳酸钾溶液混合:Ca2++ =CaCO3↓
=CaCO3↓_________ ,_________________ 。
(1)铁粉溶于稀硫酸:2Fe2++6H+=2Fe3++H2 ↑
(2)用饱和氯化铁溶液制备氢氧化铁胶体:Fe3++3OH-=Fe(OH)3↓
(3)氧化钙溶于盐酸反应:CaO+2H+=Ca2++H2O
(4)BaCO3与稀硫酸反应:Ba2++
 =BaSO4↓
=BaSO4↓(5)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-= Mg(OH)2↓
(6)硝酸钙溶液和碳酸钾溶液混合:Ca2++
 =CaCO3↓
=CaCO3↓
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知 是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究
是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究 的性质,进行了如下实验:
的性质,进行了如下实验:
Ⅰ.配制480mL
 溶液
溶液
(1)用托盘天平称量,需要称取
_________ g。
(2)定容时,若仰视容量瓶刻度线会使配制的 溶液浓度
溶液浓度_________ (填“偏大”、“偏小”或“不变”)。
(3)若在加蒸馏水时,不小心加过了刻度线,此时应该进行的操作是_________ 。
Ⅱ.探究 的性质
的性质
(4)取20mL上述 溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为
溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为_________ 。
(5)再取20mL上述 溶液,逐滴加入新制氯水直至过量,再加入
溶液,逐滴加入新制氯水直至过量,再加入 溶液振荡静置,现象为
溶液振荡静置,现象为_________ 。
(6)有上述实验现象可得到的结论:还原性:
_________  (填“>”“<”或者“=”)
(填“>”“<”或者“=”)
(7)若向10mL上述 溶液通入44.8mL
溶液通入44.8mL (标准状况),反应的离子方程式为
(标准状况),反应的离子方程式为_________ 。
 是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究
是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究 的性质,进行了如下实验:
的性质,进行了如下实验:Ⅰ.配制480mL

 溶液
溶液(1)用托盘天平称量,需要称取

(2)定容时,若仰视容量瓶刻度线会使配制的
 溶液浓度
溶液浓度(3)若在加蒸馏水时,不小心加过了刻度线,此时应该进行的操作是
Ⅱ.探究
 的性质
的性质(4)取20mL上述
 溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为
溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为(5)再取20mL上述
 溶液,逐滴加入新制氯水直至过量,再加入
溶液,逐滴加入新制氯水直至过量,再加入 溶液振荡静置,现象为
溶液振荡静置,现象为(6)有上述实验现象可得到的结论:还原性:

 (填“>”“<”或者“=”)
(填“>”“<”或者“=”)(7)若向10mL上述
 溶液通入44.8mL
溶液通入44.8mL (标准状况),反应的离子方程式为
(标准状况),反应的离子方程式为
您最近一年使用:0次
【推荐2】现有下列反应:
①
②
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目_______________ 。
(2)Cl2、H2SO4和KMnO4的氧化性由强到弱的顺序为_______________ 。
(3)反应②中氯化氢表现出的性质是_______________ 。
a.还原性 b.酸性 c.氧化性
(4)已知实验室制备NO的反应为: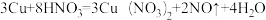 。
。
①反应中氧化剂是______________ ;被氧化的元素是______________ ;氧化产物是______________ 。
②若有2gNO生成,有______________ gHNO3被还原。
(5)请配平下列方程式,并用双线桥法标出电子转移的方向和数目_________ 。

①

②

针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目
(2)Cl2、H2SO4和KMnO4的氧化性由强到弱的顺序为
(3)反应②中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
(4)已知实验室制备NO的反应为:
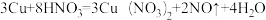 。
。①反应中氧化剂是
②若有2gNO生成,有
(5)请配平下列方程式,并用双线桥法标出电子转移的方向和数目

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)已知碘元素最终变为无色HIO3。上述整个过程中的还原剂是_______________________ 。写出CCl4层变成紫色的离子反应方程式________________________________________ 。
(2)若把KI换成KBr,则CCl4层变为_________ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是______________________________________ 。
(3)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。试配平该反应的化学方程式,并用短线标出电子转移方向及总数__ NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+_H2O,已知含氧酸盐的氧化作用随溶液酸性的加强而增强,在制备实验时,定时取样,并用酸化的氯化钡来检测SO42-离子生成的量,发现开始阶段反应速度呈递增的趋势,试简述这变化趋势发生的原因:________________ 。
(1)已知碘元素最终变为无色HIO3。上述整个过程中的还原剂是
(2)若把KI换成KBr,则CCl4层变为
(3)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。试配平该反应的化学方程式,并用短线标出电子转移方向及总数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。
请回答下列问题。
(1)下列属于氮的固定的是___________ 。
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为___________ 。
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途___________ 。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是___________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3>CH3COOH>H2PO ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为___________ 。
请回答下列问题。
(1)下列属于氮的固定的是
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3>CH3COOH>H2PO
 ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
您最近一年使用:0次
【推荐2】已知:还原性HSO3->I-,氧化性IO3-> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目_______ 。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为_______ (填化学式);
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______ ;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______ mol。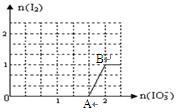
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式

您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】碳氧化物的转化有重大用途,回答关于CO和CO2的问题。
(1)已知:① C (s) + H2O(g) CO (g) +H2(g) △H1
CO (g) +H2(g) △H1
② 2CO(g) + O2(g) = 2CO2(g) △H2
③H2O (g)= H2(g) +1/2 O2(g) △H3
则C (s) + O2(g) =CO2(g)的△H =(用△H1、△H2、△H3表示)。
(2)对于化学平衡①,在不同温度下,CO的浓度与反应时间的关系如图所示,

由图可得出如下规律:随着温度升高,①;②。
(3)某温度下,将6.0 mol H2O(g)和足量碳充入3 L的恒容密闭容器中,发生如下反应: C (s) + H2O(g) CO (g) +H2(g),达到平衡时测得lgK=-1.0(K为平衡常数),求平衡时H2O(g)的转化率?(写出计算过程)
CO (g) +H2(g),达到平衡时测得lgK=-1.0(K为平衡常数),求平衡时H2O(g)的转化率?(写出计算过程)
(4)在神舟九号飞船中,宇航员呼出的CO2也可以采用Na2O2吸收,写出相关的化学方程式并标明电子转移的方向和数目:。
(1)已知:① C (s) + H2O(g)
 CO (g) +H2(g) △H1
CO (g) +H2(g) △H1② 2CO(g) + O2(g) = 2CO2(g) △H2
③H2O (g)= H2(g) +1/2 O2(g) △H3
则C (s) + O2(g) =CO2(g)的△H =(用△H1、△H2、△H3表示)。
(2)对于化学平衡①,在不同温度下,CO的浓度与反应时间的关系如图所示,

由图可得出如下规律:随着温度升高,①;②。
(3)某温度下,将6.0 mol H2O(g)和足量碳充入3 L的恒容密闭容器中,发生如下反应: C (s) + H2O(g)
 CO (g) +H2(g),达到平衡时测得lgK=-1.0(K为平衡常数),求平衡时H2O(g)的转化率?(写出计算过程)
CO (g) +H2(g),达到平衡时测得lgK=-1.0(K为平衡常数),求平衡时H2O(g)的转化率?(写出计算过程)(4)在神舟九号飞船中,宇航员呼出的CO2也可以采用Na2O2吸收,写出相关的化学方程式并标明电子转移的方向和数目:。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。
(1)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:____ 。
(2)实验室利用如图装置制备KClO和KClO3。
已知:6OH-+3Cl2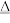 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O

①盛放浓盐酸的仪器名称是____ ,A中发生反应的离子方程式为____ 。
②B的作用是____ ;C中试管内盛放的试剂为____ 。
③用8.7gMnO2与足量浓盐酸充分反应,生成Cl2在标况下的体积为____ 。
(3)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为____ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是____ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。取含次氯酸钠14.9g·L-1的84消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为___ mol·L-1。
(1)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:
(2)实验室利用如图装置制备KClO和KClO3。
已知:6OH-+3Cl2
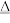 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
①盛放浓盐酸的仪器名称是
②B的作用是
③用8.7gMnO2与足量浓盐酸充分反应,生成Cl2在标况下的体积为
(3)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。取含次氯酸钠14.9g·L-1的84消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为
您最近一年使用:0次
【推荐2】按要求完成下列填空:
(1)硫酸铁在水溶液中的电离方程式:___ 。
(2)实验室制取氯气的化学方程式:___ 。
(3)单线桥法标出下列反应电子转移的方向和数目并填空:___ 。
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
在该反应中,氧化剂是___ (填化学式)。
(1)硫酸铁在水溶液中的电离方程式:
(2)实验室制取氯气的化学方程式:
(3)单线桥法标出下列反应电子转移的方向和数目并填空:
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
在该反应中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】盐酸、硫酸、硝酸是工业生产中常用的三种强酸。回答下列问题:
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有_______ (酸性、氧化性、还原性)的物质发生反应;若用0.6 mol  与100 mL
与100 mL 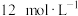 的浓盐酸加热反应,生成
的浓盐酸加热反应,生成 的物质的量
的物质的量_______ (填标号)。
A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为_______ 。上述两种方法中,制取硫酸铜的最佳方法是_______ (填“①”或“②”),理由是_______ 。
(3)将12.8 g铜与足量的浓硝酸反应,产生NO和 气体的体积为5.60 L(STP),则参加反应的硝酸的物质的量为
气体的体积为5.60 L(STP),则参加反应的硝酸的物质的量为_______ 。
(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。

若M为酸。则M的化学式可能为_______ 。
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有
 与100 mL
与100 mL 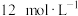 的浓盐酸加热反应,生成
的浓盐酸加热反应,生成 的物质的量
的物质的量A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为
(3)将12.8 g铜与足量的浓硝酸反应,产生NO和
 气体的体积为5.60 L(STP),则参加反应的硝酸的物质的量为
气体的体积为5.60 L(STP),则参加反应的硝酸的物质的量为(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。

若M为酸。则M的化学式可能为
您最近一年使用:0次



