二氯化二硫(S2Cl2)是一种常用于橡胶硫化、有机物氯化的试剂。查阅资料:①将干燥的氯气在110~140 ℃间与硫反应,即可得S2Cl2粗品;②有关物质的部分性质如表所示:
设计如图所示实验装置在实验室合成S2Cl2:
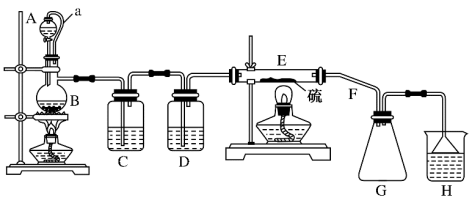
回答以下问题:
(1)A仪器的名称____ ,B仪器的名称______ ,a的作用是____ 。
(2)C装置的作用是____ 。
(3)乙同学发现,该装置中除了E处的温度不能过高外,还有一处重大缺陷需改进,否则会导致S2Cl2的产率大大降低,原因是____ (用化学方程式表示);请简要提出改进方案:______________________ 。
(4)H中的溶液选择下列试剂中的最佳试剂是____ (填序号)。
①碳酸钠溶液 ②NaOH溶液 ③饱和NaCl溶液
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 一种橙黄色的液体,遇水易水解,有淡黄色固体S出现,同时产生能使品红溶液褪色的气体SO2;300℃以上完全分解;S2Cl2 + Cl2 2SCl2 。 2SCl2 。 |
设计如图所示实验装置在实验室合成S2Cl2:

回答以下问题:
(1)A仪器的名称
(2)C装置的作用是
(3)乙同学发现,该装置中除了E处的温度不能过高外,还有一处重大缺陷需改进,否则会导致S2Cl2的产率大大降低,原因是
(4)H中的溶液选择下列试剂中的最佳试剂是
①碳酸钠溶液 ②NaOH溶液 ③饱和NaCl溶液
更新时间:2022-11-29 21:51:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氨气与适量氯气混合反应可生成NH4Cl(岩脑砂的主要成分)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。
A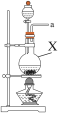 B
B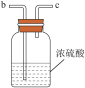
C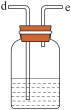 D
D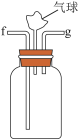
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为________________ 。
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→________________ → ________________ → ________________ → ________________ 。
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从__________ 通入,反应的化学方程式为 ___________ ;可能观察到的现象是________________ 。
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
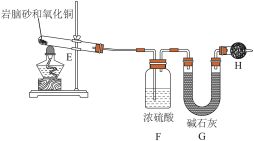
①为顺利完成有关物理量的测定,请完善下列表格。
②如果不用H装置,测出NH4Cl的含量将_____ (填“偏高”“偏低”或“无影响”)。
A
 B
B
C
 D
D
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO
 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
①为顺利完成有关物理量的测定,请完善下列表格。
| 测量时间点 | 反应前 | 反应后 |
| 测量内容 | 当观察到 时停止加热,冷却,称量H装置的总质量 |
②如果不用H装置,测出NH4Cl的含量将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
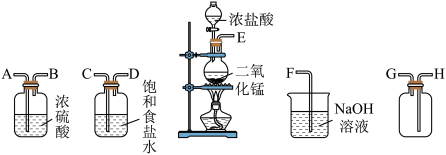
(1)连接上述仪器的正确顺序(填各接口处的字母):_______ 。
(2)装置中,饱和食盐水的作用是_______ ; NaOH溶液的作用是_______ 。
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到_______ 。
(4)写出制氯气的化学方程式:_______ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(4)写出制氯气的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
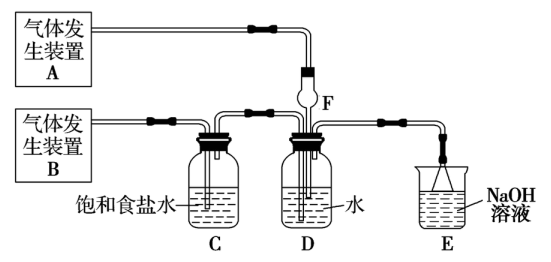
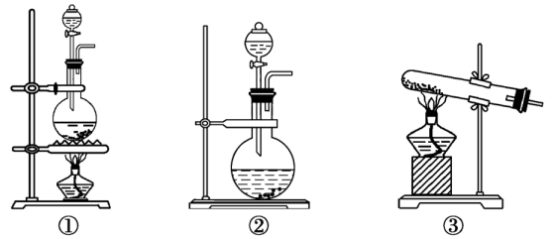
(1)该化学兴趣小组的同学现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2,在此实验中,F仪器的作用是___________ ;气体发生装置B应选择以上三种装置中的___________ (填序号)。
(2)装置D中主要反应的离子方程式为___________ 。
(3)为验证通入装置D中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液②氯化亚铁溶液③硫氰化钾溶液④品红溶液
若Cl2过量,取适量D中溶液滴加至盛有___________ (填一个序号)的试管内,再加入___________ (填一个序号)。产生的现象是___________ 。
若SO2过量,取适量D中溶液滴加至盛有___________ (填一个序号)的试管内,产生的现象是___________ 。


(1)该化学兴趣小组的同学现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2,在此实验中,F仪器的作用是
(2)装置D中主要反应的离子方程式为
(3)为验证通入装置D中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液②氯化亚铁溶液③硫氰化钾溶液④品红溶液
若Cl2过量,取适量D中溶液滴加至盛有
若SO2过量,取适量D中溶液滴加至盛有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】钌(Ru)为重要的稀有元素,广泛应用于电子、航空航天、化工等领域。一种以含钌废料(主要成分为Ru,含有SiO2、Bi2O3等杂质)为原料制RuCl3的工艺流程如图:
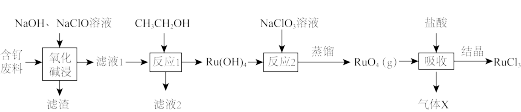
已知:滤液1中Ru元素和Bi元素存在形式为RuO 、BiO
、BiO 。
。
回答下列问题:
(1)“氧化碱浸”时,为提高钌的浸出率可采取的措施有____ (任写一条),Ru发生反应的离子方程式为_____ 。
(2)滤液2的主要成分有NaCl、CH3CHO和____ ,反应1的离子方程式是___ 。
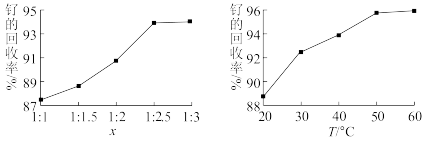
(3)金属钌与乙醇的质量比x和反应温度T对钌的回收率的影响如图所示,则回收钌较为适宜的条件是____ 。
(4)气体X经处理可以循环利用,“吸收”过程发生反应的化学方程式为____ 。
(5)可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2=2Ru+6HCl。产品纯度进行测定时,所得数据见表:
则产品的纯度为____ 。
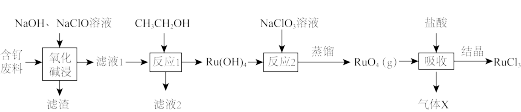
已知:滤液1中Ru元素和Bi元素存在形式为RuO
 、BiO
、BiO 。
。回答下列问题:
(1)“氧化碱浸”时,为提高钌的浸出率可采取的措施有
(2)滤液2的主要成分有NaCl、CH3CHO和
(3)金属钌与乙醇的质量比x和反应温度T对钌的回收率的影响如图所示,则回收钌较为适宜的条件是

(4)气体X经处理可以循环利用,“吸收”过程发生反应的化学方程式为
(5)可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2=2Ru+6HCl。产品纯度进行测定时,所得数据见表:
| 实验序号 | 产品质量/g | 固体Ru质量/g |
| ① | 5.000 | 2.0210 |
| ② | 5.000 | 2.0190 |
| ③ | 5.000 | 2.0200 |
| ④ | 5.000 | 1.6200 |
则产品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是
可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是 ,杂质有
,杂质有 、
、 、
、 )制取
)制取 的流程如图
的流程如图
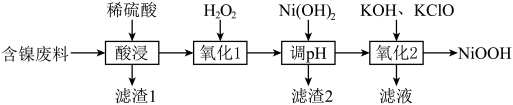
已知:i. 的性质较稳定;
的性质较稳定;
ii.有关金属离子沉淀的相关 见下表
见下表
回答下列问题:
(1) 与
与 同族,则
同族,则 在周期表中的位置
在周期表中的位置_______ ,“滤渣2”的主要成分_________ 。
(2)实际生产中发现 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是___________ 。
(3)“调 ”时
”时 的范围是
的范围是___________ 。
(4)“氧化2”中反应的离子方程式为___________ 。
(5)配合物 ,四羰基合镍的配位原子
,四羰基合镍的配位原子___________ 。
 可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是
可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是 ,杂质有
,杂质有 、
、 、
、 )制取
)制取 的流程如图
的流程如图
已知:i.
 的性质较稳定;
的性质较稳定;ii.有关金属离子沉淀的相关
 见下表
见下表| 沉淀物 |  |  |  |  |
开始沉淀时 | 3.0 | 1.5 | 5.9 | 7.1 |
完全沉淀时 | 4.7 | 3.2 | 9.0 | 9.2 |
(1)
 与
与 同族,则
同族,则 在周期表中的位置
在周期表中的位置(2)实际生产中发现
 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是(3)“调
 ”时
”时 的范围是
的范围是(4)“氧化2”中反应的离子方程式为
(5)配合物
 ,四羰基合镍的配位原子
,四羰基合镍的配位原子
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】三氧化二镍(Ni2O3)是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分为镍、铝、氧化铁、碳等)提取Ni2O3,工业流程如图:
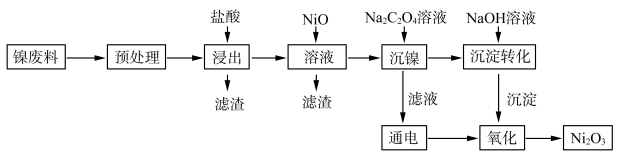
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O。
③Ksp[Al(OH)3]=1.9×10-23,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Ni(OH)2]=1.6×10-14,Ksp(NiC2O4)=1.0×10-9。
回答下列问题:
(1)“预处理”操作可以选择用___ (填标号)来除去废旧镍电池表面的矿物油污。
A.纯碱溶液浸泡 B.NaOH溶液浸泡 C.酒精清洗
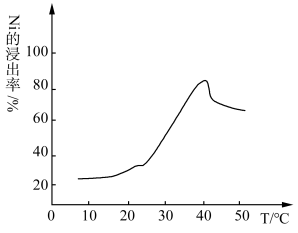
(2)酸浸时①镍的浸出率与温度的关系如图所示,温度高于40℃时镍的浸出率开始下降,主要原因可能是___ (从两个角度分析)
②常温下,盐酸的浓度为2.5mol/L,液固比与镍的浸出率的关系如表所示,
实际生产采取的液固比为___ ,主要原因是___ 。
(3)室温下,“浸出”所得溶液中Fe3+的浓度为0.2mol·L-1,当溶液的pH从1调到2时,沉铁率为___ 。
(4)证明“沉镍”中,Ni2+已经沉淀完全的实验步骤及现象为:___ 。
(5)写出加入Na2C2O4溶液的反应的化学方程式:___ 。
(6)电解过程产生的氯气在弱碱条件下生成了ClO-,再把二价镍氧化为三价镍,写出“氧化”反应的离子方程式:___ 。

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O。
③Ksp[Al(OH)3]=1.9×10-23,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Ni(OH)2]=1.6×10-14,Ksp(NiC2O4)=1.0×10-9。
回答下列问题:
(1)“预处理”操作可以选择用
A.纯碱溶液浸泡 B.NaOH溶液浸泡 C.酒精清洗
(2)酸浸时①镍的浸出率与温度的关系如图所示,温度高于40℃时镍的浸出率开始下降,主要原因可能是

②常温下,盐酸的浓度为2.5mol/L,液固比与镍的浸出率的关系如表所示,
| 液固比 | 7:1 | 6:1 | 5:1 |
| 镍的浸出率/% | 95.63 | 95.32 | 89.68 |
实际生产采取的液固比为
(3)室温下,“浸出”所得溶液中Fe3+的浓度为0.2mol·L-1,当溶液的pH从1调到2时,沉铁率为
(4)证明“沉镍”中,Ni2+已经沉淀完全的实验步骤及现象为:
(5)写出加入Na2C2O4溶液的反应的化学方程式:
(6)电解过程产生的氯气在弱碱条件下生成了ClO-,再把二价镍氧化为三价镍,写出“氧化”反应的离子方程式:
您最近一年使用:0次



