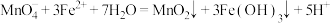焦亚锑酸钠是一种化工产品,难溶于水。以粗锑酸钠(主要成分是Na3SbO4,含少量硫)为原料制备焦亚锑酸钠的流程如下:

下列说法不正确的是

下列说法不正确的是
| A.“酸溶”时温度不宜过高 |
| B.“中和”反应之一为SbCl5+6NaOH=NaSb(OH)6↓+5NaCl |
| C.“一系列操作”包括蒸发浓缩、冷却结晶等 |
| D.一般采用蒸发结晶操作从“中和液”中提取氯化钠 |
更新时间:2022-08-19 20:37:56
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列表示对应化学反应的离子方程式正确的是
A.铜跟浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
B.向硫酸铝溶液中加入过量氨水:Al3++3NH3·H2O =Al(OH)3↓+3NH |
C.向酸性KMnO4溶液中滴加H2O2:2MnO +7H2O2+6H+=2Mn2++6O2↑+10H2O +7H2O2+6H+=2Mn2++6O2↑+10H2O |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3·H2O +OH-=NH3·H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某容器中发生一个化学反应,反应过程中存在 、
、 、
、 、NO、
、NO、 、
、 中物质,已知
中物质,已知 是反应物之一、下列有关判断不正确的是
是反应物之一、下列有关判断不正确的是
 、
、 、
、 、NO、
、NO、 、
、 中物质,已知
中物质,已知 是反应物之一、下列有关判断不正确的是
是反应物之一、下列有关判断不正确的是| A.该容器中发生了氧化还原反应 |
B.该反应中 、 、 也是反应物, 也是反应物, 、NO、 、NO、 是生成物 是生成物 |
| C.该反应中只有砷元素被氧化、只有氮元素被还原 |
| D.氧化剂和还原剂的个数之比为28:3 |
您最近一年使用:0次
【推荐3】白硼钙石的主要成分是Ca4B10O19·7H2O(含有少量Fe2O3、FeO、CaCO3和SiO2等杂质),利用白硼钙石制取强还原剂NaBH4的工艺流程如下:
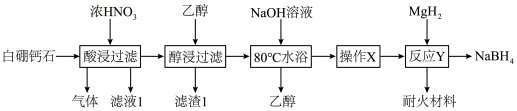
| A.“滤渣1”的主要成分是SiO2 |
| B.“气体”的主要成分是NO2 |
| C.“操作X”涉及到蒸发浓缩、降温结晶 |
D.“反应Y”的化学方程式是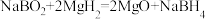 |
您最近一年使用:0次
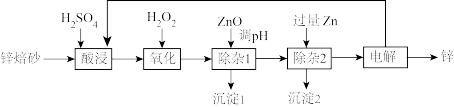
【推荐1】锌是一种常用金属,工业上利用锌培砂(主要含ZnO、 ,还含有少量CaO、FeO、CuO、NiO等)湿法制取金属锌的流程如图所示。已知:Fe的活泼性强于Ni。下列说法错误的是
,还含有少量CaO、FeO、CuO、NiO等)湿法制取金属锌的流程如图所示。已知:Fe的活泼性强于Ni。下列说法错误的是
 ,还含有少量CaO、FeO、CuO、NiO等)湿法制取金属锌的流程如图所示。已知:Fe的活泼性强于Ni。下列说法错误的是
,还含有少量CaO、FeO、CuO、NiO等)湿法制取金属锌的流程如图所示。已知:Fe的活泼性强于Ni。下列说法错误的是
A.加入 是为了将 是为了将 氧化为 氧化为 | B.ZnO可以用 代替 代替 |
| C.“沉淀2”中只含有两种金属 | D.可循环利用的物质为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用磁铁矿(主要成分 、含
、含 和
和 等杂质)制取
等杂质)制取 的工艺流程如下:
的工艺流程如下:
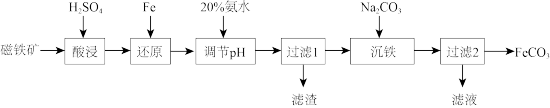
下列说法正确的是
 、含
、含 和
和 等杂质)制取
等杂质)制取 的工艺流程如下:
的工艺流程如下:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 4.0 | 6.5 |
| 完全沉淀的pH | 3.3 | 5.2 | 9.7 |
| A.“酸浸”过程中加入过量硫酸能抑制金属离子水解和提高铁元素的浸出率 |
| B.“调节pH时应控制溶液的pH大于3.3 |
C.“沉铁”时应将过滤1的滤液滴加到 溶液中,并不断搅拌 溶液中,并不断搅拌 |
D.“过滤2”所得滤液中的溶质为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
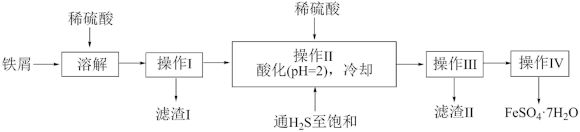
已知:室温饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6,FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.根据以上流程图,下列说法错误的是

已知:室温饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6,FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.根据以上流程图,下列说法错误的是
| A.“溶解”中用到25%的稀硫酸,可用98%浓硫酸配制,需玻璃棒、烧杯、量筒、胶头滴管等仪器 |
| B.操作Ⅱ中用硫酸酸化至pH=2的主要目的是抑制Fe2+的水解 |
| C.操作Ⅱ中,通入H2S至饱和的目的是使Sn2+转化为SnS沉淀并防止Fe2+被氧化 |
| D.操作IV中所得的晶体最后用乙醇洗去晶体表面附着的水分 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】分离下列物质的方法正确的是
| A.氯化钠溶液中的泥沙----蒸馏 |
| B.提取溴水中的溴单质----萃取分液 |
| C.除去硝酸钾中的少量氯化钠-----蒸发结晶 |
| D.分离汽油和水------过滤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以粗铜为原料制取并收集NO2。从反应后的溶液中回收Cu(NO3)2•6H2O。实验装置如下:
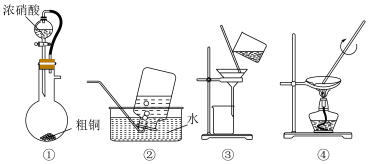
下列设计不能达到实验目的的是

下列设计不能达到实验目的的是
| A.用装置①制取NO2 |
| B.用装置④蒸发浓缩装置③所得滤液,然后冷却结晶、固液分离 |
| C.用装置②收集NO2 |
| D.用装置③除去反应残液中的不溶物 |
您最近一年使用:0次

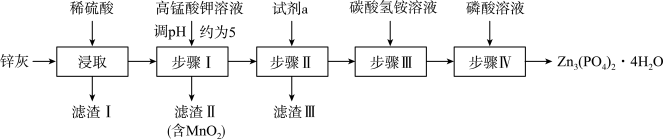
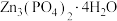 ]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含Zn、ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备
]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含Zn、ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备