聚合硫酸铁铝是一种新型高效水处理剂。利用硫铁矿烧渣(主要成分为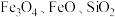 等)为铁源,粉煤灰(主要成分为
等)为铁源,粉煤灰(主要成分为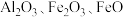 等)为铝源制备聚合硫酸铁铝的工艺流程如下:
等)为铝源制备聚合硫酸铁铝的工艺流程如下:
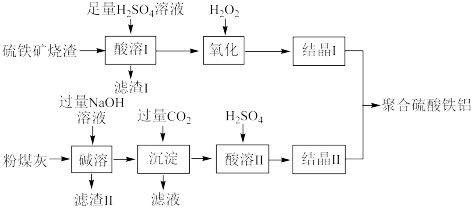
(1)“酸溶Ⅰ”中, 发生反应的离子方程式为
发生反应的离子方程式为_________ 。
(2)“氧化”时应控制温度不超过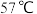 ,原因是
,原因是_________ ,“氧化”过程中发生反应的离子方程式为_________ 。
(3)滤渣Ⅱ的主要成分为_________ (填化学式)。
(4)通入 后生成沉淀的化学方程式为
后生成沉淀的化学方程式为_________ 。
(5)已知聚合硫酸铁铝的化学式为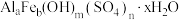 ,则该化学式中a、b、m、n间的关系为
,则该化学式中a、b、m、n间的关系为_________ 。
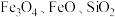 等)为铁源,粉煤灰(主要成分为
等)为铁源,粉煤灰(主要成分为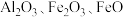 等)为铝源制备聚合硫酸铁铝的工艺流程如下:
等)为铝源制备聚合硫酸铁铝的工艺流程如下:
(1)“酸溶Ⅰ”中,
 发生反应的离子方程式为
发生反应的离子方程式为(2)“氧化”时应控制温度不超过
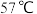 ,原因是
,原因是(3)滤渣Ⅱ的主要成分为
(4)通入
 后生成沉淀的化学方程式为
后生成沉淀的化学方程式为(5)已知聚合硫酸铁铝的化学式为
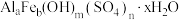 ,则该化学式中a、b、m、n间的关系为
,则该化学式中a、b、m、n间的关系为
更新时间:2022-12-06 13:36:07
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
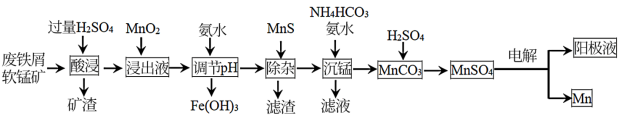
【推荐1】采用废铁屑还原软锰矿 软锰矿主要成分是
软锰矿主要成分是 ,还含有
,还含有 、MgO、
、MgO、 和
和 杂质
杂质 来制备Mn的工艺流程如图所示:
来制备Mn的工艺流程如图所示:
已知: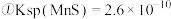 ,
, ;
; 生成氢氧化物的pH见下表
生成氢氧化物的pH见下表
回答下列问题:
(1)“酸浸”前将原料粉碎的目的是_______________________________________ 。
(2)写出氨水中溶质的电离平衡常数表达式
_________________________ 。
(3)“调节pH”操作中pH控制范围为_____________ 。
(4)“除杂”加入MnS,请写出此过程发生的离子方程式:__________________ 当该反应完全后,滤液中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是_____________ 。
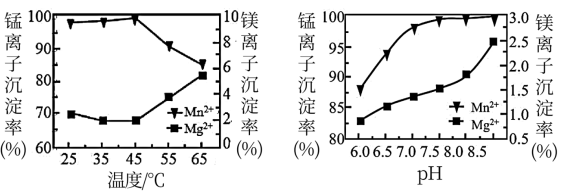
(5)“沉锰”过程中温度和pH对 和
和 沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是
沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是_______ 。
(6)MnSO4溶液电解制备Mn的过程中,电解反应的离子方程式是_____________________ 。
 软锰矿主要成分是
软锰矿主要成分是 ,还含有
,还含有 、MgO、
、MgO、 和
和 杂质
杂质 来制备Mn的工艺流程如图所示:
来制备Mn的工艺流程如图所示:
已知:
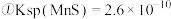 ,
, ;
; 生成氢氧化物的pH见下表
生成氢氧化物的pH见下表| 离子 |  |  |  |  |  |
| 开始沉淀的pH |  |  | 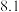 |  |  |
| 完全沉淀的pH | 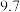 | 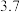 |  |  |  |
回答下列问题:
(1)“酸浸”前将原料粉碎的目的是
(2)写出氨水中溶质的电离平衡常数表达式

(3)“调节pH”操作中pH控制范围为
(4)“除杂”加入MnS,请写出此过程发生的离子方程式:
 与
与 的物质的量浓度之比是
的物质的量浓度之比是(5)“沉锰”过程中温度和pH对
 和
和 沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是
沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是
(6)MnSO4溶液电解制备Mn的过程中,电解反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】FeOOH可用于脱硫工序,脱除效果较好。工业上利用冶金废渣(主要成分为FeSO4,还含有少量的Fe2(SO4)3、MgSO4及TiOSO4)为主要原料生产FeOOH的一种工艺流程如下:

(1)FeOOH中Fe的化合价为_______ 。
(2)冶金废渣“溶解”时一般要粉碎,目的是_______ ,TiOSO4与水反应生成难溶于水的H2TiO3和一种常见的酸,该反应的化学方程式为_______ 。
(3)“除杂”时,加入NaF溶液的作用为沉淀Mg2+,则滤液Y中的主要含有的溶质为_______ 。
(4)“氧化”时,试剂X最佳选择为_______ (填序号)。
a.KMnO4 b. HNO3 c. Cl2 d.空气
(5)工业上冶炼Fe的方法是_______ ,铝与四氧化三铁的反应方程式:_______ 。

(1)FeOOH中Fe的化合价为
(2)冶金废渣“溶解”时一般要粉碎,目的是
(3)“除杂”时,加入NaF溶液的作用为沉淀Mg2+,则滤液Y中的主要含有的溶质为
(4)“氧化”时,试剂X最佳选择为
a.KMnO4 b. HNO3 c. Cl2 d.空气
(5)工业上冶炼Fe的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某废旧金属材料中主要含Fe、Al、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物。
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物。

(已知:绿矾为 ,相对分子质量为:278)
,相对分子质量为:278)
回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去_______ 。
(2)“碱浸”时发生反应的化学方程式为_______ 。
(3)“操作Ⅰ”的名称是_______ ,该操作需用到的玻璃仪器除烧杯、玻璃棒外,还需要_______ 。
(4)试剂a是_______ (填名称),“操作Ⅲ”主要为蒸发浓缩,_______ 。
(5)绿矾( )易被空气中的氧气氧化,快速取少量样品溶于试管中,滴加
)易被空气中的氧气氧化,快速取少量样品溶于试管中,滴加_______ 溶液(填化学式),可以确定产物是否被氧化。用下列方法测定绿矾纯度:称取6.0g样品用稀硫酸溶解,滴加0.1mol/L的酸性 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为40.00mL,则
溶液的体积为40.00mL,则 的纯度为
的纯度为_______ 。(结果保留1位小数,已知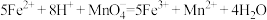 )
)
 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物。
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物。
(已知:绿矾为
 ,相对分子质量为:278)
,相对分子质量为:278)回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去
(2)“碱浸”时发生反应的化学方程式为
(3)“操作Ⅰ”的名称是
(4)试剂a是
(5)绿矾(
 )易被空气中的氧气氧化,快速取少量样品溶于试管中,滴加
)易被空气中的氧气氧化,快速取少量样品溶于试管中,滴加 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为40.00mL,则
溶液的体积为40.00mL,则 的纯度为
的纯度为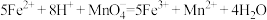 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钯(Pd)是有机合成中常用的催化剂。一种由废钯催化剂(主要成分为Pd,还有PdO、Fe有机物残留以及其他杂质)制取金属Pd的工艺流程如图:

回答下列问题:
(1)废钯催化剂经烘干、粉碎后,再在700℃的高温下焙烧,不断通入足量空气的目的除了使有机物充分燃烧而除去,还可以___ 。
(2)查资料可知,PdO不溶于王水,加入甲酸还原PdO,其目的是___ ,
(3)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为___ ;酸溶时温度不能过高,原因是___ 。
(4)加入适量的稀氨水溶液调节pH至3~4除杂,废渣的主要成分是___ 。
(5)焙烧2的目的是___ ;
(6)有水参加情况下,可以将CO通入氯化钯(PdCl2)得到黑色金属Pd粉末,化学方程式为___ 。

回答下列问题:
(1)废钯催化剂经烘干、粉碎后,再在700℃的高温下焙烧,不断通入足量空气的目的除了使有机物充分燃烧而除去,还可以
(2)查资料可知,PdO不溶于王水,加入甲酸还原PdO,其目的是
(3)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为
(4)加入适量的稀氨水溶液调节pH至3~4除杂,废渣的主要成分是
(5)焙烧2的目的是
(6)有水参加情况下,可以将CO通入氯化钯(PdCl2)得到黑色金属Pd粉末,化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】高纯硅被誉为“信息革命的催化剂”。某小组模拟工业上用SiHCl3与H2在1357K的条件下制备高纯硅,实验装置如图所示(部分加热及夹持装置略去)。
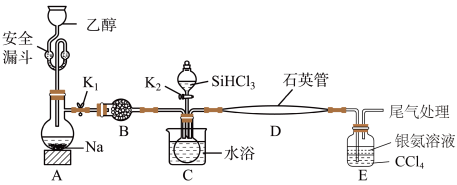
实验操作步骤有:①打开K1,向安全漏斗中加入足量乙醇,装置A中反应一段时间;②加热装置C,打开K2,滴加VmLSiHCl3;③加热装置D至1357K;④关闭K1;⑤关闭K2。
已知:①SiHCl3的沸点为33.0℃,密度为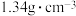 ;易溶于有机溶剂;能与水剧烈反应;在空气中易被氧化;
;易溶于有机溶剂;能与水剧烈反应;在空气中易被氧化;
② ;
;
③银氨溶液中存在: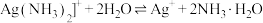 。
。
回答下列问题:
(1)相比长颈漏斗,安全漏斗使用时的优点是___________ 。
(2)装置B中试剂宜选择___________ (填标号)。
a.碱石灰 b.无水氯化钙 c.五氧化二磷 d.硅胶
(3)加热装置C之前,先进行装置A的反应,这样操作的目的是___________ 。
(4)装置D中发生反应的化学方程式为___________ 。
(5)E中CCl4的作用是防倒吸和___________ ,用化学平衡原理解释银氨溶液中有白色沉淀生成:___________ 。
(6)本实验制得高纯硅ag,则高纯硅的产率为___________ (只列计算式)。

实验操作步骤有:①打开K1,向安全漏斗中加入足量乙醇,装置A中反应一段时间;②加热装置C,打开K2,滴加VmLSiHCl3;③加热装置D至1357K;④关闭K1;⑤关闭K2。
已知:①SiHCl3的沸点为33.0℃,密度为
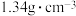 ;易溶于有机溶剂;能与水剧烈反应;在空气中易被氧化;
;易溶于有机溶剂;能与水剧烈反应;在空气中易被氧化;②
 ;
;③银氨溶液中存在:
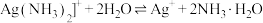 。
。回答下列问题:
(1)相比长颈漏斗,安全漏斗使用时的优点是
(2)装置B中试剂宜选择
a.碱石灰 b.无水氯化钙 c.五氧化二磷 d.硅胶
(3)加热装置C之前,先进行装置A的反应,这样操作的目的是
(4)装置D中发生反应的化学方程式为
(5)E中CCl4的作用是防倒吸和
(6)本实验制得高纯硅ag,则高纯硅的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】1,2-二氯乙烷(CH2ClCH2Cl)是重要的有机化工原料,不溶于水,常用作有机溶剂,沸点83.6°C,实验室可用“乙烯液相直接氯化法”来制备:
C2H5OH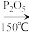 CH2=CH2↑+H2O
CH2=CH2↑+H2O
Cl2(g)+CH2=CH2(g)→CH2ClCH2Cl(l) ∆H<0
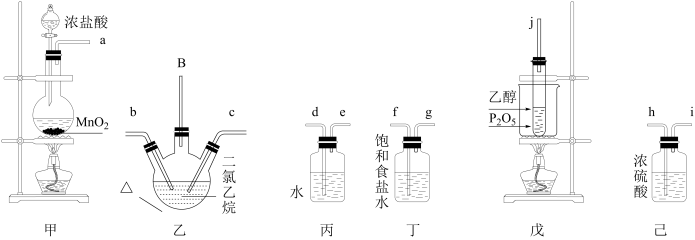
(1)关于乙装置及其中的反应填空:
①仪器A的名称:_______ 。
②乙装置控制反应温度在50℃~70℃(加热装置已省略),控制在此温度范围的原因:_______ 。
③乙装置在通入气体前,加入适量的二氯乙烷,其作用是_______ 。
④若反应气(Cl2和CH2=CH2)中混有水,则可能发生的化学反应方程式为_______ 。
(2)根据实验原理,该装置的连接顺序为:a→_______ →bc←_______ ←j(按接口顺序连接,装置可重复使用)。
(3)产品提纯:由于有副反应存在,该方法获得的1,2-二氯乙烷(CH2ClCH2Cl)还含有少量的多氯化物和HCl。下列提纯操作的顺序是:用水洗涤,静置,分去水层;_______ (填序号);干燥 ;精馏。
① 蒸馏脱去大部分水,获得共沸物
② 加碱闪蒸除去酸性物质及部分高沸物
③ 用水洗涤余碱至中性
④ 将馏分静置、分液
(4)产品纯度的测定:量取5.0mL产品,密度为0.44g·mL-1,加足量稀NaOH水溶液,加热充分反应得到250mL水解液。取25.00mL水解液先用稀硝酸中和至酸性,然后加入过量的50.00mL0.1000mol/LAgNO3溶液,充分反应后再加入硝基苯,用力摇动。用0.1000mol/LNH4SCN标准液滴定过量的AgNO3溶液,重复实验三次,平均消耗标准液10.00mL。已知:Ag++SCN-=AgSCN↓(白色沉淀),Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12。
①滴定时,应选用的指示剂为_______ (填标号)。
A.FeSO4 B.FeCl3 C. Fe(NO3)3 D. 甲基橙
②产品中1,2-二氯乙烷的纯度为_______ %。
③实验中加入硝基苯的作用是_______ 。
C2H5OH
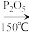 CH2=CH2↑+H2O
CH2=CH2↑+H2OCl2(g)+CH2=CH2(g)→CH2ClCH2Cl(l) ∆H<0

(1)关于乙装置及其中的反应填空:
①仪器A的名称:
②乙装置控制反应温度在50℃~70℃(加热装置已省略),控制在此温度范围的原因:
③乙装置在通入气体前,加入适量的二氯乙烷,其作用是
④若反应气(Cl2和CH2=CH2)中混有水,则可能发生的化学反应方程式为
(2)根据实验原理,该装置的连接顺序为:a→
(3)产品提纯:由于有副反应存在,该方法获得的1,2-二氯乙烷(CH2ClCH2Cl)还含有少量的多氯化物和HCl。下列提纯操作的顺序是:用水洗涤,静置,分去水层;
① 蒸馏脱去大部分水,获得共沸物
② 加碱闪蒸除去酸性物质及部分高沸物
③ 用水洗涤余碱至中性
④ 将馏分静置、分液
(4)产品纯度的测定:量取5.0mL产品,密度为0.44g·mL-1,加足量稀NaOH水溶液,加热充分反应得到250mL水解液。取25.00mL水解液先用稀硝酸中和至酸性,然后加入过量的50.00mL0.1000mol/LAgNO3溶液,充分反应后再加入硝基苯,用力摇动。用0.1000mol/LNH4SCN标准液滴定过量的AgNO3溶液,重复实验三次,平均消耗标准液10.00mL。已知:Ag++SCN-=AgSCN↓(白色沉淀),Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12。
①滴定时,应选用的指示剂为
A.FeSO4 B.FeCl3 C. Fe(NO3)3 D. 甲基橙
②产品中1,2-二氯乙烷的纯度为
③实验中加入硝基苯的作用是
您最近一年使用:0次



