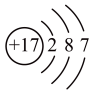
表格是周期表中的一部分,根据A~I在周期表中的位置,用元素符号 (化学式 )或化学符号 回答下列问题:
(1)A~I中,化学性质最不活泼的元素基态原子的电子排布式是_______ ,写出E基态原子价层电子的轨道表示式_______ 。
(2)其单质能用于制漂白粉的元素是_______ 。
(3)在D、E、J中,原子半径最大的元素是_______ 。
(4)A分别与D、E、G形成的化合物中,最稳定的化合物的电子式是_______ 。
(5)表格中C的单质与NaOH溶液发生反应的化学方程式为_______ 。
| 主族 周期 | I | II | III | IV | V | VI | VII | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)其单质能用于制漂白粉的元素是
(3)在D、E、J中,原子半径最大的元素是
(4)A分别与D、E、G形成的化合物中,最稳定的化合物的电子式是
(5)表格中C的单质与NaOH溶液发生反应的化学方程式为
更新时间:2022-12-17 21:31:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:

(1)元素⑩在周期表中的位置是______ ,⑦的原子结构示意图为______ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为____ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是_____ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是____ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式____________________________________ 。
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
①只存在共价键的是______ ,只存在离子键的是_____ ,既存在离子键又存在共价键的是__ 。
②写出下列物质的电子式:CO2_________ ,NaOH___________ 。

(1)元素⑩在周期表中的位置是
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
①只存在共价键的是
②写出下列物质的电子式:CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】A元素原子M电子层上有6个电子,B元素与A元素的原子核外电子层数相同,B元素的原子最外电子层上只有1个电子。
(1)B元素的原子结构示意图为________ 。
(2)A、B两元素形成的化合物的名称是________ ,化学式是_______ ,该化合物在无色火焰上灼烧时,火焰呈_______ 色。
(1)B元素的原子结构示意图为
(2)A、B两元素形成的化合物的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的是 ,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;
(3)按要求写出下列两种物质的电子式:①的氢化物 ;⑨的最高价氧化物的对应的水化物 ;
(4)在以上元素的单质中,化学性质最不活泼的是 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是 ,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;
(3)按要求写出下列两种物质的电子式:①的氢化物 ;⑨的最高价氧化物的对应的水化物 ;
(4)在以上元素的单质中,化学性质最不活泼的是 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】1869年俄国化学家门捷列夫制出第一张元素周期表。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
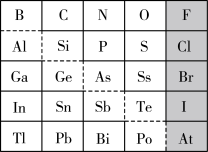
(1)Sn的最高正价为_______ ,I的最高价氧化物对应水化物的化学式为_______ ,Bi的最高价氧化物为_______ 。
(2)元素Ga在元素周期表中的位置为:_______ 。
(3)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是_______ (填化学式)。
②N3-、O2-、Al3+、S2-,四种离子半径大小顺序:_______ (用离子符号排序)。
③H3AsO4、H2SeO4、H2SO4的酸性强弱顺序:_______ 。
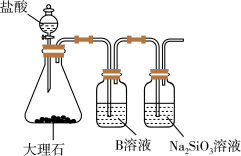
(4)查阅资料可知:硅酸(H2SiO3)是一种难溶于水的弱酸。为比较元素C和Si的非金属性强弱,用图所示装置进行实验。溶液B应该选用_______ 溶液,作用是_______ ,其中能说明C和Si非金属性强弱的化学方程式是:_______ 。

(1)Sn的最高正价为
(2)元素Ga在元素周期表中的位置为:
(3)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是
②N3-、O2-、Al3+、S2-,四种离子半径大小顺序:
③H3AsO4、H2SeO4、H2SO4的酸性强弱顺序:
(4)查阅资料可知:硅酸(H2SiO3)是一种难溶于水的弱酸。为比较元素C和Si的非金属性强弱,用图所示装置进行实验。溶液B应该选用

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据表格中提供的甲、乙、丙、丁四种元素的相关信息完成下列问题:
(1)填写表格中各序号所对应的空白:①_________________ ②__________________
③_________________ ④_________________ 。
(2)甲、乙、丙、丁四种元素中,原子半径最大的是_______ (填元素符号),丁元素的最高正价为____ 价(填化合价)。
(3)最高价氧化物对应水化物的碱性:甲_______________ 乙(填“>”或“<”),简单气态氢化物的稳定性:丙_______________ 丁(填“>”或“<”)。
(4)元素乙的最高价氧化物对应水化物,既能与元素甲的最高价氧化物对应水化物反应,又能中和过多的胃酸。
请分别写出上述反应的离子方程式:_____________ ;______________ 。
(5)丁单质通入冷的消石灰中可制得漂白粉,写出该反应的化学方程式:_____________________ 。
元素 | 甲 | 乙 | 丙 | 丁 |
原子序数 | 11 | ③ | ||
元素符号 | ② | S | ||
原子结构示意图 | ① |
| ||
元素周期表中的位置 | 第三周期 ⅢA族 | ④ |
③
(2)甲、乙、丙、丁四种元素中,原子半径最大的是
(3)最高价氧化物对应水化物的碱性:甲
(4)元素乙的最高价氧化物对应水化物,既能与元素甲的最高价氧化物对应水化物反应,又能中和过多的胃酸。
请分别写出上述反应的离子方程式:
(5)丁单质通入冷的消石灰中可制得漂白粉,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
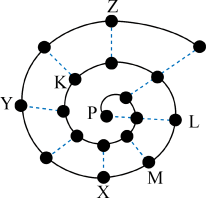
(1)X元素符号为__________________ 。
(2)M与Z两种元素形成的化合物含有的化学键为________________ 。
(3)下列说法正确的是__________________ 。
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键

(1)X元素符号为
(2)M与Z两种元素形成的化合物含有的化学键为
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上常用SO2除去原料气中少量CO生成物为S和氧和CO2。
(1)写出该反应的化学方程式为__________________________________________
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为________________ 。
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为______________ ;三种元素非金属性由强到弱的顺序为__________________ ;反应所涉及的化合物中仅有一种是非极性分子,其电子式为_______________ 。
(1)写出该反应的化学方程式为
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】针对下面10种元素,完成以下各小题
(1)地壳中含量最多的元素是___________ (填名称)。
(2)化学性质最不活泼的元素是___________ (填元素符号)。
(3)Al的原子结构示意图为___________________ 。
(4)C与N相比,原子半径较小的是___________ 。
(5)最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________ 。
(7)S和Cl相比,元素非金属性较强的是___________ 。
(1)地壳中含量最多的元素是
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Al | Si | S | Cl | Ne |
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,其中字母代表相应的元素。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为_______ 。
(2)c、d、e、f元素原子的第一电离能( )由小到大的顺序为
)由小到大的顺序为_______ (用相应元素符号表示)。
(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛( )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为_____ 。1mol苯甲醛( )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为______ mol。
(4)一种由表中元素形成的离子与单质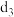 互为等电子体,其离子符号为
互为等电子体,其离子符号为_______ 。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为
(2)c、d、e、f元素原子的第一电离能(
 )由小到大的顺序为
)由小到大的顺序为(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛(
 )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为 )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为(4)一种由表中元素形成的离子与单质
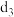 互为等电子体,其离子符号为
互为等电子体,其离子符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知各元素原子的电子排布如下: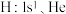
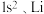
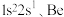

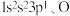
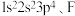
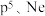
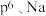
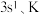
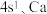
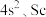
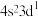 ……(s最多填2个电子,p最多填6个电子,d最多填10个电子)
……(s最多填2个电子,p最多填6个电子,d最多填10个电子)
(1)根据规律写出铁(26)和铜(29)的电子排布式_______ 、_______ ;
(2)如果其规则下一个是f,则f可填充_____ 个电子,写出通式_______ ;
(3)通过规律推断 和
和 哪个更稳定
哪个更稳定_______ 。
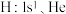
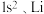
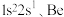

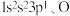
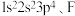
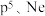
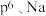
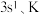
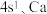
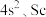
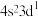 ……(s最多填2个电子,p最多填6个电子,d最多填10个电子)
……(s最多填2个电子,p最多填6个电子,d最多填10个电子)(1)根据规律写出铁(26)和铜(29)的电子排布式
(2)如果其规则下一个是f,则f可填充
(3)通过规律推断
 和
和 哪个更稳定
哪个更稳定
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)基态Se原子的核外电子排布式为[Ar]_______ 。
(2)基态S原子的价电子中,两种自旋状态的电子数之比为_______ 。
(3)基态O原子的电子排布式_______ ,其中未成对电子有_______ 个。
(4)基态F原子的价电子排布图(轨道表示式)为_______ 。
(5)研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
(6)比较 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:_______ 。
(1)基态Se原子的核外电子排布式为[Ar]
(2)基态S原子的价电子中,两种自旋状态的电子数之比为
(3)基态O原子的电子排布式
(4)基态F原子的价电子排布图(轨道表示式)为
(5)研究发现,给小鼠喂食适量硒酸钠(
 )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)比较
 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:
您最近一年使用:0次