工业上常用SO2除去原料气中少量CO生成物为S和氧和CO2。
(1)写出该反应的化学方程式为__________________________________________
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为________________ 。
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为______________ ;三种元素非金属性由强到弱的顺序为__________________ ;反应所涉及的化合物中仅有一种是非极性分子,其电子式为_______________ 。
(1)写出该反应的化学方程式为
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为
更新时间:2020-03-25 13:50:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,__ 元素的化合价升高,则该元素的原子__ (填“得到”或“失去”)电子;而__ 元素的化合价降低,则该元素的原子被__ (填“氧化”或“还原”)。
(2)上述反应中,若有10个铝原子参与反应,则转移的电子总数为__ ,用“双线桥法”表示反应中电子转移的方向和数目:___
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(1)上述反应中,
(2)上述反应中,若有10个铝原子参与反应,则转移的电子总数为
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
您最近一年使用:0次
【推荐2】二氧化氯消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氮常温下为黄绿色或桔黄色气体,以下是二氧化氮的几种工业制备方法。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目_______ 。
(2) 还原法:
还原法:
①配平该反应的离子方程式:_______ 。





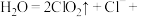




②还原产物为_______ 。
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为_______ ,0.1mol NaClO3参加反应,做酸性介质的HCl的物质的量为_______ mol。
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为_______ ,0.2mol HCl参加反应,转移的电子数为_______ 。
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:_______ 。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目
(2)
 还原法:
还原法:①配平该反应的离子方程式:





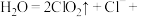




②还原产物为
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:
您最近一年使用:0次
【推荐3】NaCN是重要的基本化工原料,常用于基本化学合成、冶金等,回答下列问题:
(1)NaCN中C的化合价为_____ ;写出NaCN的电子式:_________________________________ ;
(2)现代开采金矿:先以NaCN溶液浸取粉碎的含金(Au)矿石,得到 Na[Au(CN)2](二氰合金酸钠)溶液;再用锌与Na[Au(CN)2]溶液发生置换反应生成金。“粉碎”的目的是______________ ;“浸取”反应的氧化剂是______________ ;消耗的锌与生成的金的物质的量之比为___________ 。
(3)工业上常用纯碱、焦炭、氨气反应制备NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目:____________________________________________ 。
(1)NaCN中C的化合价为
(2)现代开采金矿:先以NaCN溶液浸取粉碎的含金(Au)矿石,得到 Na[Au(CN)2](二氰合金酸钠)溶液;再用锌与Na[Au(CN)2]溶液发生置换反应生成金。“粉碎”的目的是
(3)工业上常用纯碱、焦炭、氨气反应制备NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】碘元素在海带中主要以I-的形式存在,加碘食盐中主要以 的形式存在,几种微粒之间的转化关系如图所示。
的形式存在,几种微粒之间的转化关系如图所示。
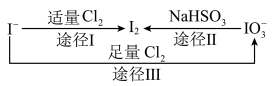
(1)写出相关反应离子方程式:
途径Ⅰ:__________________ ;
途径Ⅱ:__________________ ;
途径Ⅲ:__________________ 。
(2)溶液中I-与一定量Cl2反应,生成物质的量相同的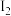 和
和 ,则反应的总离子方程式为
,则反应的总离子方程式为____________ 。
 的形式存在,几种微粒之间的转化关系如图所示。
的形式存在,几种微粒之间的转化关系如图所示。
(1)写出相关反应离子方程式:
途径Ⅰ:
途径Ⅱ:
途径Ⅲ:
(2)溶液中I-与一定量Cl2反应,生成物质的量相同的
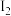 和
和 ,则反应的总离子方程式为
,则反应的总离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氧硫化碳(COS)可替代磷化氢(PH3)而被用作熏蒸剂,粉末状的KSCN与浓硫酸在一定条件下可得到COS和两种硫酸氢盐,生成物的物质的量之比为1∶1∶1,写出相应的化学方程式_____ 。
(2)氧硫化碳水解及部分应用流程如下(部分产物已略去):
COS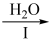 H2S
H2S Na2S
Na2S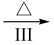 M溶液+H2
M溶液+H2
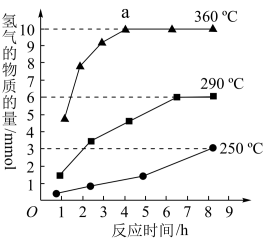
如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol),由图象分析可知,a点时M溶液中除S2O 外,还有
外,还有_____ (填含硫微粒的离子符号)。
(2)氧硫化碳水解及部分应用流程如下(部分产物已略去):
COS
 H2S
H2S Na2S
Na2S M溶液+H2
M溶液+H2如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol),由图象分析可知,a点时M溶液中除S2O
 外,还有
外,还有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是_______ (填序号,下同),主要成分属于盐类的是_______ ,相互间能发生反应的是_______ 。
(2)食盐不慎洒落在天然气的火焰上,可观察到_______ 。
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是_______ 。
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的_______ (填物质名称),将该反应的离子方程式补充完整:
ClO- + CO2 + H2O =_______ + _____
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为_______ 。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,可观察到
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的
ClO- + CO2 + H2O =
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。部分元素在周期表中位置如图:
回答下列问题:
(1)六种元素中,非金属性最强的元素是:____ ,其在元素周期表中的位置是___ ;写出As原子的最外层的电子排布式____ ,As原子核外有____ 个未成对电子。
(2)根据元素周期律,可判断原子半径Ga____ As。(选填“>”、“<”或“=”)。
(3)根据元素周期律,可判断PH3的分子构型是____ ,属于____ 分子(填“极性”或“非极性”)。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,可能的原因是___ 。
| Al | Si | P |
| Ga | Ge | As |
回答下列问题:
(1)六种元素中,非金属性最强的元素是:
(2)根据元素周期律,可判断原子半径Ga
(3)根据元素周期律,可判断PH3的分子构型是
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表的用途广泛。
(1)用“>”或“<”填空:
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液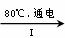 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
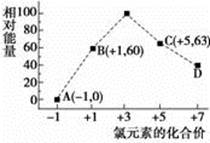
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
(1)用“>”或“<”填空:
| 离子半径 | 非金属性 | 熔点 | 沸点 |
| K+_____S2- | N____O | 金刚石_____晶体硅 | HF____HCl |
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液
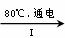 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。

①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了①~⑩十种元素在周期表中的位置。
回答下列问题:
(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________ 。
(2)这10种元素中,化学性质最不活泼的元素是_____________ (填元素符号,下同),得电子能力最强的原子是__________________ ,失电子能力最强的单质与水反应的化学方程式是_________________________ 。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是____________________ (填化学式)
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为______________________________ 。
(6)元素 ①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ⑩ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ | ||
回答下列问题:
(1)①、④按原子个数比1:1 组成的分子的电子式为
(2)这10种元素中,化学性质最不活泼的元素是
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为
(6)元素 ①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的元素是___________ ,电负性最小的金属元素是___________ 。
(2)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子,离子半径由大到小的顺序是___________ 。
(4)①和⑨的最高价氧化物对应水化物的化学式分别为___________ 、___________ 。
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:___________ 。
(7)⑨元素的价层电子轨道表示式为___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第二周期 | ⑥ | ⑦ | ||||||
| 第三周期 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 第四周期 | ② | ④ | ⑨ |
(2)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应水化物的化学式分别为
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素的价层电子轨道表示式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)金属性最强的元素是___ ;
(2)属于稀有气体元素的是___ ;
(3)可用于制造光导纤维的氧化物是___ ;
(4)C与F的原子半径较大的是___ ;
(5)H2S与HCl热稳定性较弱的是___ ;
(6)Mg(OH)2与Al(OH)3中,能与强碱溶液反应的是___ ;
(7)外层电子数为17的原子,其元素符号是___ ;
(8)某阴离子结构示意图为 ,其离子符号是
,其离子符号是___ ;
(9)P元素最高价氧化物对应水化物的化学式是___ ;(填“H3PO4”或“HPO3”);
(10)HClO4中氯元素的化合价是___ ,写出工业冶炼Al的化学方程式:___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | F | |||||
| 3 | Na | Mg | Al | P | S | Cl | Ar |
(2)属于稀有气体元素的是
(3)可用于制造光导纤维的氧化物是
(4)C与F的原子半径较大的是
(5)H2S与HCl热稳定性较弱的是
(6)Mg(OH)2与Al(OH)3中,能与强碱溶液反应的是
(7)外层电子数为17的原子,其元素符号是
(8)某阴离子结构示意图为
 ,其离子符号是
,其离子符号是(9)P元素最高价氧化物对应水化物的化学式是
(10)HClO4中氯元素的化合价是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界______ 。
(2)表中最活泼的金属与最活泼的非金属形成的物质是___________ (填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:___________ ,这两种化合物中所含的化学键有______ (填字母)。
A.共价键 B.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为___________ (填离子符号)。
(5)d、m对应的离子还原性由强到弱顺序为___________ (填离子符号)。
(6)d、e、m、p的气态氢化物中,最不稳定的是___________ (填分子式)。

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界
(2)表中最活泼的金属与最活泼的非金属形成的物质是
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
A.共价键 B.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为
(5)d、m对应的离子还原性由强到弱顺序为
(6)d、e、m、p的气态氢化物中,最不稳定的是
您最近一年使用:0次



