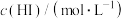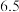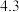下列实验操作和现象能达到相应实验目的是
| 操作及现象 | 实验目的 | |
| A | 向2mL 0.1mol/L FeCl3溶液中滴加0.1mol/L KI溶液5~6滴,充分反应后,再滴加几滴0.01mol/L KSCN溶液,出现血红色溶液 | 证明Fe3+与I—之间的反应属于可逆反应 |
| B | 向某溶液中滴加稀NaOH溶液,然后在液面上方用湿润的红色石蕊试纸检验,试纸未变蓝 | 检验溶液中是否存在NH |
| C | 分别向装有2mL 0.1mol/L H2C2O4溶液和2mL 0.2mol/L H2C2O4溶液的两支试管中加入4mL 0.01mol/L酸性KMnO4溶液,振荡,后者溶液先褪色 | 探究浓度对反应速率的影响 |
| D | 将碳酸钙与6mol/L盐酸产生的气体直接通入硅酸钠溶液,产生白色胶状沉淀 | 证明C的非金属性强于Si |
| A.A | B.B | C.C | D.D |
更新时间:2022-12-05 10:27:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向Ca(ClO)2溶液中通入SO2气体 | 有沉淀生成 | 酸性:H2SO3>HClO |
| B | 向5mL碘水中加入1mLCCl4振荡,静置 | 上层无色,下层紫色 | 符合“相似相溶”规律 |
| C | 将足量的H2O2溶液滴入少量的酸性高锰酸钾溶液 | 溶液的紫色褪去 | H2O2具有漂白性 |
| D | 向某溶液中滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验设计能达到实验目的的是
选项 | 实验目的 | 实验设计 |
A | 检验某盐中是否含 | 向盛某盐溶液的试管中滴入氢氧化钠溶液后,加热,观察试管口处湿润的红色石蕊试纸是否变蓝 |
B | 检验 样品是否变质 样品是否变质 | 取少量待测样品溶于蒸馏水,加入稀硝酸酸化的 溶液,观察现象 溶液,观察现象 |
C | 探究氨气是否具有还原性 | 向一干燥集气瓶同时通入纯净的氨气和氯化氢气体,观察是否有白烟产生 |
D | 除去 气体中混有的少量NO气体 气体中混有的少量NO气体 | 向该气体中充入过量空气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案设计不能达到目的的是
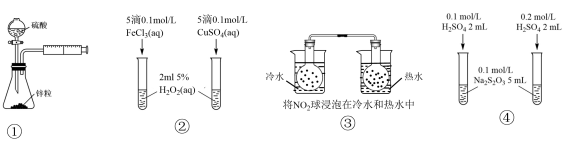

| A.①可用于测定硫酸与锌反应的化学反应速率 |
| B.②可通过实验产生气泡的快慢比较Cu2+、Fe3+对H2O2分解反应的催化效果 |
| C.③可通过球内气体颜色的深浅判断温度对平衡的影响 |
| D.④可用于探究H2SO4浓度对化学反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将足量铝片和一定体积 的盐酸充分反应,记录相关数据,作出反应过程中放出气体的体积随反应时间的变化图(如下图所示),下列说法正确的是
的盐酸充分反应,记录相关数据,作出反应过程中放出气体的体积随反应时间的变化图(如下图所示),下列说法正确的是
 的盐酸充分反应,记录相关数据,作出反应过程中放出气体的体积随反应时间的变化图(如下图所示),下列说法正确的是
的盐酸充分反应,记录相关数据,作出反应过程中放出气体的体积随反应时间的变化图(如下图所示),下列说法正确的是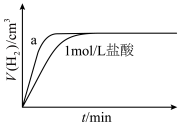
A.O点 浓度最大,此时反应速率最快 浓度最大,此时反应速率最快 |
B.出现曲线a图像,可能采取的措施为在溶液中加入少量 |
C.出现曲线a图像,可能采取的措施是将 的盐酸用 的盐酸用 的硫酸代替 的硫酸代替 |
D.为探究 浓度对反应速率的影响,在保持其他条件相同的情况下,将 浓度对反应速率的影响,在保持其他条件相同的情况下,将 的盐酸替换成 的盐酸替换成 的硫酸进行对照 的硫酸进行对照 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某学习小组研究过氧化氢溶液与氢碘酸( )反应:
)反应: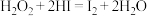 ,室温下得到实验数据如下表。已知:该反应的速率方程可表示为
,室温下得到实验数据如下表。已知:该反应的速率方程可表示为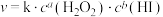 。
。
下列说法不正确 的是
 )反应:
)反应: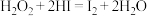 ,室温下得到实验数据如下表。已知:该反应的速率方程可表示为
,室温下得到实验数据如下表。已知:该反应的速率方程可表示为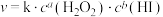 。
。实验编号 | ① | ② | ③ | ④ | ⑤ |
|
|
|
|
|
|
|
|
|
|
|
|
从混合至溶液出现棕黄色的时间 | 13 |
|
|
|
|
A.实验①进行 后测得 后测得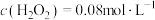 ,则 ,则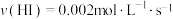 |
B.对比表中数据, , , |
C.实验③若改用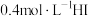 ,推测出现棕黄色的时间约为 ,推测出现棕黄色的时间约为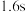 |
| D.将实验⑤的温度升高,溶液出现棕黄色时间变长,可能是温度升高使双氧水分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏伽德罗常数的值,下列说法正确的有( )个
①常温常压下,28gC2H4和C4H8的混合物中一定含有6NA个原子
②0℃,101kPa,22.4LCl2通入足量的NaOH溶液充分反应,有2NA个电子转移
③常温下,pH=12的氢氧化钠溶液中OH-数目为0.01NA
④1L1.0mol/LFeCl3溶液全部水解制备氢氧化铁胶体,所得氢氧化铁胶体数目为NA
⑤同温同压下,O2和CO组成的混合气体的密度是氢气的15倍,则O2和CO的体积比1:1
⑥常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA
⑦lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
⑧100克质量分数为46%的乙醇溶液中,含有的氧原子数目为4NA
⑨标准状况下,22.4LHF气体中含有NA个气体分子
①常温常压下,28gC2H4和C4H8的混合物中一定含有6NA个原子
②0℃,101kPa,22.4LCl2通入足量的NaOH溶液充分反应,有2NA个电子转移
③常温下,pH=12的氢氧化钠溶液中OH-数目为0.01NA
④1L1.0mol/LFeCl3溶液全部水解制备氢氧化铁胶体,所得氢氧化铁胶体数目为NA
⑤同温同压下,O2和CO组成的混合气体的密度是氢气的15倍,则O2和CO的体积比1:1
⑥常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA
⑦lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
⑧100克质量分数为46%的乙醇溶液中,含有的氧原子数目为4NA
⑨标准状况下,22.4LHF气体中含有NA个气体分子
| A.4 | B.1 | C.2 | D.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,NA为阿伏加 德罗常数的值。下列说法中正确的是( )
A.0.5mol雄黄(As4S4,已知As和N同主族,结构如图)含有NA个S-S键 |
| B.合成氨工业中,投料1mol[N2(g)+3H2(g)]可生成2NA个[NH3(g)] |
| C.用惰性电极电解1L浓度均为2mol•L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子发生转移时,阴极析出6.4g金属 |
| D.273K,101kPa下,1mol过氧化氢分子中含有的共用电子对数目为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
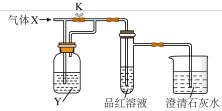
【推荐1】用下列实验装置进行相应实验,能达到实验目的的是
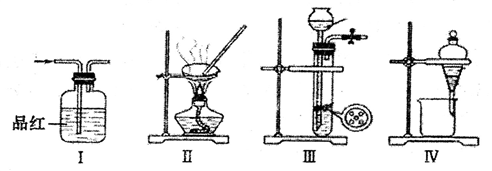

| A.将装置I中通入C12和SO2的混合气体,然后加热褪色后的溶液,据溶液是否变红来证明SO2的是否存在 |
| B.用装置Ⅱ来蒸发浓缩CuSO4溶液,并通过冷却结晶、过滤的方法获得胆矾晶体 |
| C.用浓氨水和块状固体NaOH在装置III中作用,来快速制取NH3 |
| D.用装置IV来分离乙醇萃取碘水后的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设计实验方案,分析实验原理,解决实验问题,是化学独特的学科思想。下图所示,当把胶头滴管内液体全部滴入试管中时,能达到实验目的的是
| A | B | C | D |
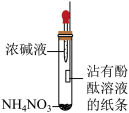 | 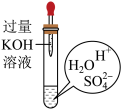 |  | 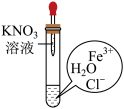 |
| 检验铵根离子 | 处理酸性废水 | 检验气体成分 | 证明反应发生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次