各题中的物质均由核电荷数为1~10的元素组成,按要求填写化学式:
(1)只有两个原子核和两个电子组成的分子是_______ ;
(2)最外层有5个电子的原子所形成的氢化物_______ ;
(3)由3个原子组成的电子总数为10的化合物是_______ ;
(4)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是_______ 。
(1)只有两个原子核和两个电子组成的分子是
(2)最外层有5个电子的原子所形成的氢化物
(3)由3个原子组成的电子总数为10的化合物是
(4)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是
更新时间:2022-12-11 08:43:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
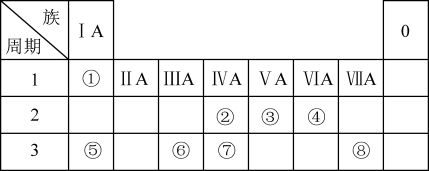
(1)地壳中含量居于第二位的元素在周期表中的位置是________________ 。
除稀有气体外,原子半径最大的元素是______ ,它的原子结构示意图是________ 。
(2)②的最高价氧化物的分子式为________ ;
⑦的最高价氧化物对应水化物的分子式为________ ;
最高价氧化物对应的水化物中酸性最强的是________ 。
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:________________________________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是________ 。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为________________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
除稀有气体外,原子半径最大的元素是
(2)②的最高价氧化物的分子式为
⑦的最高价氧化物对应水化物的分子式为
最高价氧化物对应的水化物中酸性最强的是
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F为六种20号以前的元素,其核电荷数依次增大,A、B同周期,两者相隔一元素;B、D同主族相邻,A、B、D三种元素的核电荷数之为和30。C、E能形成CE型离子化合物。F的次外层有8个电子,已知它的最外层不止一个电子。回答:
(1)写出各元素名称:A___ ; B___ ;C___ ;D___ ;E____ ;F____ ;
(2)A、D、E最高价氧化物的水化物酸性由强到弱的顺序(填化学式):___________ ;
(3)比较A、B气态氢化物的稳定性(填化学式):_____________ ;
(4)比较D、E氢化物的还原性(填化学式):_____________________ 。
(1)写出各元素名称:A
(2)A、D、E最高价氧化物的水化物酸性由强到弱的顺序(填化学式):
(3)比较A、B气态氢化物的稳定性(填化学式):
(4)比较D、E氢化物的还原性(填化学式):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,元素①-⑦是短周期的主族元素,请参照元素①-⑥在表中的位置,回答下列问题:
(1)写出⑥在元素周期表中的位置_____ 。
(2)②的气态氢化物的沸点____ ⑥的气态氢化物的沸点。(填大于、小于或等于)
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
_____ 。
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是_____ , 与该化合物晶体类型相同的是______ (请用相应的编号填写)。
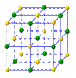
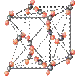

A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为_____ ,化合物乙与过量盐酸反应的化学方程式为_____ 。
| ① | ② | |||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)写出⑥在元素周期表中的位置
(2)②的气态氢化物的沸点
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是



A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为______ 。
(2)写出与H2O分子互为等电子体的微粒________________ (填2种)。
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为_________ ,与冰的晶体类型相同的是________ (请用相应的编号填写)
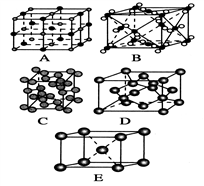
(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有___ 个K+和___ 个O2— ;晶体中K+ 的配位数为___ ,O2— 的配位数为______ 。
(5)60 g 金刚石中的共价键数为_________ 个,60g SiO2晶体中的共价键数为_______ 个。
(1)水分子中氧原子在基态时核外电子排布式为
(2)写出与H2O分子互为等电子体的微粒
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为

(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有
(5)60 g 金刚石中的共价键数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.硒—钴—镧La 三元整流剂在导电玻璃中应用广泛,且三种元素形成的单质及其化合物均有重要的应用。请回答下列问题:
(1)钴位于元素周期表中_____ (填“s”、“p”、“d”或“ds”)区,与钴位于同一周期且含有相同未成对电子数的元素有_____ 种。
(2)元素Se 、O、N 的第一电离能由大到小的顺序_____ 。
硒的某种氧化物为链状聚合结构如图所示,该氧化物的化学式为_____ 。
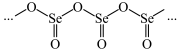
(3)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用图表示。
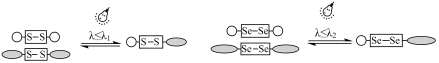
已知光的波长与键能成反比,则图中实现光响应的波长: λ1_________ λ 2 (填“>”、“<”或“=”),其原因是_____ 。
Ⅱ.
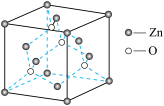
(4)ZnO 的晶胞结构如下图,则 Zn2+的配位数为_____ ;已知晶胞参数为 a cm,该晶体的密度为_____ g cm-3(写出计算式,阿伏加德罗常数的值为 NA)。
(1)钴位于元素周期表中
(2)元素Se 、O、N 的第一电离能由大到小的顺序
硒的某种氧化物为链状聚合结构如图所示,该氧化物的化学式为

(3)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用图表示。

已知光的波长与键能成反比,则图中实现光响应的波长: λ1
Ⅱ.
(4)ZnO 的晶胞结构如下图,则 Zn2+的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)基态Cu原子核外电子排布式_____ ,CuH是_____ 晶体。
(2)写出CuH在氯气中燃烧的化学反应方程式:_____ 。
(3)CuH溶解在稀盐酸中生成的气体是_____ (填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:_____ 。
II.某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1molX在该反应中失去3.01×1023个电子。
(5)X的化学式为_____ 。
(6)写出该反应的化学方程式:_____ 。
(1)基态Cu原子核外电子排布式
(2)写出CuH在氯气中燃烧的化学反应方程式:
(3)CuH溶解在稀盐酸中生成的气体是
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
II.某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1molX在该反应中失去3.01×1023个电子。
(5)X的化学式为
(6)写出该反应的化学方程式:
您最近一年使用:0次



