下表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是_______ (填元素符号,下同);金属性最强的元素是_______ ;单质的化学性质最不活泼的元素是_______ ;气体单质有颜色的元素_______ ;可运输浓硫酸的金属元素是_______ 。
(2)最高价氧化物对应水化物酸性最强的是_______ ,碱性最强的是_______ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是_______ (填化合物化学式);
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:_______ ,氢氧化铝治疗胃酸分泌过多的离子方程式:_______ 。
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:
更新时间:2022-12-16 19:34:36
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有以下几种物质:①锌丝;②CO2;③75%酒精溶液;④稀盐酸;⑤H2SO4;⑥NaOH固体;⑦熔融KNO3。
(1)以上物质属于单质的是____ (填序号,下同),属于电解质的是____ ,属于非电解质的是_____ 。
(2)①与⑤的稀溶液反应的化学方程式为____ 。
(3)写出硝酸银溶液与④反应的离子方程式是____ 。
(4)在发生离子反应的反应物或生成物中,一定存在的是____ (填字母)。
(5)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表____ 。
(6)根据酸能电离出H+的数目可将酸分为一元酸 如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
①H2SO3是二元酸,写出它与Ba(OH)2反应生成的酸式盐的方程式____ 。
②H3PO3能与KOH反应生成两种盐,则H3PO3是____ 元酸,生成的正盐的方程式_____ 。
(1)以上物质属于单质的是
(2)①与⑤的稀溶液反应的化学方程式为
(3)写出硝酸银溶液与④反应的离子方程式是
(4)在发生离子反应的反应物或生成物中,一定存在的是
| A.单质 | B.氧化物 | C.酸 | D.化合物 |
(6)根据酸能电离出H+的数目可将酸分为一元酸
 如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。①H2SO3是二元酸,写出它与Ba(OH)2反应生成的酸式盐的方程式
②H3PO3能与KOH反应生成两种盐,则H3PO3是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在第一次世界大战期间,德国首次使用了毒气战——氯气,氯气化学式为Cl2.常温常压下为黄绿色,有强烈刺激性气味的剧毒气体,可溶于水和碱溶液,可以用来消毒自来水和制造漂白液、漂白粉,也可用于制盐酸。
(1)标出下列物质中Cl元素的化合价:HClO4_________ ,KClO3_________ ,NaClO_________ 。
(2)实验室制氯气的方程式MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①将上述反应改写成离子方程式:_________ 。
②上述反应中,被还原的物质是_________ (填化学式,下同),被氧化的物质是_________ 。
③用单线桥法标出该反应的电子转移情况:_________ 。
(3)有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O
根据上述两个反应回答:
a.氧化性强弱顺序为_________ ,还原性强弱顺序为_________ 。
b.反应①中氧化产物和还原产物的分子个数之比为_________ 。
c.反应②中浓盐酸表现出的性质是酸性和_________ 。
A.还原性 B.氧化性
(1)标出下列物质中Cl元素的化合价:HClO4
(2)实验室制氯气的方程式MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O①将上述反应改写成离子方程式:
②上述反应中,被还原的物质是
③用单线桥法标出该反应的电子转移情况:
(3)有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O
根据上述两个反应回答:
a.氧化性强弱顺序为
b.反应①中氧化产物和还原产物的分子个数之比为
c.反应②中浓盐酸表现出的性质是酸性和
A.还原性 B.氧化性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】结合下图所示元素周期表,回答下列问题:
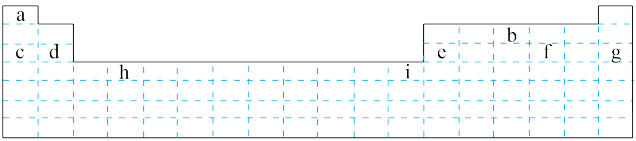
(1)表中所列元素,属于金属元素的有_______ (填字母)
(2)d元素位于第_______ 周期第_______ 族。
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应,写出反应的离子方程式:_______ 、_______ 、_______ 。

(1)表中所列元素,属于金属元素的有
(2)d元素位于第
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】结合元素周期表,用化学用语回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。_______

(2)表中所列元素,属于短周期元素的有____ ,属于主族元素的有___ 种;i元素位于第_____ 周期第______ 族。
(3)元素f是第____ 周期____ 族元素,请在如图方框中按氮元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。______
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是_______ (填标号)。
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。

(2)表中所列元素,属于短周期元素的有
(3)元素f是第

(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:

(1)地壳中含量最高的金属元素是___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)用电子式表示J与C形成化合物的过程:___________ 。
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。

(1)地壳中含量最高的金属元素是
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)用电子式表示J与C形成化合物的过程:
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等;氮是地球上极为丰富的元素。
(1)在光照条件下,氯气和氢气反应过程如下:
①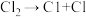 ②
②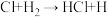 ③
③
反应②中形成的化合物的电子式为___________ 。
(2)与氯元素同周期且金属性最强的元素位于周期表的第___________ 周期___________ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是___________ 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:___________ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:___________ 。
(5)已知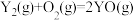
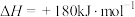 ,其中
,其中 键、
键、 键的键能分别为
键的键能分别为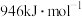 、
、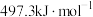 ,则
,则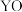 分子中
分子中 、
、 之间共价键的键能为
之间共价键的键能为___________ 。
(1)在光照条件下,氯气和氢气反应过程如下:
①
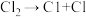 ②
②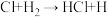 ③
③
反应②中形成的化合物的电子式为
(2)与氯元素同周期且金属性最强的元素位于周期表的第
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
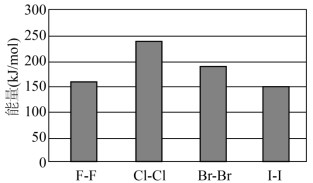
②卤素单质键能大小与键长的关系为:
(5)已知
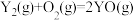
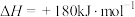 ,其中
,其中 键、
键、 键的键能分别为
键的键能分别为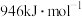 、
、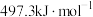 ,则
,则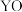 分子中
分子中 、
、 之间共价键的键能为
之间共价键的键能为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下面为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
(1)①的元素名称为:___________ ,元素④的原子结构示意图为___________ 。
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
(3)②、④组成的能引起温室效应的化合物的电子式为___________ ,其中含有的化学键为___________ 。
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为___________ (用化学式表示)。
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为___________ (用元素符号表示)。
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
| A.②的单质为固体,而③的单质为气体 |
| B.原子半径②比③大 |
| C.②的非金属性比③弱 |
| D.原子序数③比②大 |
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式
您最近一年使用:0次



