NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第_______ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(4)Na的最高价氧化物对应的水化物的化学式为_______ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物对应的水化物的化学式为
更新时间:2022-12-19 00:16:27
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】根据①~⑫元素的编号所在周期表中的位置,用相应的元素符号或者化学用语回答有关问题:
(1)能显+1 价,还能显-1 价的元素是___________ 。
(2)最难形成化合物的元素是___________ 。
(3)单质具有半导体性质的元素是___________ 。
(4)任意排放的氧化物溶于雨水形成酸雨的元素是___________ 。
(5)元素⑦氢化物水溶液与 SiO2反应的化学方程式为___________ 。
(6)最新发现的一种单质是由 60 个原子组成球状结构的分子。这种单质叫足球烯,它是由___________ 元素组成的。
(7)第三周期某元素氢化物(组成为 RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为___________ 。
(8)元素⑤与元素⑩形成化合物化学式为___________ ,该化合物在工业上用途是 ___________ (列举一种即可)。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)能显+1 价,还能显-1 价的元素是
(2)最难形成化合物的元素是
(3)单质具有半导体性质的元素是
(4)任意排放的氧化物溶于雨水形成酸雨的元素是
(5)元素⑦氢化物水溶液与 SiO2反应的化学方程式为
(6)最新发现的一种单质是由 60 个原子组成球状结构的分子。这种单质叫足球烯,它是由
(7)第三周期某元素氢化物(组成为 RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为
(8)元素⑤与元素⑩形成化合物化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】与氯元素同族的短周期元素的原子,其核外能量最高的电子所处的电子亚层是________ ;碘元素在元素周期表中的位置是___________ ;液溴的保存通常采取的方法是__________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】元素周期表是元素周期律的具体表见形式,是学习和研究化学的重要工具,下图是元素周期表的一部分。请根据要求回答问题:
1.1869年俄国化学家___________ 在多年的研究和大量的试验基础上,编排出了世上第一张元素周期表,有力的推动了近代科学的发展,在世界上留下了不朽的光荣。
2. 在元素周期表中的位置为
在元素周期表中的位置为___________ 。
3.分析上表规律,可推知,表中X的元素符号为___________ 。所列前20种元素中,最高价氧化物对应的水化物酸性最强的是___________ (填酸的化学式)。
4.写出一种由原子序数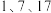 三种元素组成化合物的化学式
三种元素组成化合物的化学式___________ 。
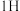 氢 | 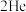 氦 | |||||||
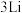 锂 | 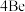 铍 | 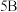 硼 | 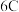 碳 | 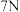 氮 |  氧 | 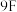 氟 | 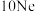 氖 | |
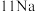 钠 |  镁 | 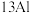 铝 | 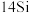 硅 | 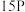 磷 | X | 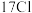 氯 | 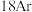 氩 | |
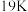 钾 | 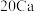 钙 | …… | ||||||
2.
 在元素周期表中的位置为
在元素周期表中的位置为3.分析上表规律,可推知,表中X的元素符号为
4.写出一种由原子序数
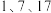 三种元素组成化合物的化学式
三种元素组成化合物的化学式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】已知溴原子的原子结构示意图为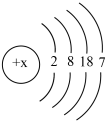
(1)溴元素在元素周期表中位置是___________ 。
(2)溴元素的最低化合价为___________ ,溴元素的最高价氧化物的水化物的化学式为___________ 。
(3)溴元素的非金属性比氯元素的非金属性___________ (选填“强”或“弱”)。
(4)向 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为___________ 。继续加入少量苯,充分振荡,静置后观察到实验现象为___________ 。

(1)溴元素在元素周期表中位置是
(2)溴元素的最低化合价为
(3)溴元素的非金属性比氯元素的非金属性
(4)向
 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是____________ 。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________ (填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式 _______________________________ 。
(3)只由④形成的18电子微粒的电子式________________ 。
(4)写出由①和③形成的离子化合物的化学式____________________________ 。
(5)用电子式表示⑦和⑨形成的化合物的形成过程_________________________________ 。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式_________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(3)只由④形成的18电子微粒的电子式
(4)写出由①和③形成的离子化合物的化学式
(5)用电子式表示⑦和⑨形成的化合物的形成过程
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
(1)元素⑤在周期表中的位置描述为____________ ,元素⑧的元素符号__________________ 。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________ (填化学式)。
(3)元素②的单质的电子式______________ ,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________ (填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低 的顺序是___________________ (用化学式表示)。
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______ 。
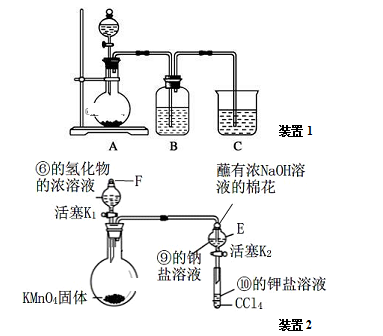
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______ (填“能”或“不能”)证明非金属性⑥>⑨>⑩。
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
| ⑩ | |||||||||||||||||
(1)元素⑤在周期表中的位置描述为
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是
(3)元素②的单质的电子式
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:

b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。几种主族元素在周期表中的位置如图:

根据上表回答下列问题:
(1)⑥元素的氢化物是______ (填化学式)。
(2)③④⑦三种元素简单离子半径由大到小的顺序是______ (用离子符号表示)。
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是______ ,用电子式表示该化合物的形成过程______ 。
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是______ ,最高价氧化物对应水化物酸性最强的化合物的化学式是______ 。
(5)写出②与水反应的离子方程式为______ 。
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是______ (填字母,下同)。
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是______ 。


根据上表回答下列问题:
(1)⑥元素的氢化物是
(2)③④⑦三种元素简单离子半径由大到小的顺序是
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是
(5)写出②与水反应的离子方程式为
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】海洋是巨大的化学资源宝库。从海水中可以制取氯、溴、镁等多种化工产品。
(1)Mg在元素周期表中的位置是第_______ 周期、第IIA族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是_______ 。
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,_______ ,原子半径Na大于Mg,失电子能力Na强于Mg。
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是_______ (填字母)。
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
(1)Mg在元素周期表中的位置是第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】元素周期表的一部分,按要求完成各小题。
(1)金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有下列四种微粒:①168O、②2311Na、③2412Mg、④14 7N
(1)按原子半径由大到小顺序排列的是___________________ (用序号回答,下同)
(2)微粒中质子数小于中子数的是______________________________
(3)在化合物中呈现的化合价的数值最多的是____________________
(4)能形成X2Y2型化合物的是___________ 。
(1)按原子半径由大到小顺序排列的是
(2)微粒中质子数小于中子数的是
(3)在化合物中呈现的化合价的数值最多的是
(4)能形成X2Y2型化合物的是
您最近一年使用:0次

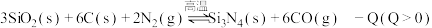 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空: 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列 属于
属于

