请分析下列氧化还原反应,该反应为实验室用MnO2和浓盐酸(注意不是稀盐酸)反应制备Cl2:MnO2 + 4 HCl(浓)  MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
(1)用双线桥法表示出电子转移方向和数量____________________
(2)该反应的氧化剂是___________ ,被氧化的元素是___________ 元素。
(3)HCl在该反应中体现的化学性质有___________ 、___________
(4)实验测定,当MnO2足量时,无论如何控制条件,用含146g HCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的原因可能是___________
 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O(1)用双线桥法表示出电子转移方向和数量
(2)该反应的氧化剂是
(3)HCl在该反应中体现的化学性质有
(4)实验测定,当MnO2足量时,无论如何控制条件,用含146g HCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的原因可能是
21-22高一上·广东汕头·阶段练习 查看更多[2]
更新时间:2022-12-20 20:02:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】两同学为制得纯净的Fe(OH)2,使用如图所示的装置,A管中是Fe和H2SO4,B管中是NaOH溶液:
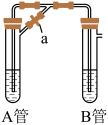
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是___________ ;
(2)同学乙:打开a,使A管中反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是___________ ,B中发生反应的离子方程式为____________________________________
(3)在制备纯净的Fe(OH)2实验中,一定要注意避免Fe(OH)2被氧化,一旦实验失败就会看到白色絮状沉淀逐渐变为灰绿色,最后变成红褐色,请写出这个过程的化学方程式,并用单线桥法标出电子转移的方向和数目:_________________________________

(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是
(2)同学乙:打开a,使A管中反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是
(3)在制备纯净的Fe(OH)2实验中,一定要注意避免Fe(OH)2被氧化,一旦实验失败就会看到白色絮状沉淀逐渐变为灰绿色,最后变成红褐色,请写出这个过程的化学方程式,并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中一定有_______ 。有关的离子方程式为:_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(5)写出Fe2O3 与CO 在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目_______ 。
(6)写出Cu和AgNO3 溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目_______ 。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中一定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.Cl- | B.NO | C.CO | D.OH- |
(6)写出Cu和AgNO3 溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、X、Y六种物质均由短周期元素组成,其中X为常见离子化合物,它们之间的转换关系如下图所示
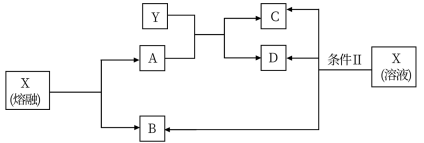
(1)已知条件I和条件II相同,则该反应条件为____________________ 。
(2)物质X的电子式为_____________________ 。
(3)写出B与Ca(OH)2反应的化学方程式______________________________ 。
(4)写出X在条件II下反应生成B、C、D的离子方程式_____________________________________________ 。
(5)写出实验室制B的化学方程式,并标出电子转移方向、数目____________________________________________ 。
(6)请简述鉴定物质X的实验方法____________________________________ 。

(1)已知条件I和条件II相同,则该反应条件为
(2)物质X的电子式为
(3)写出B与Ca(OH)2反应的化学方程式
(4)写出X在条件II下反应生成B、C、D的离子方程式
(5)写出实验室制B的化学方程式,并标出电子转移方向、数目
(6)请简述鉴定物质X的实验方法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】铝氢化钠(NaAlH4)是有机合成中的重要还原剂,其合成线路如图所示。
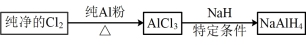
已知AlCl3的熔点194℃(0.25MPa),177.8℃开始升华,在潮湿的空气中易水解。某实验小组利用如图装置(尾气处理装置未画出)制备无水AlCl3。
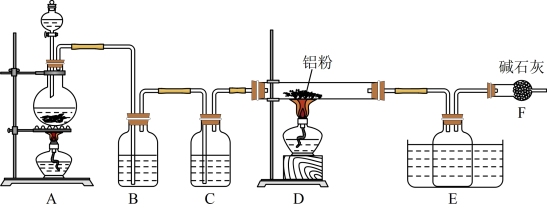
(1)写出Cl2的电子式_______ 。
(2)①写出圆底烧瓶中发生反应的离子方程式:_______ 。
②装置B的作用是_______ ,装置F的作用是_______ 。
(3)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂中,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是_______ 。
(4)铝氢化钠与水反应生成四羟基合铝酸钠和氢气,利用氢气的体积测定铝氢化钠样品的纯度。
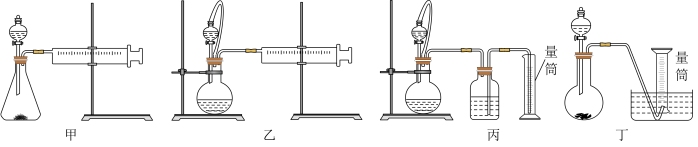
①该反应的化学方程式为_______ 。
②设计如图四种装置测定铝氢化钠样品的纯度(杂质不参与反应)。从简约性、准确性考虑,最合适的装置是_______ (填序号)。
(5)Cl2的尾气可选择NaOH吸收,其反应的离子方程式为_______ 。

已知AlCl3的熔点194℃(0.25MPa),177.8℃开始升华,在潮湿的空气中易水解。某实验小组利用如图装置(尾气处理装置未画出)制备无水AlCl3。

(1)写出Cl2的电子式
(2)①写出圆底烧瓶中发生反应的离子方程式:
②装置B的作用是
(3)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂中,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是
(4)铝氢化钠与水反应生成四羟基合铝酸钠和氢气,利用氢气的体积测定铝氢化钠样品的纯度。
①该反应的化学方程式为
②设计如图四种装置测定铝氢化钠样品的纯度(杂质不参与反应)。从简约性、准确性考虑,最合适的装置是

(5)Cl2的尾气可选择NaOH吸收,其反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用浓盐酸和二氧化锰制氯气的实验装置如图所示:
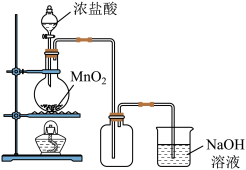
(1)下列气体实验室制备时,可以用相同发生装置的是_______
A.O2 B. H2 C.HCl D. CO2
(2)制得的氯气中还含有氯化氢杂质,可通过装有______ 的洗气瓶除去。
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________ ;漂白粉在空气中很容易变质,请写出漂白粉在空气中变质的反应方程式____ 。
(4)据报道,日常生活中,将洁厕液(主要成分是HCl)与84消毒液(主要成分是次氯酸钠)混合使用会发生中毒的事故,生成有毒的氯气。写出反应的化学方程式______ 。
(5)二氧化锰和高锰酸钾都是强氧化剂,均可将浓盐酸氧化为氯气。用浓盐酸和高锰酸钾制氯气的反应方程式如下: KMnO4 + HCl= KCl + MnCl2 + Cl2↑+ H2O
①配平该反应的化学方程式______ 。
②用“单线桥”在上述方程式上标出电子转移的方向和数目______ 。该反应中______ 元素被氧化,起酸性作用的HCl是______ mol。当有1mol电子转移时,可生成气体(标准状态下)______ 升。
(6)(如图)有人做了一个改进实验。挤压软塑料瓶,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可以看到明显的燃烧现象(金属网用以防止气体混合爆炸)。
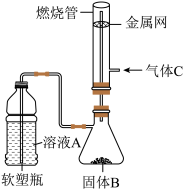
①用此装置模拟工业合成盐酸。则相应试剂选择正确的是_________ (选填序号)。
②管口可观察到的现象是__________ 。

(1)下列气体实验室制备时,可以用相同发生装置的是
A.O2 B. H2 C.HCl D. CO2
(2)制得的氯气中还含有氯化氢杂质,可通过装有
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(4)据报道,日常生活中,将洁厕液(主要成分是HCl)与84消毒液(主要成分是次氯酸钠)混合使用会发生中毒的事故,生成有毒的氯气。写出反应的化学方程式
(5)二氧化锰和高锰酸钾都是强氧化剂,均可将浓盐酸氧化为氯气。用浓盐酸和高锰酸钾制氯气的反应方程式如下: KMnO4 + HCl= KCl + MnCl2 + Cl2↑+ H2O
①配平该反应的化学方程式
②用“单线桥”在上述方程式上标出电子转移的方向和数目
(6)(如图)有人做了一个改进实验。挤压软塑料瓶,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可以看到明显的燃烧现象(金属网用以防止气体混合爆炸)。

①用此装置模拟工业合成盐酸。则相应试剂选择正确的是
| 溶液A | 固体B | 气体C | |
| a | 稀硫酸 | Zn | Cl2 |
| b | 浓盐酸 | MnO2 | H2 |
| c | 稀硝酸 | Fe | Cl2 |
| d | 浓盐酸 | KMnO4 | H2 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为____ ,装置F中试剂的作用是____ 。
②装置连接顺序:A→____→____→____→E→D。____
③写出A中反应的化学方程式____ 。
④实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是____ 。
⑤为了提高S2Cl2的纯度,实验的关键是控制好温度和____ 。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图实验方案来测定该混合气体中SO2的体积分数。
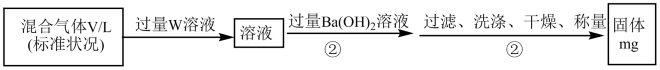
①W溶液可以是____ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为____ (用含V、m的式子表示)。
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②S2Cl2+Cl2  2SCl2 2SCl2③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为
②装置连接顺序:A→____→____→____→E→D。
③写出A中反应的化学方程式
④实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
⑤为了提高S2Cl2的纯度,实验的关键是控制好温度和
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图实验方案来测定该混合气体中SO2的体积分数。

①W溶液可以是
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次



