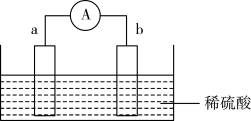
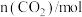如图所示,两电极一为碳棒,一为铁片, 若电流表的指针发生偏转,且a极上有大量气泡生成,则电子由_______ (填 “a”或“b”,下同)极流向_______ 极,电解质溶液中SO 移向
移向_______ 极,a极上的电极反应式为_______ 。
 移向
移向
更新时间:2022-12-20 23:18:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】完成下列填空
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
①高铁电池的负极材料是_______ 。
②放电时,正极发生_______ (填“氧化”或“还原”)反应。已知负极电极反应式为:Zn − 2e- +2OH- = Zn(OH)2,则正极电极反应式为_______ 。
③放电时,_______ (填“正”或“负”)极附近溶液的碱性增强。
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。
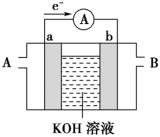
①使用时,空气从_______ 口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇,a极的电极反应式为_______ 。
(3)氧化还原滴定与中和滴定类似,指的是用已知浓度的氧化剂(还原剂)溶液滴定未知浓度的还原剂(氧化剂)溶液。现有 酸性溶液和未知浓度的无色
酸性溶液和未知浓度的无色 溶液,已知二者发生氧化还原反应的离子方程式是
溶液,已知二者发生氧化还原反应的离子方程式是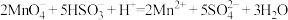 ,通过滴定实验测定
,通过滴定实验测定 溶液的浓度。完成下列问题:
溶液的浓度。完成下列问题:
①该滴定实验_______ (填“需要”或“不需要”)指示剂,滴定终点的现象为_______ 。
②滴定前平视 酸性溶液的液面,读数为amL,滴定后俯视液面,读数为bmL,则
酸性溶液的液面,读数为amL,滴定后俯视液面,读数为bmL,则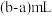 比实际消耗的
比实际消耗的 溶液体积
溶液体积_______ (填“偏大”或“偏小”)。则根据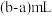 计算得到的待测液浓度比实际浓度
计算得到的待测液浓度比实际浓度_______ (填“偏大”或“偏小”)。
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:①高铁电池的负极材料是
②放电时,正极发生
③放电时,
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲醇,a极的电极反应式为
(3)氧化还原滴定与中和滴定类似,指的是用已知浓度的氧化剂(还原剂)溶液滴定未知浓度的还原剂(氧化剂)溶液。现有
 酸性溶液和未知浓度的无色
酸性溶液和未知浓度的无色 溶液,已知二者发生氧化还原反应的离子方程式是
溶液,已知二者发生氧化还原反应的离子方程式是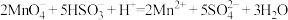 ,通过滴定实验测定
,通过滴定实验测定 溶液的浓度。完成下列问题:
溶液的浓度。完成下列问题:①该滴定实验
②滴定前平视
 酸性溶液的液面,读数为amL,滴定后俯视液面,读数为bmL,则
酸性溶液的液面,读数为amL,滴定后俯视液面,读数为bmL,则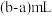 比实际消耗的
比实际消耗的 溶液体积
溶液体积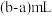 计算得到的待测液浓度比实际浓度
计算得到的待测液浓度比实际浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学知识在生活中应用广泛,但形成原电池和电解池均需要一定的条件。
(1)现有下列装置:

其中,能构成原电池的是______ (填字母代号),能构成电解池的是______ (填字母代号)。
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
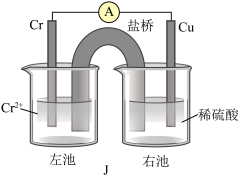
(3)已知Cr比Fe的金属性稍活泼,铜铬构成原电池如装置J所示(盐桥中装的是饱和KCl琼脂溶液)。
则Cr为______ 极(填“正”或“负”),盐桥中 移向
移向______ (填“左池”或“右池”),盛稀硫酸烧杯中的现象为______ 。
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。
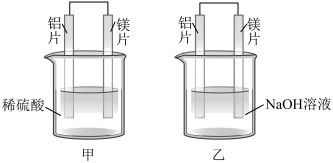
甲装置用______ (填“铝片”或“镁片”)作负极,两同学实验现象的不同之处为______ ,由此得出不能简单根据金属的活动性来判断原电池的正负极的结论,正确的判断方法是______ 。
(1)现有下列装置:

其中,能构成原电池的是
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
A. |
B.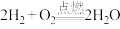 |
C.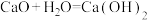 |
D. |
则Cr为
 移向
移向
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。

甲装置用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在人类生产、生活对能量的需求日益增长的今天,研究化学反应及其能量变化,合理利用常规能源和开发新能源具有十分重要的意义。能源是人类赖以生存和发展不可缺少的因素。请回答下列问题:
(1)一种蓄电池在充电和放电时发生的反应是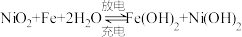 。则该电池放电时发生还原反应的物质是_______(填标号)。
。则该电池放电时发生还原反应的物质是_______(填标号)。
(2)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导O2-。则c电极的名称为
固体,它在高温下能传导O2-。则c电极的名称为_______ (填“正极”或“负极”),d电极上的电极反应式为_______ 。
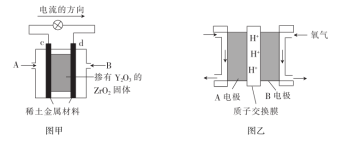
(3)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理如图乙所示。H+的移动方向为由_______ (填“A”或“B”,下同)电极到_______ 电极。写出B电极的电极反应式:_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为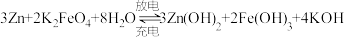 。
。
①放电时,正极发生_______ (填“氧化”或“还原”)反应。已知负极的电极反应式为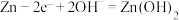 ,则正极的电极反应式为
,则正极的电极反应式为_______ 。
②放电时,_______ (填“正”或“负”)极附近溶液的碱性增强。
(1)一种蓄电池在充电和放电时发生的反应是
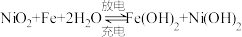 。则该电池放电时发生还原反应的物质是_______(填标号)。
。则该电池放电时发生还原反应的物质是_______(填标号)。A.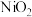 | B. | C. | D. |
 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导O2-。则c电极的名称为
固体,它在高温下能传导O2-。则c电极的名称为
(3)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理如图乙所示。H+的移动方向为由
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为
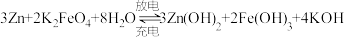 。
。①放电时,正极发生
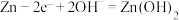 ,则正极的电极反应式为
,则正极的电极反应式为②放电时,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为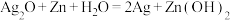 。
。
(1)工作时电流从___________ 极流向___________ 极(填“ ”或“Zn”)。
”或“Zn”)。
(2)电极反应式:
正极:___________ ,发生___________ 反应;
负极:___________ ,发生___________ 反应。
(3)工作时电池正极区的pH___________ (填“增大”、“减小”或“不变”)。
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为
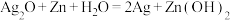 。
。(1)工作时电流从
 ”或“Zn”)。
”或“Zn”)。(2)电极反应式:
正极:
负极:
(3)工作时电池正极区的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】燃料电池是利用燃料(如H2、CO、CH4、CH3OH、NH3等)与O2反应从而将化学能转化为电能的装置。
(1)甲烷燃料电池(NaOH作电解质溶液)的负极反应式为_________________________ ,正极电极反应式为________________________________ ,放电过程中溶液的pH_______ (填“增大”、“减小”或“不变”)。
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨−液氧燃料电池示意图如图所示,有关说法正确的是____________ 。

a.电池工作时,Na+向负极移动
b.电子由电极2经外电路流向电极1
c.电池总反应为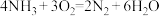
d.电极2发生的电极反应为
(3)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的________ (填“正”或“负”)极。
②正极反应式为_________________________________________________________ 。
负极反应式为___________________________________________________________ 。
③放电过程中,H+由________ 极区向________ 极区迁移(填“正”或“负”)。
④在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体_______ L。
⑤该电池________ (填“能”或“不能”)在高温下工作。
(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2−可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:

①a极电极反应式为________________________________________ 。
②工作时,O2−由电极________ 向电极________ 移动(填“a”或“b”,下同),电子由电极________ 通过传感器流向电极________ 。
(1)甲烷燃料电池(NaOH作电解质溶液)的负极反应式为
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨−液氧燃料电池示意图如图所示,有关说法正确的是

a.电池工作时,Na+向负极移动
b.电子由电极2经外电路流向电极1
c.电池总反应为
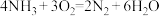
d.电极2发生的电极反应为

(3)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的
②正极反应式为
负极反应式为
③放电过程中,H+由
④在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体
⑤该电池
(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2−可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:

①a极电极反应式为
②工作时,O2−由电极
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
(1)锌片上发生的电极反应:___________________ ;
(2)银片上发生的电极反应:____________________ ;
(3)总反应的离子方程式:_________________ ;
(4)在______ 片上有气泡产生,电子从______ 片上流向_______ 片上。
(5)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算产生氢气的体积(标准状况)为___________________ 。
(1)锌片上发生的电极反应:
(2)银片上发生的电极反应:
(3)总反应的离子方程式:
(4)在
(5)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算产生氢气的体积(标准状况)为
您最近一年使用:0次
【推荐1】在容积为2L的恒温容器中,充入 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。
(1)下列说法正确的是______ (填标号)。
a.反应达到平衡后,反应不再进行
b.使用催化剂可以增大反应速率,提高生产效率
c.当容器内混合气体的平均相对分子质量不变时,说明反应达到了化学平衡状态
d.通过调控反应条件,可以提高该反应进行的程度,使 可以100%地转化为
可以100%地转化为
(2)3~6min内,
______  .
.
(3)12min末时,混合气体中 的体积分数为
的体积分数为______ 。
(4)第3min时
______ (填“>”“<”或“=”)第9min时 。
。
(5)一定温度条件下,能够说明该反应到达平衡的标志是____________ 。
①若恒压容器中,混合气体的密度保持不变;②单位时间内生成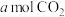 ,同时消耗
,同时消耗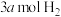 ;③
;③ 与
与 的总浓度等于
的总浓度等于 与
与 的总浓度;④
的总浓度;④ 的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
(6) 还可以直接由CO和
还可以直接由CO和 制得,根据如图一所示的转化关系判断,生成
制得,根据如图一所示的转化关系判断,生成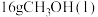 放出
放出______ kJ能量。
(7) 和
和 可以形成碱性燃料电池,结构如图二所示。
可以形成碱性燃料电池,结构如图二所示。
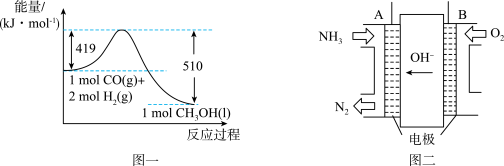
①电极A反应式为__________ 。
②若反应生成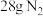 ,则该燃料电池理论上消耗的
,则该燃料电池理论上消耗的 的体积(在标准状况下)为
的体积(在标准状况下)为______ L。
 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。时间 | 0min | 3min | 6min | 9min | 12min |
| 0 | 0.50 | 0.65 | 0.75 | 0.75 |
| 1 | 0.50 | 0.35 | x | 0.25 |
(1)下列说法正确的是
a.反应达到平衡后,反应不再进行
b.使用催化剂可以增大反应速率,提高生产效率
c.当容器内混合气体的平均相对分子质量不变时,说明反应达到了化学平衡状态
d.通过调控反应条件,可以提高该反应进行的程度,使
 可以100%地转化为
可以100%地转化为
(2)3~6min内,

 .
.(3)12min末时,混合气体中
 的体积分数为
的体积分数为(4)第3min时

 。
。(5)一定温度条件下,能够说明该反应到达平衡的标志是
①若恒压容器中,混合气体的密度保持不变;②单位时间内生成
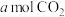 ,同时消耗
,同时消耗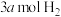 ;③
;③ 与
与 的总浓度等于
的总浓度等于 与
与 的总浓度;④
的总浓度;④ 的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;(6)
 还可以直接由CO和
还可以直接由CO和 制得,根据如图一所示的转化关系判断,生成
制得,根据如图一所示的转化关系判断,生成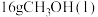 放出
放出(7)
 和
和 可以形成碱性燃料电池,结构如图二所示。
可以形成碱性燃料电池,结构如图二所示。
①电极A反应式为
②若反应生成
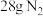 ,则该燃料电池理论上消耗的
,则该燃料电池理论上消耗的 的体积(在标准状况下)为
的体积(在标准状况下)为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过。
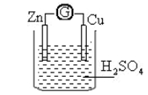
(1)锌片为________ (填“正极”或“负极”),电极反应是_______________ 。
(2)铜片为__________ (填“正极”或“负极”),发生_____ 反应(填“氧化”或“还原”)。
(3)该原电池工作时,溶液中的SO42-向_____ 极移动,铜极上的现象是____________ 。

(1)锌片为
(2)铜片为
(3)该原电池工作时,溶液中的SO42-向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氢能是发展中的新能源,它的利用包括氢的制备和储存。回答下列问题:
(1)如图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为_____ (用a、b表示)。
②正极反应式为_____ 。
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此储氢是关键技术之一、某些金属氢化物可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g) MHx+2y(s)达到化学平衡。下列有关叙述正确的是
MHx+2y(s)达到化学平衡。下列有关叙述正确的是_____ 。
a.v(放氢)=v(吸氢)
b.若通入惰性气体Ar,压强增大,反应速率增大
c.容器内气体压强保持不变
d.吸收ymolH2只需1molMHx
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_____ 。
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取Na2FeO4的同时还能获得氢气:Fe+2H2O+2OH- FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
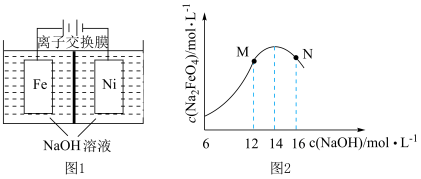
①电解一段时间后,c(OH−)降低的区域在_____ (填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_____ 。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c(Na2FeO4)低于最高值的原因:_____ 。
(1)如图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为
②正极反应式为
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此储氢是关键技术之一、某些金属氢化物可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
 MHx+2y(s)达到化学平衡。下列有关叙述正确的是
MHx+2y(s)达到化学平衡。下列有关叙述正确的是a.v(放氢)=v(吸氢)
b.若通入惰性气体Ar,压强增大,反应速率增大
c.容器内气体压强保持不变
d.吸收ymolH2只需1molMHx
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取Na2FeO4的同时还能获得氢气:Fe+2H2O+2OH-
 FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
①电解一段时间后,c(OH−)降低的区域在
②电解过程中,须将阴极产生的气体及时排出,其原因是
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c(Na2FeO4)低于最高值的原因:
您最近一年使用:0次