下列说法正确的是
A.由 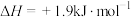 ,可知:金刚石比石墨更稳定 ,可知:金刚石比石墨更稳定 |
B.吸热反应: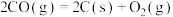 ,设 ,设 和 和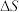 不随温度而变,则该反应任何温度下都不能自发进行 不随温度而变,则该反应任何温度下都不能自发进行 |
C.由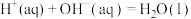 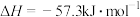 ,可知:含1mol ,可知:含1mol 的溶液与含1mol 的溶液与含1mol 的溶液混合,放出热量等于 的溶液混合,放出热量等于 |
D.2g 完全燃烧生成液态水放出 完全燃烧生成液态水放出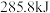 热量,则氢气燃烧的热化学方程式为 热量,则氢气燃烧的热化学方程式为 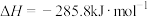 |
更新时间:2022-12-28 09:43:07
|
相似题推荐
【推荐1】2-甲氧-2-甲基丁烷(用TAME表示)常用作汽油添加剂。在催化剂作用下,可通过甲醇与烯烃的液相反应制得,体系中同时存在如下反应:
反应I:
反应II:
反应III:

反应Ⅰ、Ⅱ、Ⅲ的平衡常数Kx分别为Kx1、Kx2、Kx3(Kx是以物质的量分数代替物质的量浓度表示的平衡常数)与温度T变化关系如上图所示。现向某反应容器中加入1.0molTAME,控制温度为353K,反应30min后达到平衡状态。下列说法正确的是
反应I:

反应II:

反应III:


反应Ⅰ、Ⅱ、Ⅲ的平衡常数Kx分别为Kx1、Kx2、Kx3(Kx是以物质的量分数代替物质的量浓度表示的平衡常数)与温度T变化关系如上图所示。现向某反应容器中加入1.0molTAME,控制温度为353K,反应30min后达到平衡状态。下列说法正确的是
| A.烯烃A和B,其中A相对稳定 |
| B.反应Ⅰ、Ⅱ中,△H1大于△H2 |
| C.达到平衡时,容器中烯烃A与CH3OH的物质的量之比为1:10 |
| D.同温同压下,向该容器中注入惰性溶剂稀释,反应Ⅰ的平衡将正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中不正确的是
| A.石墨转化为金刚石需要吸收能量 |
| B.CaCO3受热分解是吸热反应 |
| C.化学变化中的能量变化主要是由化学键变化引起的 |
| D.浓硫酸溶于水是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列化学用语正确的是
A.电解液为稀硫酸的甲醇燃料电池中,负极的电极反应式为: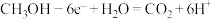 |
B.铅蓄电池中 放电时是电池的负极,充电时是电池的阳极 放电时是电池的负极,充电时是电池的阳极 |
C.用惰性电极电解饱和食盐水时阴极反应: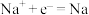 |
D. 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: 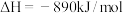 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4 kJ/mol,则含0.5 mol NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.7 kJ |
| C.可燃物的系数为1的燃烧反应的焓变即为该可燃物的燃烧热 |
| D.已知2C(s)+2O2(g)=2CO2(g) △H=a kJ/mol,2C(s)+O2(g)=2CO(g) △H=b kJ/mol,则a>b |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列热化学方程式书写正确的是
A.已知:1molH2(g)和1molCl2(g)反应生成2molHCl(g)时放出184.6kJ的热量,则有 H2(g)+ H2(g)+ Cl2(g)=HClg) △H=-92.3kJ/mol Cl2(g)=HClg) △H=-92.3kJ/mol |
| B.2NO2=O2+2NO △H=+116.2kJ/mol |
| C.已知稀溶液中,H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l) △H=571.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于反应热的叙述正确的是
| A.当ΔH<0时,表示该反应为吸热反应 |
| B.1molH2与0.5molO2反应生成1mol水时放出的热量即是H2的燃烧热 |
| C.热化学方程式中的化学计量数只能是整数,不能是分数 |
| D.1molNaOH分别和1molCH3COOH、1molHNO3反应放出的热量:CH3COOH<HNO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】含Ba(OH)217.1 g的稀溶液与足量稀盐酸反应,放出11.46 kJ热量,表示该反应中和热的化学方程式正确的是( )
| A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
| B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=114.6 kJ·mol-1 |
C. Ba(OH)2(aq)+HCl(aq)= Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 BaCl2(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 |
D. Ba(OH)2(aq)+HCl(aq)= Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l) ΔH=57.3 kJ·mol-1 BaCl2(aq)+H2O(l) ΔH=57.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法不正确的是
| A.反应4Fe(OH)2(s)+2H2O(l)+O2(g) =4Fe(OH)3(s)常温下能自发进行,该反应的ΔH<0 |
| B.反应H2S(g)+ZnO(s) =H2O(g)+ZnS(s)在一定条件下可自发进行,且ΔS<0,则ΔH>0 |
| C.反应3C(s)+CaO(s) =CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0 |
| D.SiO2(s)+2C(s) =Si(s)+2CO(g)必须在高温下反应才能发生,则ΔH>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 工业合成氨,关乎到世界化工发展和粮食安全,对其研究意义重大。下列有关合成氨反应:
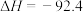 kJ⋅mol
kJ⋅mol 的说法
的说法不 正确的是

 kJ⋅mol
kJ⋅mol 的说法
的说法A.合成氨反应的 J⋅K J⋅K ⋅mol ⋅mol ,在较低温度下不能自发进行 ,在较低温度下不能自发进行 |
| B.氮气和氢气的反应活化能很大,需要外界提供能量才可能发生反应 |
C.恒温恒容密闭容器中充入1mol 和3mol 和3mol ,充分反应后放出热量小于92.4kJ ,充分反应后放出热量小于92.4kJ |
| D.温度升高,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大 |
您最近一年使用:0次

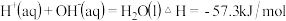 ,若将含
,若将含 的稀硫酸与含1mol NaOH的稀溶液混合,放出的热量等于
的稀硫酸与含1mol NaOH的稀溶液混合,放出的热量等于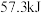
 异丁烷
异丁烷 ,则正丁烷比异丁烷稳定
,则正丁烷比异丁烷稳定 ,则
,则 的燃烧热为
的燃烧热为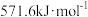
 ,
,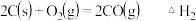 ,则
,则
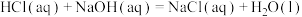
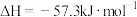 ,则
,则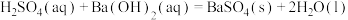
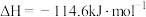

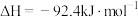 将
将 和过量的
和过量的 充分反应放出的热量为92.4kJ
充分反应放出的热量为92.4kJ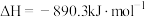 ,则
,则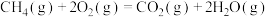
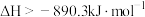
 能自发进行,则该反应的
能自发进行,则该反应的


