下列热化学方程式书写正确的是
A.已知:1molH2(g)和1molCl2(g)反应生成2molHCl(g)时放出184.6kJ的热量,则有 H2(g)+ H2(g)+ Cl2(g)=HClg) △H=-92.3kJ/mol Cl2(g)=HClg) △H=-92.3kJ/mol |
| B.2NO2=O2+2NO △H=+116.2kJ/mol |
| C.已知稀溶液中,H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l) △H=571.6kJ/mol |
更新时间:2023-10-03 10:42:37
|
相似题推荐
【推荐1】反应A+B→C+D过程中的能量变化如图所示。下列说法中错误的是( )
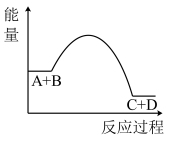

| A.该反应是放热反应 |
| B.反应物的总能量大于生成物的总能量 |
| C.反应物的总键能大于生成物的总键能 |
| D.向反应体系中加入催化剂,不会改变反应的热效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】汽车受到猛烈碰撞时,安全气囊内的 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法错误 的是
 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法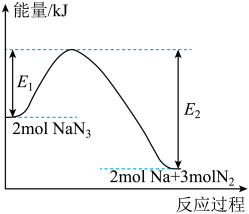
A. 属于离子化合物 属于离子化合物 |
B. 的分解反应属于放热反应 的分解反应属于放热反应 |
C.反应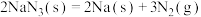 的 的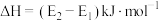 |
D. 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
您最近一年使用:0次
【推荐3】三甲胺N(CH3)3是重要的化工原料。我国科学家实现了在铜催化剂条件下将N,N—二甲基甲酰胺[(CH3)2NCHO,简称DMF]转化为三甲胺[N(CH3)3]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示(*表示物质吸附在铜催化剂上),下列说法正确的是


| A.步骤①表示DMF分子和H原子吸附在铜催化剂表面的过程,而步骤③则表明形成了N—H键 |
| B.该历程中决速步骤能垒(活化能)为0.93 eV |
| C.升高温度可以加快反应速率,并提高DMF的平衡转化率 |
| D.由图可知,该条件下,DMF完全转化为三甲胺的热化学方程式为:(CH3)2NCHO(g)+2H2(g)=N(CH3)3(g)+H2O(g) △H=-98.25 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知: (g) ⇌
(g) ⇌  (g) ΔH>0.下列说法正确的是
(g) ΔH>0.下列说法正确的是
 (g) ⇌
(g) ⇌  (g) ΔH>0.下列说法正确的是
(g) ΔH>0.下列说法正确的是| A.表示丁烯燃烧热的热化学方程式为C4H8(g) + 6O2(g)=4CO2(g) + 4H2O(g) ΔH=Q kJ·mol-1(Q<0) |
| B.该反应正反应的活化能小于逆反应的活化能 |
| C.反-2-丁烯燃烧热的数值更大 |
| D.稳定性:反-2-丁烯>顺-2-丁烯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】依据下列含硫物质转化的热化学方程式,得出的相关结论正确的是
①

②

③

①


②


③


A.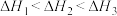 |
B. 的燃烧热为 的燃烧热为 |
| C.反应②在任何温度下都不能自发进行 |
D. 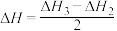 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
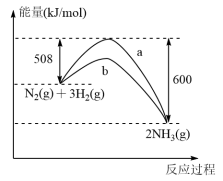

| A.已知2C(s)+2O2(g)=2CO2(g) ∆H1;2C(s)+O2(g)=2CO(g) ∆H2,则∆H1>∆H2 |
| B.已知冰的熔化热为6.0 kJ·mol-1,冰中氢键键能为20.0 kJ·mol-1,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰中的氢键,则最多只能破坏1 mol冰中5%氢键 |
C.已知H+(aq)+OH-(aq)=H2O(l) ∆H=-57.3kJ/mol则1mol强酸的稀溶液与足量的强碱反应放出热量均为 |
D.如图,可知b为加入催化剂后的能量变化,正反应活化能比逆反应活化能低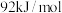 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法或表示法正确的是
| A.测定HCl和NaOH中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH起始温度和反应体系的最高温度 |
| B.由“C(石墨;S)=C(金刚石;S);△H = +1.19kJ/mol ”可知金刚石比石墨稳定 |
| C.在稀溶液中: H++OH-=H2O;△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】强酸和强碱的稀溶液中和热可表示为:H+(aq) + OH-(aq)=H2O(l);ΔH=-57.3kJ/mol,以下3个化学方程式中,反应热为-57.3kJ/mol的是
①H2SO4(aq) + 2NaOH(aq) = Na2SO4(aq) + 2H2O(l);②H2SO4(aq) + Ba(OH)2(aq) = BaSO4(s) + 2H2O(l);③NH3·H2O(aq) + HCl(aq) = NH4Cl(aq) + H2O(l)
①H2SO4(aq) + 2NaOH(aq) = Na2SO4(aq) + 2H2O(l);②H2SO4(aq) + Ba(OH)2(aq) = BaSO4(s) + 2H2O(l);③NH3·H2O(aq) + HCl(aq) = NH4Cl(aq) + H2O(l)
| A.① | B.② | C.③ | D.均不符合 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于焓变 的叙述或判断正确的是
的叙述或判断正确的是

 的叙述或判断正确的是
的叙述或判断正确的是
A.据如图可知: |
B.由 可知,若将含1mol 可知,若将含1mol  的稀溶液与含1mol NaOH的稀溶液混合,放出的热量为 的稀溶液与含1mol NaOH的稀溶液混合,放出的热量为 |
C. 、30MPa下,将 、30MPa下,将 和 和 置于密闭容器中充分反应,放出 置于密闭容器中充分反应,放出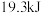 热量,则反应 热量,则反应 的 的 |
D. 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的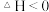 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.需要加热才能进行的化学反应一定是吸热反应 |
| B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| C.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 |
D.相同条件下稀溶液之间进行的反应① ;② ;②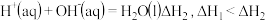 |
您最近一年使用:0次



