研究表明N2O与CO在Fe+的作用下会发生如下反应:① ,②
,② 。其能量变化示意图如下所示。下列说法不正确的是
。其能量变化示意图如下所示。下列说法不正确的是
 ,②
,② 。其能量变化示意图如下所示。下列说法不正确的是
。其能量变化示意图如下所示。下列说法不正确的是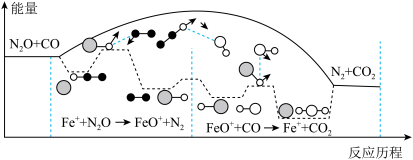
A. 使反应的活化能变小 使反应的活化能变小 |
| B.该催化剂不能有效提高反应物的平衡转化率 |
C. 与CO在不同催化剂表面上转化成 与CO在不同催化剂表面上转化成 与 与 的反应历程完全相同 的反应历程完全相同 |
D.反应①过程中, 中的极性键发生了断裂 中的极性键发生了断裂 |
更新时间:2022-12-29 20:14:45
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】有效碰撞是指
| A.反应物分子间的碰撞 | B.反应物活化分子间的碰撞 |
| C.反应物分子发生合适取向的碰撞 | D.活化分子之间发生合适取向的碰撞 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和 ,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
 ,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
A.可以通过 和 和 计算HCOOH的总键能 计算HCOOH的总键能 |
B. |
C.途径Ⅱ中 参与反应,通过改变反应途径加快反应速率 参与反应,通过改变反应途径加快反应速率 |
| D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度和压强下利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应机理和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注)。

| A.第①步存在共价键的断裂和形成 |
B.第②步是反应的决速步骤,化学方程式为 |
| C.铜基催化剂可以改变反应历程 |
| D.保持压强不变,室温下进行该反应,焓变变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中错误的
| A.升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| B.对有气体参加的化学反应,减小容器体积、体系压强增大,从而增大了活化分子的浓度,因而反应速率增大 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.加入正催化剂,可使活化分子的百分数大大增加,从而增大化学反应的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知反应:A2(g)+2B2(g) ⇌2AB2(g) ΔH>0,下列说法正确的是
| A.升高温度正反应速率加快,逆反应速率减慢 |
| B.0.1 mol A2和0.2 mol B2反应达到平衡时生成0.2 mol AB2 |
| C.达平衡后,升高温度,正、逆反应速率均加快,B的转化率不变 |
| D.催化剂可同等程度改变正、逆反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列所示装置或操作能达到实验目的的是
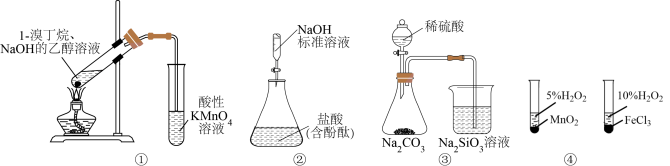

| A.图①:验证1-溴丁烷发生消去反应 |
B.图②: 标准溶液滴定盐酸 标准溶液滴定盐酸 |
| C.图③:比较硫、碳、硅三种元素的非金属性强弱 |
| D.图④:比较不同催化剂对反应速率的影响 |
您最近一年使用:0次

 、
、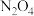 平衡混合气体加压后颜色加深,能用勒夏特列原理解释
平衡混合气体加压后颜色加深,能用勒夏特列原理解释 催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴(
催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴( ,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
 ,共转移4mol
,共转移4mol 
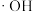 、
、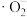 和
和
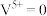 降低该反应的焓变
降低该反应的焓变 的还原性除去
的还原性除去 ,减少了空气污染
,减少了空气污染 有利于
有利于


