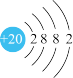
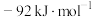下列说法中,正确的是
| A.活化分子间的碰撞一定是有效碰撞 | B.同一原子1s、2s的电子云半径相同 |
| C.原子核外电子发生跃迁属于化学变化 | D.同一原子中没有运动状态完全相同的电子 |
更新时间:2023-01-06 08:58:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③一般说来,活化分子比普通分子具有更高的能量
④化学反应的实质是原子的重新组合
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③一般说来,活化分子比普通分子具有更高的能量
④化学反应的实质是原子的重新组合
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
| A.①③④⑤ | B.②③⑥ | C.③④⑤⑥ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】硼氢化钠(NaBH4)中的氢元素为-1价,具有很强的还原性,被称为“万能还原剂”,NaBH4在催化剂钌(Ru)表面与水反应的历程如图所示:
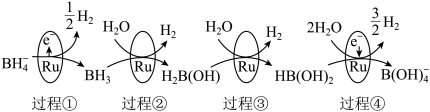
下列说法中错误的是

下列说法中错误的是
| A.过程②反应为BH3+H2O=H2↑+H2B(OH) |
| B.反应过程中硼元素的化合价发生了变化 |
| C.若过程③和过程④均产生lmol H2,则转移电子数目不相等 |
| D.Ru可使上述反应活化分子的百分数提高,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以下能级符号正确的是
| A.4s | B.3f | C.2d | D.1p |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某核素核外共有15个不同运动状态的电子,以下说法正确的是
| A.该元素的最高价氧化物的水化物为强酸 |
| B.原子中有3种能量不同的电子,9种不同的空间运动状态 |
C.若将该原子的电子排布式写成1s22s22p63s23p 3p 3p ,它违背了泡利原理 ,它违背了泡利原理 |
| D.该基态原子中能量最高的电子的电子云的形状为哑铃形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确 的是
| A.乙烯中碳碳双键的键能小于乙烷中碳碳单键键能的2倍 |
| B.共价键一定有原子轨道的重叠 |
| C.两个p轨道不能形成σ键,只能形成π键 |
D.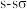 键和 键和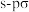 键的电子云图形都是轴对称 键的电子云图形都是轴对称 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
①某价层电子排布为3d54s1的基态原子,该元素位于周期表中第四周期第IB族
②电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
③原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似
④Be与Al在周期表中处于对角线位置,可推出Be(OH)2+2OH-=BeO +2H2O
+2H2O
⑤基态原子的4s轨道上只有1个电子的元素只有K
①某价层电子排布为3d54s1的基态原子,该元素位于周期表中第四周期第IB族
②电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
③原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似
④Be与Al在周期表中处于对角线位置,可推出Be(OH)2+2OH-=BeO
 +2H2O
+2H2O⑤基态原子的4s轨道上只有1个电子的元素只有K
| A.①②③ | B.①③⑤ | C.②⑤ | D.③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】2023年5月神舟十六号载人飞船在酒泉卫星发射中心发射。发射航天器的材料、常用的燃料及助燃剂如表所示。下列有关叙述正确的是
| 航天器材料 | 液体燃料 | 固体燃料 | 助燃剂 |
| 钢、钛合金、石墨纤维等 | 液氢、低级醇类、1,2-二甲基肼 (CH3NHNHCH3) | 硼氢化钠 (NaBH4) | 液氧、五氟化溴(BrF5)、高氯酸铵 (NH4ClO4) |
A.基态Ti原子的简化电子排布式为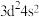 |
B. 的阴离子空间结构为正四面体形 的阴离子空间结构为正四面体形 |
| C.基态N原子核外电子占据的最高能级的电子云轮廓图为球形 |
D.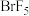 中各原子均满足 中各原子均满足 稳定结构 稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M、N分别为五种原子序数不大于20的元素,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素形成的化合物在自然界中种类最多,M的阳离子通常存在于硝石、明矾和草木灰中,N的原子序数比M大1。下列说法正确的是
| A.熔点:Y4Z晶体低于单质Z |
| B.X与Al的某些化学性质相似,XO是两性氧化物 |
| C.M的阳离子半径是同周期主族元素的简单离子中半径最大的 |
| D.NZ2仅含离子键,可用于制备乙炔 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】“下列化学用语表述错误的是
| A.Mn的核外电子排布式为[Ar]3d54s2 |
B.用电子式表示K2S的形成过程: |
C.NH3分子的VSEPR模型: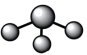 |
D.基态N原子的价层电子排布图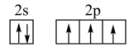 |
您最近一年使用:0次

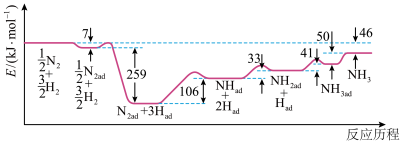
 正反应的活化能高于逆反应的活化能
正反应的活化能高于逆反应的活化能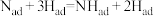
 的反应热为
的反应热为