Li2CO3和C只有在MoS2的催化作用下才能发生2Li2CO3+C-4e-=4Li++3CO2电极反应,反应历程中的能量变化如图。
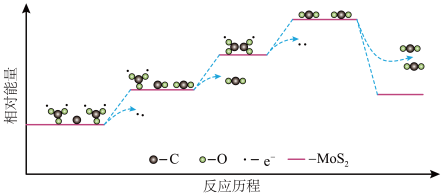
下列说法正确的是

下列说法正确的是
| A.碳原子在电极反应中均发生氧化反应 |
| B.反应历程中存在碳氧键的断裂和形成 |
| C.反应历程中涉及电子转移的变化均释放能量 |
| D.MoS2催化剂通过降低电极反应的焓变使反应速率加快 |
更新时间:2023-01-06 16:00:20
|
相似题推荐
【推荐1】二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的重要反应之一,下列说法正确的是
2SO3(g)是工业制硫酸的重要反应之一,下列说法正确的是
 2SO3(g)是工业制硫酸的重要反应之一,下列说法正确的是
2SO3(g)是工业制硫酸的重要反应之一,下列说法正确的是| A.煅烧硫铁矿(主要成分FeS2)可获得SO2,将矿石粉碎成细小颗粒可以提高反应的转化率 |
| B.已知该催化氧化反应K(300℃)>K(350℃),则该反应正向是吸热反应 |
| C.采用正向催化剂时,反应的活化能降低,使反应明显加快 |
| D.工业生产中,采用的压强越高,温度越低,越有利于提高经济效益 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】使用催化剂能加快反应速率的主要原因是
| A.加快了分子运动的速率 | B.降低了反应物分子的能量 |
| C.减小了活化分子的百分数 | D.降低了反应的活化能 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】为了说明影响化学反应快慢的因素,某同学分别设计了如下A~D四个实验,你认为结论不正确的是( )
| A.将大小、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 |
| B.在相同条件下,等质量的大理石块和大理石粉与相同浓度的盐酸反应,大理石粉反应快 |
| C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 |
| D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】已知反应: ,若其它条件不变,下列措施
,若其它条件不变,下列措施不能 加快该反应速率的是
 ,若其它条件不变,下列措施
,若其它条件不变,下列措施| A.升高温度 | B.加入少量MnO2 |
| C.加入少量FeCl3 | D.加水稀释H2O2溶液 |
您最近一年使用:0次

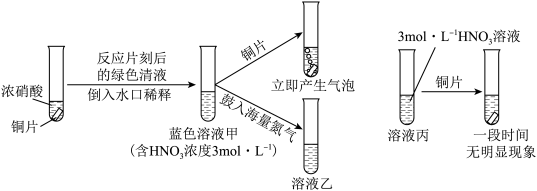
 对该反应没有催化作用
对该反应没有催化作用 ,铜片表面立即产生气泡,说明
,铜片表面立即产生气泡,说明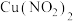 ,铜片上立即生成气泡,说明
,铜片上立即生成气泡,说明 对该反应有催化作用
对该反应有催化作用

