已知反应:①

②

相关化学键的键能数据如下:
下列说法正确的是


②


相关化学键的键能数据如下:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | a | b | c | d |
| A.①中反应物的总能量小于生成物的总能量 |
B. |
C. |
D.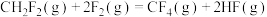 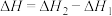 |
22-23高二上·北京东城·期末 查看更多[11]
云南省开远市第一中学校2023-2024学年高二上学期12月月考化学试题北京市2023-2024学年北京三中高二(上)期中化学试卷 北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京市第三中学2023-2024学年高二上学期期中练习化学试题北京市密云区第二中学2023-2024学年高二上学期期中(选考)化学试卷 北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第五十五中学2023-2024学年高二上学期12月月考调研化学试题福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题北京市海淀区2023-2024学年高二上学期期中考试化学试题 北京市第一七一中学2023-2024学年高二上学期10月月考化学试题北京市东城区2022-2023学年高二上学期期末统一检测化学试卷
更新时间:2023-01-05 23:59:43
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】强酸和强碱在稀溶液里反应的热化学方程式可表示为:
H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1
已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) ΔH=-Ql kJ/mol
HNO3(aq)+NaOH(aq) = NaNO3(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
上述均系在溶液中进行的反应,Q1、Q2的关系正确的是
H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1
已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) ΔH=-Ql kJ/mol
HNO3(aq)+NaOH(aq) = NaNO3(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
上述均系在溶液中进行的反应,Q1、Q2的关系正确的是
| A.Ql-Q2=57.3 | B.Q1>Q2>57.3 |
| C.Q1<Q2 = 57.3 | D.无法确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关热化学方程式及其描述正确的是
A.甲烷的燃烧热为890.3 kJ/mol,则甲烷的燃烧热的热化学方程式为:  kJ/mol kJ/mol |
B.500℃,30MPa下,将0.5 mol  和1.5 mol 和1.5 mol  置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为: 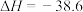 kJ/mol kJ/mol |
C.已知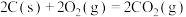  ; ;  ,则 ,则 |
D.含20.0 g NaOH的稀溶液与稀硫酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:  kJ/mol kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:
① CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
② CO2(g) + H2(g) CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法不正确 的是
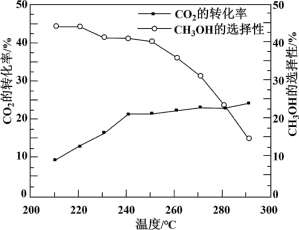
【注】CH3OH的选择性=
① CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol② CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法

【注】CH3OH的选择性=

A.CO(g) + 2H2(g) CH3OH(g) ΔH=- 90.6 kJ/mol CH3OH(g) ΔH=- 90.6 kJ/mol |
| B.使用催化剂,能降低反应的活化能,增大活化分子百分数 |
| C.其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行 |
| D.220~240 ℃,升高温度,对反应②速率的影响比对反应①的小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5⇌NO3+NO2快速平衡
第二步 NO2+NO3→NO+NO2+O2慢反应
第三步 NO+NO3→2NO2快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
第一步 N2O5⇌NO3+NO2快速平衡
第二步 NO2+NO3→NO+NO2+O2慢反应
第三步 NO+NO3→2NO2快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
| A.v(第一步的逆反应) < v(第二步反应) |
| B.反应的中间产物只有NO3 |
| C.第二步中NO2与NO3的碰撞仅部分有效 |
| D.第三步反应活化能较高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用CO2催化加氢制二甲醚,可以实现CO2的再利用,该过程中涉及以下两个反应:
①

②

则反应 的
的 为
为
①


②


则反应
 的
的 为
为A.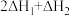 | B.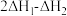 | C.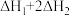 | D.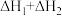 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】利用CO2(g)与H2(g)反应生成CH3OCH3(g)和H2O(g)有利于实现碳中和,其反应过程中的能量变化如图所示。下列有关说法正确的是
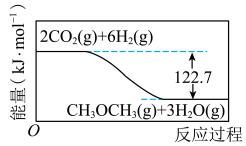

| A.若该反应在绝热密闭容器中进行,则反应过程中体系温度会降低 |
| B.1 molH2(g)在O2(g)中完全燃烧生成H2O(g)时放出的热量大于20.45kJ |
| C.若反应消耗0.4 molCO2(g)和1.2molH2(g),则该反应放出49.08kJ热量 |
| D.CH3OCH3(g)+3H2O(g)=2CO2(g) +6H2(g) ∆H=-122.7 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】H2和I2在一定条件下能发生反应:H2(g)+I2(g) 2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )

 2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
| A.反应物的总能量低于生成物的总能量 |
| B.断开1molH—H键和1molI—I键所需能量大于断开2molH—I键所需能量 |
| C.向密闭容器中加入2molH2和2molI2,充分反应后放出的热量等于2akJ |
| D.断开2molH—I键所需能量为(c+b+a)kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知氟化氢气体中有平衡关系:已知a、b均大于0,①2H3F3(g)  3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)
3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)  2HF(g) ΔH2=+b kJ·mol-1,则可推测反应H3F3(g)=3HF(g)的ΔH为( )
2HF(g) ΔH2=+b kJ·mol-1,则可推测反应H3F3(g)=3HF(g)的ΔH为( )
 3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)
3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)  2HF(g) ΔH2=+b kJ·mol-1,则可推测反应H3F3(g)=3HF(g)的ΔH为( )
2HF(g) ΔH2=+b kJ·mol-1,则可推测反应H3F3(g)=3HF(g)的ΔH为( )| A.+(a+b) kJ·mol-1 |
| B.+(a-b) kJ·mol-1 |
| C.+(0.5a+1.5b) kJ·mol-1 |
| D.+(a+3b) kJ·mol-1 |
您最近一年使用:0次

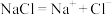


 在水中电离:
在水中电离:
 与
与 反应能量变化:
反应能量变化:



