“84”消毒液是生活中常见的消毒剂,可用 与NaOH溶液在冷水浴中制备。
与NaOH溶液在冷水浴中制备。
I.240.00mL1.00mol/LNaOH溶液的配制:
(1)配制溶液时,一般有以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其正确的操作顺序为_______ 。
A.①②④⑤⑦⑥③ B.②①③⑤⑥⑦④ C.②①⑥③⑤④⑦ D.①②⑥③⑦⑤④
实验中必须用到的玻璃仪器有烧杯、玻璃棒、量筒、_______ 、_______ 。
(2)下列操作使所配NaOH溶液浓度偏低的是_______。
II.“84”消毒液的制备(装置如图所示):

(3)写出圆底烧瓶中发生反应的离子方程式_______ 。
(4)已知C中广口瓶和D中烧杯内均为NaOH溶液,则B中试剂为_______ ,C中发生反应的化学方程式为_______ ,D的作用为_______ 。
 与NaOH溶液在冷水浴中制备。
与NaOH溶液在冷水浴中制备。I.240.00mL1.00mol/LNaOH溶液的配制:
(1)配制溶液时,一般有以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其正确的操作顺序为
A.①②④⑤⑦⑥③ B.②①③⑤⑥⑦④ C.②①⑥③⑤④⑦ D.①②⑥③⑦⑤④
实验中必须用到的玻璃仪器有烧杯、玻璃棒、量筒、
(2)下列操作使所配NaOH溶液浓度偏低的是_______。
| A.在天平两边放相同大小的滤纸后,再进行称量 |
| B.未冷却至室温就将溶液转移到容量瓶中 |
| C.定容时俯视刻度线 |
| D.未洗涤溶解NaOH固体的烧杯 |
II.“84”消毒液的制备(装置如图所示):

(3)写出圆底烧瓶中发生反应的离子方程式
(4)已知C中广口瓶和D中烧杯内均为NaOH溶液,则B中试剂为
更新时间:2023-01-11 09:41:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯化铁在工农业生产中有着广泛的应用,也是中学实验中常见的试剂。某化学兴趣小组根据所学知识,探究干法和湿法条件下制备氯化铁。
查阅资料:FeCl3加热易升华,易溶于水,并且有强烈的吸水性易潮解。
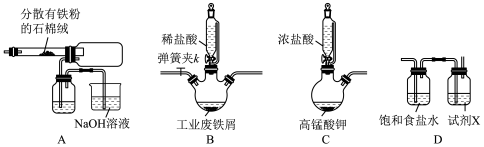
I.干法制取:
(1)按照气体流向从左到右连接仪器的顺序为___________→____________→___________。___________
(2)D装置中饱和食盐水的作用是___________ ,试剂X是___________ 。
(3)C装置的烧瓶中发生反应的离子方程式为___________ 。
(4)A装置中将硬质玻璃管直接插入集气瓶的原因是___________ 。
II.湿法制取:
向B装置加入一定量盐酸后,通入稍过量的氯气,然后将反应后的溶液经过一系列操作后得到FeCl3·6H2O晶体。
(5)通入稍过量氯气的目的是___________ 。
(6)纯度测定:
准确称取干法粗产品m g配成50 mL溶液,向其中滴加稍过量的硝酸银溶液过滤、洗涤、干燥得到固体2.87 g,则得到的产品中氯化铁的质量分数为___________ (计算结果保留小数点后两位,用 m表示),配制的溶液中c(Cl-) =___________ mol·L-1。
查阅资料:FeCl3加热易升华,易溶于水,并且有强烈的吸水性易潮解。

I.干法制取:
(1)按照气体流向从左到右连接仪器的顺序为___________→____________→___________。
(2)D装置中饱和食盐水的作用是
(3)C装置的烧瓶中发生反应的离子方程式为
(4)A装置中将硬质玻璃管直接插入集气瓶的原因是
II.湿法制取:
向B装置加入一定量盐酸后,通入稍过量的氯气,然后将反应后的溶液经过一系列操作后得到FeCl3·6H2O晶体。
(5)通入稍过量氯气的目的是
(6)纯度测定:
准确称取干法粗产品m g配成50 mL溶液,向其中滴加稍过量的硝酸银溶液过滤、洗涤、干燥得到固体2.87 g,则得到的产品中氯化铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】四氯化锡 可用作媒染剂和有机合成的氯化催化剂。实验室可按下图装置(部分夹持装置略去)制备
可用作媒染剂和有机合成的氯化催化剂。实验室可按下图装置(部分夹持装置略去)制备 。
。

已知:① 和
和 的部分物理性质:
的部分物理性质:
② 能与
能与 反应生成
反应生成 ,无水
,无水 遇水易水解生成
遇水易水解生成
③ 与
与 加热条件下生成
加热条件下生成 和
和
回答下列问题:
(1)A装置中带有玻璃管a的装置的名称是_______ ;a的作用是_______ ;B中的试剂:_______ 。E中球形冷凝管的进水口是_______ (填“c”或“d”)。A中发生反应的离子方程式 是_______ 。
(2)当D中充满黄绿色气体时再点燃酒精灯,原因是_______ 。
(3)若无C装置,可观察到E中试管内有白雾产生,试解释产生该现象原因:_______ 。
(4)E中收集的产品因混有氯气而呈黄绿色。欲得到较纯的 ,可再加入几片锡薄片,加热蒸馏,收集温度范围为
,可再加入几片锡薄片,加热蒸馏,收集温度范围为_______ (填标号)的馏分,得到无水 成品。
成品。
A. B.
B.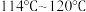 C.
C.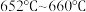
 可用作媒染剂和有机合成的氯化催化剂。实验室可按下图装置(部分夹持装置略去)制备
可用作媒染剂和有机合成的氯化催化剂。实验室可按下图装置(部分夹持装置略去)制备 。
。
已知:①
 和
和 的部分物理性质:
的部分物理性质:| 物质 |  |  |
| 颜色、状态 | 无色晶体 | 无色液体 |
熔点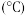 | 246 |  |
沸点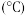 | 652 | 114 |
 能与
能与 反应生成
反应生成 ,无水
,无水 遇水易水解生成
遇水易水解生成
③
 与
与 加热条件下生成
加热条件下生成 和
和
回答下列问题:
(1)A装置中带有玻璃管a的装置的名称是
(2)当D中充满黄绿色气体时再点燃酒精灯,原因是
(3)若无C装置,可观察到E中试管内有白雾产生,试解释产生该现象原因:
(4)E中收集的产品因混有氯气而呈黄绿色。欲得到较纯的
 ,可再加入几片锡薄片,加热蒸馏,收集温度范围为
,可再加入几片锡薄片,加热蒸馏,收集温度范围为 成品。
成品。A.
 B.
B.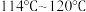 C.
C.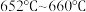
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学设计如图装置(省略夹持装置)制备氯气并探究其性质,请回答下列问题。

(1)盛装浓盐酸的仪器名称为___________ ,试管内发生反应的化学方程式为___________ 。
(2)湿润的蓝色石蕊试纸先变红后褪色,请结合化学方程式和文字解释该现象产生的原因:___________ 。
(3)浸有溴化钠溶液的试纸变橙黄色,反应的离子方程式为___________ 。
(4)一段时间之后,湿润的淀粉碘化钾试纸会变蓝(I2遇淀粉会变蓝),___________ (填“能”或“不能”)说明Br2的氧化性比I2强;烧杯中的溶液可以为___________ (填标号),倒置漏斗的作用是___________ 。
A.饱和食盐水 B.饱和NaOH溶液
C.澄清石灰水 D.浓盐酸

(1)盛装浓盐酸的仪器名称为
(2)湿润的蓝色石蕊试纸先变红后褪色,请结合化学方程式和文字解释该现象产生的原因:
(3)浸有溴化钠溶液的试纸变橙黄色,反应的离子方程式为
(4)一段时间之后,湿润的淀粉碘化钾试纸会变蓝(I2遇淀粉会变蓝),
A.饱和食盐水 B.饱和NaOH溶液
C.澄清石灰水 D.浓盐酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
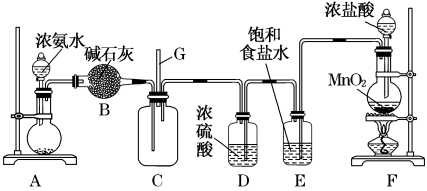
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用______(填序号)。
(2)装置B的作用是____ ;装置E的作用是____ 。
(3)通入装置C的两根导管左边较长、右边较短,目的是__________ 。
(4)装置F中发生反应的化学方程式是_______ 。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:_______ 。
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?___ 。

请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用______(填序号)。
| A.生石灰 | B.碱石灰 | C.五氧化二磷 | D.烧碱 |
(3)通入装置C的两根导管左边较长、右边较短,目的是
(4)装置F中发生反应的化学方程式是
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯气、“84”消毒液、源白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
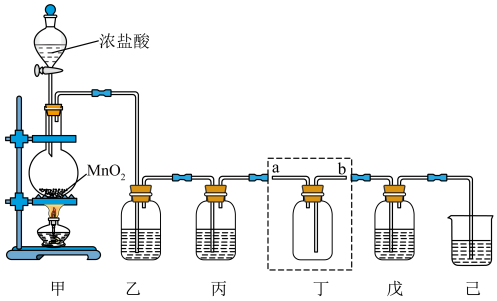
(1)装置甲中发生反应的化学方程式为_______ ,盛装浓盐酸的仪器的名称为________ 。
(2)实验开始前应进行的操作是___________ 。
(3)装置丁用来收集纯净且干燥的氯气,进气口为___________ (填a或b);装置乙盛装的试剂是___________ ,其作用是___________ ;丙盛装的试剂是___________ ,其作用是___________ 。(试剂填名称)
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为___________ ;漂白粉长时间暴露在空气中容易发生变质的原因为___________ (结合化学方程式说明)。
(5)实验室中,除上述制取氯气的方法以外,还可利用以下反应: 。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
①写出该反应的离子方程式:___________ 。
②该反应中,氧化剂是___________ ,被氧化的物质是___________ 。

(1)装置甲中发生反应的化学方程式为
(2)实验开始前应进行的操作是
(3)装置丁用来收集纯净且干燥的氯气,进气口为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
(5)实验室中,除上述制取氯气的方法以外,还可利用以下反应:
 。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。①写出该反应的离子方程式:
②该反应中,氧化剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有关物质的转化关系如图所示。C为常见的调味品,D是常见的无色液体。E、F、H和J均为气体,其中H和J为单质,且两者在一定条件下可生成E。
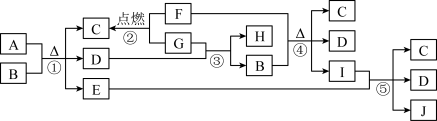
(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有__ 性。
(2)写出反应①的化学方程式:_____ 。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目 :___ 。
(4)写出反应④的离子方程式:____ 。
(5)写出反应⑤的化学方程式:____ 。

(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有
(2)写出反应①的化学方程式:
(3)写出反应③的化学方程式,
(4)写出反应④的离子方程式:
(5)写出反应⑤的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学实验小组欲配制245mL 0.1mol/L硫酸亚铁溶液,实验室有如下两种试剂:①FeSO4·7H2O,②5mol/LFeSO4溶液,现分两小组分别进行实验,第一小组选择试剂①,第二小组选择试剂②。
(1)第一小组称量试剂①的质量为__________ g。
(2)第二小组经计算需要______ mL5mol/LFeSO4溶液,在量取试剂②后,进行了下列操作:
a.等稀释的溶液的温度与室温一致后,沿玻璃棒注入容量瓶中。
b.________ 使溶液的液面与瓶颈的刻度标线相切。
c.在盛FeSO4溶液的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
d.用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________ 。若量取的是浓硫酸,简述第c步实验的具体操作步骤:________
(3)在上述配制过程中,若出现以下情况,对溶液浓度有何影响?
A 用量筒量取试剂②时仰视观察凹液面。
B 稀释的FeSO4溶液未恢复至室温,沿玻璃棒注入容量瓶中。
C 未用蒸馏水洗涤烧杯和玻璃棒。
D 定容时,仰视观察凹液面。
E 定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线。
F 配制溶液时,容量瓶中有蒸馏水。
偏高:______________ 偏低:____________ 无影响:_____________
(1)第一小组称量试剂①的质量为
(2)第二小组经计算需要
a.等稀释的溶液的温度与室温一致后,沿玻璃棒注入容量瓶中。
b.
c.在盛FeSO4溶液的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
d.用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)
(3)在上述配制过程中,若出现以下情况,对溶液浓度有何影响?
A 用量筒量取试剂②时仰视观察凹液面。
B 稀释的FeSO4溶液未恢复至室温,沿玻璃棒注入容量瓶中。
C 未用蒸馏水洗涤烧杯和玻璃棒。
D 定容时,仰视观察凹液面。
E 定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线。
F 配制溶液时,容量瓶中有蒸馏水。
偏高:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图表示配制100mL 0.10mol·L-1 CuSO4溶液的几个关键实验步骤和操作,据图回答下列问题:

(1)将上述实验步骤A-F按实验过程先后次序排列______________________________ 。
若用CuSO4•5H2O晶体来配制480mL 0.20mol·L-1的溶液需称取CuSO4•5H2O 晶体的质量为_____ g。若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏___________ (填“高”或“低”)。
(2)写出配制480mL0.20mol·L-1CuSO4溶液所需要用到的玻璃仪器的名称:烧杯、量筒、_______________ 。
(3)步骤B通常称为转移,若是配制NaOH溶液,用水溶解NaOH固体后未冷却至室温即转移,配制溶液的浓度将偏______ (填“高”或“低”)。步骤A通常称为____________ ,如果俯视刻度线,配制的浓度将偏______ (填“高”或“低”)。步骤D称为_______ 。若没有步骤D,则配制的浓度偏______ (填“高”或“低”)。

(1)将上述实验步骤A-F按实验过程先后次序排列
若用CuSO4•5H2O晶体来配制480mL 0.20mol·L-1的溶液需称取CuSO4•5H2O 晶体的质量为
(2)写出配制480mL0.20mol·L-1CuSO4溶液所需要用到的玻璃仪器的名称:烧杯、量筒、
(3)步骤B通常称为转移,若是配制NaOH溶液,用水溶解NaOH固体后未冷却至室温即转移,配制溶液的浓度将偏
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三位同学分别进行“Na2CO3和NaCl混合物中Na2CO3质量分数测定”的实验:
(1)甲同学实验的主要步骤有:①过滤②加入足量的CaCl2溶液③将沉淀小心烘干、称量,测得固体质量为ng④称取mg样品溶于适量蒸馏水⑤洗涤沉淀2-3次。该同学正确的操作步骤为_______ (填序号);混合物中碳酸钠的质量分数为_______ (只需列出计算式)。
(2)乙同学把一定量的混合物与足量盐酸反应,然后用如图所示装置测定产生的气体体积。实验室中只有如下试剂:样品、6mol/L盐酸、Na2CO3溶液、CaCl2溶液、饱和NaHCO3溶液。

回答下列问题:
①广口瓶中盛放的溶液是_______ 。
②该装置测定的气体体积往往不准确(不考虑导管中水的体积),理由是_______ 。
(3)丙同学准确称取wg固体混合物放入锥形瓶中,加入V1mL。0.1000mol/L盐酸,充分反应,用0.1000mol/L的氢氧化钠溶液滴定过量盐酸,消耗氢氧化钠溶液V2mL。请回答下列问题:
①实验室现有1.000mol/L的盐酸。为了精确配制100mL0.1000mol/L的盐酸,需要的仪器有:烧杯、100mL容量瓶、玻璃棒、_______ 。
②滴定时选择。_______ 作指示剂,滴定终点溶液的颜色变化为_______ 。
③混合物中碳酸钠的质量分数为_______ (只需列出计算式)。
(1)甲同学实验的主要步骤有:①过滤②加入足量的CaCl2溶液③将沉淀小心烘干、称量,测得固体质量为ng④称取mg样品溶于适量蒸馏水⑤洗涤沉淀2-3次。该同学正确的操作步骤为
(2)乙同学把一定量的混合物与足量盐酸反应,然后用如图所示装置测定产生的气体体积。实验室中只有如下试剂:样品、6mol/L盐酸、Na2CO3溶液、CaCl2溶液、饱和NaHCO3溶液。

回答下列问题:
①广口瓶中盛放的溶液是
②该装置测定的气体体积往往不准确(不考虑导管中水的体积),理由是
(3)丙同学准确称取wg固体混合物放入锥形瓶中,加入V1mL。0.1000mol/L盐酸,充分反应,用0.1000mol/L的氢氧化钠溶液滴定过量盐酸,消耗氢氧化钠溶液V2mL。请回答下列问题:
①实验室现有1.000mol/L的盐酸。为了精确配制100mL0.1000mol/L的盐酸,需要的仪器有:烧杯、100mL容量瓶、玻璃棒、
②滴定时选择。
③混合物中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图表示配制100mL0.100molL﹣1Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:
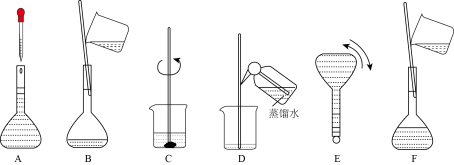
(1)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是_____ 。
①干燥的 ②瓶塞不漏水的 ③用欲配制的溶液润洗过的 ④以上三项均须要求的
(2)若用Na2CO3•10H2O来配制溶液,需要称量晶体_____ 克。若所称取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏_____ 。(填“大/小”)
(3)写出配制溶液中所需要用到的玻璃仪器的名称:烧杯、_____ 。
(4)步骤B通常称为转移,步骤A通常称为_____ 。步骤D称为_____ ,若没有步骤D,则配制的浓度偏_____ 。(填“大/小”)。
(5)将上述实验步骤A﹣F按实验过程先后次序排列_____ 。

(1)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
①干燥的 ②瓶塞不漏水的 ③用欲配制的溶液润洗过的 ④以上三项均须要求的
(2)若用Na2CO3•10H2O来配制溶液,需要称量晶体
(3)写出配制溶液中所需要用到的玻璃仪器的名称:烧杯、
(4)步骤B通常称为转移,步骤A通常称为
(5)将上述实验步骤A﹣F按实验过程先后次序排列
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】基础实验:配制一定物质的量浓度的溶液,物质的量浓度是一种常用的溶液浓度表示方法,利用其进行定量分析计算比较方便。
(1)某实验需要 溶液900mL,则实际应该配制
溶液900mL,则实际应该配制_______ mL,则应该用干燥的烧杯称量_______ 克NaOH固体。
(2)配制的正确顺序为①④③_______ (补充完整,填序号)。
(3)定容时应用_______ (写仪器名称)加水至液体凹液面最低处与刻度线相切。
(4)转移完烧杯中的溶液未洗涤烧杯和玻璃棒则溶液的浓度_______ (填“偏高”、“偏低”“不变”下同),定容时俯视刻度线则结果_______ 。

(1)某实验需要
 溶液900mL,则实际应该配制
溶液900mL,则实际应该配制(2)配制的正确顺序为①④③
(3)定容时应用
(4)转移完烧杯中的溶液未洗涤烧杯和玻璃棒则溶液的浓度

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室用KMnO4固体配制1000mL0.1 mol·L-1KMnO4溶液。
(1)计算并称量KMnO4固体的质量为_______ g。
(2)下图为甲同学的部分实验操作,其中规范的是_______。
(3)该实验中可做为反应容器的仪器名称是_______ 。
(4)下列情况对所配制的KMnO4溶液度没有影响的是_______。
(5)乙同学用所配制的KMnO4溶液测定人体血液中Ca2+的浓度,步骤如下
a.取1.0mL上述配制的KMnO4溶液稀释为10.0mL;
b.抽取血样10.0mL,使其中的Ca2+ 完全转变为草酸钙(CaC2O4)沉淀,过滤、洗涤后用稀硫酸溶解沉淀得到草酸(H2C2O4)溶液;
c.将稀释后的KMnO4溶液滴加到草酸溶液中,反应恰好消耗2.0mLKMnO4溶液。
已知,KMnO4溶液与草酸的反应为:2KMnO4+5H2C2O4+3H2SO4=2MnSO3+K2SO4+10CO2↑+8H2O
①KMnO4与H2C2O4反应中的氧化剂是_______ 。
②该血样中的Ca2+ 浓度为_______ mol·L-1。
(1)计算并称量KMnO4固体的质量为
(2)下图为甲同学的部分实验操作,其中规范的是_______。
A.称量 | B.转移溶液 | C.溶解 | D.定容 |
(4)下列情况对所配制的KMnO4溶液度没有影响的是_______。
| A.将溶解后的溶液转移至容量瓶之前,容量瓶未干燥 |
| B.将溶解后的溶液转移至容量瓶之后,未洗涤烧杯和玻璃棒 |
| C.定容时,俯视刻度线 |
| D.定容时,发现液面超过刻度线,用吸管将多余的溶液吸出 |
a.取1.0mL上述配制的KMnO4溶液稀释为10.0mL;
b.抽取血样10.0mL,使其中的Ca2+ 完全转变为草酸钙(CaC2O4)沉淀,过滤、洗涤后用稀硫酸溶解沉淀得到草酸(H2C2O4)溶液;
c.将稀释后的KMnO4溶液滴加到草酸溶液中,反应恰好消耗2.0mLKMnO4溶液。
已知,KMnO4溶液与草酸的反应为:2KMnO4+5H2C2O4+3H2SO4=2MnSO3+K2SO4+10CO2↑+8H2O
①KMnO4与H2C2O4反应中的氧化剂是
②该血样中的Ca2+ 浓度为
您最近一年使用:0次



