近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:3C+2K2Cr2O7+8H2SO4(稀)=3CO2↑+3K2SO4+2Cr2(SO4)3+8H2O。请回答下列问题。
(1)下列物质中:①碳纳米颗粒②K2Cr2O7晶体③CO2④熔融K2SO4⑤Cr2(SO4)3溶液⑥H2O⑦稀硫酸。属于电解质是______ (填序号)。
(2)CO2的摩尔质量为______ 。
(3)用单线桥法标出上述反应电子转移的方向和数目_____ 。
(4)标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,则该混合气体的平均相对分子质量是______ 。
(5)实验探究小组在实验中需要用到456mL1mol•L-1的H2SO4溶液,但是在实验室中只发现一瓶8mol•L-1的H2SO4溶液,该小组用8mol•L-1的H2SO4溶液配制所需溶液。
①如图所示的仪器中配制溶液肯定不需要的是______ (填序号),配制上述溶液还需用到的玻璃仪器是______ (填仪器名称)。
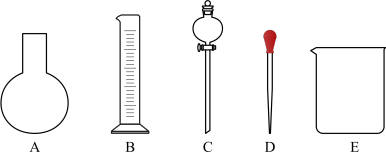
②该实验中需要量取8mol•L-1的H2SO4溶液______ mL。
(1)下列物质中:①碳纳米颗粒②K2Cr2O7晶体③CO2④熔融K2SO4⑤Cr2(SO4)3溶液⑥H2O⑦稀硫酸。属于电解质是
(2)CO2的摩尔质量为
(3)用单线桥法标出上述反应电子转移的方向和数目
(4)标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,则该混合气体的平均相对分子质量是
(5)实验探究小组在实验中需要用到456mL1mol•L-1的H2SO4溶液,但是在实验室中只发现一瓶8mol•L-1的H2SO4溶液,该小组用8mol•L-1的H2SO4溶液配制所需溶液。
①如图所示的仪器中配制溶液肯定不需要的是

②该实验中需要量取8mol•L-1的H2SO4溶液
更新时间:2023-01-12 19:05:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】一氧化二氯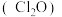 为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
实验室制备原理: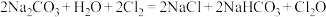 。现用如图所示装置设计实验制备少量
。现用如图所示装置设计实验制备少量 。
。

(1)仪器组装完成、加药品前应进行的实验操作为_________ 。
(2)装置A中发生反应的化学方程式为_________ ,其中参加反应的HCl中表现酸性和还原性的物质的量之比为_________ 。
(3)装置B中盛放的试剂是_________ 溶液。
(4)E装置中冰水混合物的作用_________ 。
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有Cl-_________ 。
(6)A中加入8.7克MnO2,当加入75ml10mol/L的浓盐酸时溶液澄清,理论上能得到Cl2O体积_________ L(折算成标准状况)
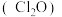 为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:| 物理性质 | 化学性质 |
常温下, 是棕黄色有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ 是棕黄色有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ |  热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 |
 。现用如图所示装置设计实验制备少量
。现用如图所示装置设计实验制备少量 。
。
(1)仪器组装完成、加药品前应进行的实验操作为
(2)装置A中发生反应的化学方程式为
(3)装置B中盛放的试剂是
(4)E装置中冰水混合物的作用
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有Cl-
(6)A中加入8.7克MnO2,当加入75ml10mol/L的浓盐酸时溶液澄清,理论上能得到Cl2O体积
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝箔可以有效减少热辐射,因此常用于食品的保温。铝土矿(主要成分为 ,还含有
,还含有 、
、 )是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
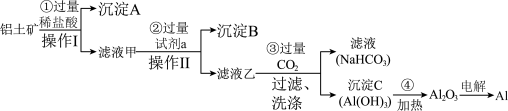
(1)步骤②中试剂a为___________ 。
(2)步骤③中通入过量 ,产生沉淀C的离子反应方程式为
,产生沉淀C的离子反应方程式为___________ 。
(3)在生活中常利用铝热反应来进行焊接钢轨。除了 ,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
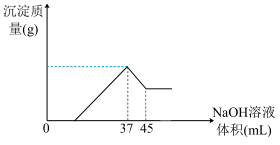
(4)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后向滤液中加入 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的百分含量为
的百分含量为___________ 。
 ,还含有
,还含有 、
、 )是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
(1)步骤②中试剂a为
(2)步骤③中通入过量
 ,产生沉淀C的离子反应方程式为
,产生沉淀C的离子反应方程式为(3)在生活中常利用铝热反应来进行焊接钢轨。除了
 ,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。| A.MgO | B. | C. | D. |
(4)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后向滤液中加入
 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的百分含量为
的百分含量为
您最近一年使用:0次
【推荐3】每年在炼钢、石油精炼等工业生产的脱硫过程中钒会转化成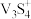 沉积在五氧化二钒(V2O5)催化剂上,另水分、酸雾、沙尘及砷对催化剂都有毒害作用,致使催化剂失去活性,产生大量的废钒催化剂。一种以该废矾催化剂为原料的湿法回收钒的工艺流程如图:
沉积在五氧化二钒(V2O5)催化剂上,另水分、酸雾、沙尘及砷对催化剂都有毒害作用,致使催化剂失去活性,产生大量的废钒催化剂。一种以该废矾催化剂为原料的湿法回收钒的工艺流程如图:
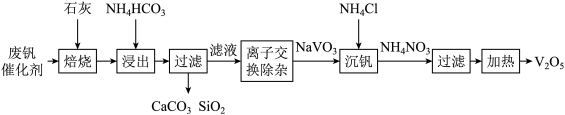
已知:V2O5是两性氧化物,以酸性为主,易溶于强碱或弱碱性介质溶液中,V2O5与碱反应生成 ,与强酸反应生成
,与强酸反应生成 。
。
回答下列问题:
(1)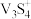 中钒的化合价为
中钒的化合价为_________ 价,“焙烧”时加石灰的目的是_________ 。
(2)写出V2O5与烧碱溶液反应的化学方程式:_________ ;“浸出”时不用烧碱而改用弱碱性的NH4HCO3溶液的原因是_________ 。
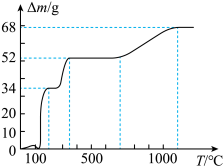
(3)溶液中有过量NH4Cl存在时,NH4VO3的溶解度会急剧下降,“沉钒”时发生反应的化学方程式为_________ 。
(4)“加热”时,NH4VO3固体减少的质量(Δm)随温度的变化曲线如图所示。加热到200℃时,得到的固体物质的化学式为_________ ,300~360℃放出的气态物质的化学式为_________ 。
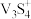 沉积在五氧化二钒(V2O5)催化剂上,另水分、酸雾、沙尘及砷对催化剂都有毒害作用,致使催化剂失去活性,产生大量的废钒催化剂。一种以该废矾催化剂为原料的湿法回收钒的工艺流程如图:
沉积在五氧化二钒(V2O5)催化剂上,另水分、酸雾、沙尘及砷对催化剂都有毒害作用,致使催化剂失去活性,产生大量的废钒催化剂。一种以该废矾催化剂为原料的湿法回收钒的工艺流程如图:
已知:V2O5是两性氧化物,以酸性为主,易溶于强碱或弱碱性介质溶液中,V2O5与碱反应生成
 ,与强酸反应生成
,与强酸反应生成 。
。回答下列问题:
(1)
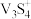 中钒的化合价为
中钒的化合价为(2)写出V2O5与烧碱溶液反应的化学方程式:
(3)溶液中有过量NH4Cl存在时,NH4VO3的溶解度会急剧下降,“沉钒”时发生反应的化学方程式为
(4)“加热”时,NH4VO3固体减少的质量(Δm)随温度的变化曲线如图所示。加热到200℃时,得到的固体物质的化学式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)下列物质中,属于电解质的是____ ,属于强电解质的是____ ,属于弱电解质的是____ (填序号)。
①H2SO4②盐酸 ③硫酸钡 ④乙醇 ⑤铜 ⑥H2S ⑦蔗糖 ⑧氨气 ⑨NH4HSO3
(2)甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,相关反应的热化学方程式及平衡常数如下所示:
i.CO(g)+2H2(g) CH3OH(g) △H=akJ•mol-1 K1
CH3OH(g) △H=akJ•mol-1 K1
ii.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=bkJ•mol-1 K2
CH3OH(g)+H2O(g) △H=bkJ•mol-1 K2
iii.CO2(g)+H2(g) CO(g)+H2O(g) △H=ckJ•mol-1 K3
CO(g)+H2O(g) △H=ckJ•mol-1 K3
回答下列问题:
①a=_____ (用b、c表示),则K1=____ (用K2、K3表示)。
②在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2和H2,在催化剂的作用下仅发生反应iii。下列叙述能表示该反应达到平衡状态的是____ (填标号)。
a.容器中混合气体的压强不再改变
b.容器中CO、CO2的物质的量相等
c.容器中气体的密度不再改变
d.相同时间内,断裂H-O的数目是断裂H-H的2倍
(3)在密闭容器中充入一定量的CO和NO气体,发生反应2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH<0,如图为平衡时NO的体积分数与温度、压强的关系:
2CO2(g)+N2(g) ΔH<0,如图为平衡时NO的体积分数与温度、压强的关系:
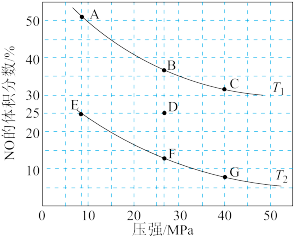
①温度:T1____ T2(填“>”、“<”或“=”)。
②若在D点对应容器升温,同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的___ 点(填字母)。
(1)下列物质中,属于电解质的是
①H2SO4②盐酸 ③硫酸钡 ④乙醇 ⑤铜 ⑥H2S ⑦蔗糖 ⑧氨气 ⑨NH4HSO3
(2)甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,相关反应的热化学方程式及平衡常数如下所示:
i.CO(g)+2H2(g)
 CH3OH(g) △H=akJ•mol-1 K1
CH3OH(g) △H=akJ•mol-1 K1ii.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=bkJ•mol-1 K2
CH3OH(g)+H2O(g) △H=bkJ•mol-1 K2iii.CO2(g)+H2(g)
 CO(g)+H2O(g) △H=ckJ•mol-1 K3
CO(g)+H2O(g) △H=ckJ•mol-1 K3回答下列问题:
①a=
②在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2和H2,在催化剂的作用下仅发生反应iii。下列叙述能表示该反应达到平衡状态的是
a.容器中混合气体的压强不再改变
b.容器中CO、CO2的物质的量相等
c.容器中气体的密度不再改变
d.相同时间内,断裂H-O的数目是断裂H-H的2倍
(3)在密闭容器中充入一定量的CO和NO气体,发生反应2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH<0,如图为平衡时NO的体积分数与温度、压强的关系:
2CO2(g)+N2(g) ΔH<0,如图为平衡时NO的体积分数与温度、压强的关系:
①温度:T1
②若在D点对应容器升温,同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】已知下列十种物质:①液态HCl ;②FeCl3溶液; ③盐酸 ;④NH4Cl晶体 ;⑤蔗糖溶液; ⑥铜; ⑦碳酸钙; ⑧淀粉溶液 ;⑨熔融NaOH; ⑩CO2.根据上述提供的物质,回答下列问题:
(1)能够导电的是_______ ,属于强电解质的是_______ ,属于非电解质的是_______ 。(填序号)
(2)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1_______ (填“增大”、“减小”或“不变”,下同),ΔH_______ 。请写出NO2和CO反应的热化学方程式:_______ 。

(3)观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:_______ ;图b:_______ 。

(4)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式_______ 。
(1)能够导电的是
(2)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1

(3)观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:

(4)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~I为中学化学常见的物质。A可帮助消化,故又称为胃酸;C、H为常见金属单质,C是目前世界上产量最高的金属,H可用作导线;E的组成元素与F相同;I是由地壳中含量最高的元素所形成的气体单质。根据如图所示(图中部分反应条件已略去)的转化关系,回答下列问题:
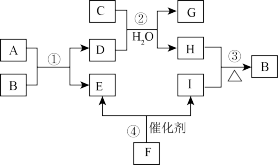
(1)物质B的化学式为___________ ,物质I的用途有___________ (任写一种)。
(2)A~D中属于电解质的是___________ (填化学式);反应①~③中属于离子反应的是___________ (填序号)。
(3)在溶液中发生反应②时的实验现象为___________ ;反应④的化学方程式为___________ 。
(4)发生反应①时,若消耗物质B的质量为120g,则生成物质E的质量为___________ 。

(1)物质B的化学式为
(2)A~D中属于电解质的是
(3)在溶液中发生反应②时的实验现象为
(4)发生反应①时,若消耗物质B的质量为120g,则生成物质E的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学习小组的同学用 和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:
和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:
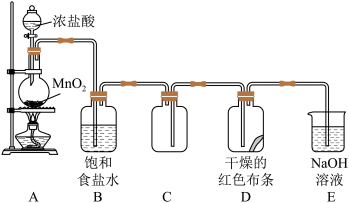
(1)A装置中反应的化学方程式:_______ ;B装置的作用是_______ ;D装置中现象_______ ;该套装置存在的缺陷:_______ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______ (用离子方程式表示)。
(3)若将 通入热的烧碱溶液中,可以发生如下两个反应:
通入热的烧碱溶液中,可以发生如下两个反应: 和
和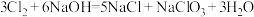 。从氧化还原角度分析
。从氧化还原角度分析 表现了
表现了_______ 。当混合液中 和
和 的个数比为15∶2时,混合液中
的个数比为15∶2时,混合液中 和
和 的个数比为
的个数比为_______ 。
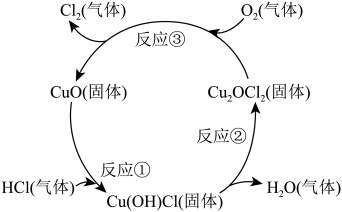
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是_______ ,CuO的作用是_______ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况_______ 。
 和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:
和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:
(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将
 通入热的烧碱溶液中,可以发生如下两个反应:
通入热的烧碱溶液中,可以发生如下两个反应: 和
和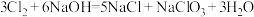 。从氧化还原角度分析
。从氧化还原角度分析 表现了
表现了 和
和 的个数比为15∶2时,混合液中
的个数比为15∶2时,混合液中 和
和 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
【推荐2】2019年4月,陨石坠落哥斯达黎加,再次引发了人们对“天外来客”的关注,下图中(部分产物已略去),X、Y、Z为单质,其它为化合物;E为陨石的主要成分,也是石英砂的主要成分;A为黑色磁性氧化物,请回答下列问题:

(1)写出E与焦炭在高温下反应制取Z的化学方程式,并用单线桥分析 标明电子转移数目_____ .
(2)写出E与 NaOH溶液反应的离子方程式______
(3)A与足量B的稀溶液反应生成D溶液,请用文字表述检验D中金属阳离子存在的一种实验方法:______
(4)已知在外加直流电作用下,G胶粒会向阳极区移动,这种现象叫做____ ;净化G胶体可采用图___ (填序号)的方法,此种方法叫_____ 。


(1)写出E与焦炭在高温下反应制取Z的化学方程式,并用
(2)写出E与 NaOH溶液反应的离子方程式
(3)A与足量B的稀溶液反应生成D溶液,请用文字表述检验D中金属阳离子存在的一种实验方法:
(4)已知在外加直流电作用下,G胶粒会向阳极区移动,这种现象叫做

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】请分析下列氧化还原反应,该反应为实验室用MnO2和浓盐酸(注意不是稀盐酸)反应制备Cl2
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①用单线桥法表示出电子转移方向和数量___________ 。
②该反应的氧化剂是___________ 。
③HCl在该反应中体现的化学性质有___________ 、___________ 。
④实验测定,当MnO2足量时,无论如何控制条件,用含146gHCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的一个原因是HCl易挥发,另一个原因可能是___________
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O①用单线桥法表示出电子转移方向和数量
②该反应的氧化剂是
③HCl在该反应中体现的化学性质有
④实验测定,当MnO2足量时,无论如何控制条件,用含146gHCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的一个原因是HCl易挥发,另一个原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】(1)写出下图中序号①~④仪器的名称:
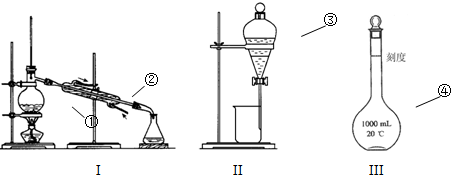
①______ ;② ______ ; ③______ ;④______ ;(填仪器序号)
(2)上述①~④四种仪器中,使用前必须检漏的是_____ 。(填仪器序号)
(3)分离碘水中的碘应先选择装置______ (填装置序号)进行 ______ 和______ 操作 ,再用装置______ (填装置序号)进行______ 操作。
(4)现欲用98%的浓硫酸(密度为1.84g/cm3)配制成浓度为0.5 mol/L的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需______ 、 ______ 、 ______ 。
②所取浓硫酸的体积为______ mL。
③下列操作引起所配溶液浓度偏高的是______
A.取浓硫酸时俯视
B.将浓硫酸倒出后,洗涤装置,并将洗涤液倒入烧杯中
C.在烧杯中稀释浓硫酸后,立即转移
D定容时俯视
E颠倒摇匀后发现液面低于刻度线,但未加水至刻度线

①
(2)上述①~④四种仪器中,使用前必须检漏的是
(3)分离碘水中的碘应先选择装置
(4)现欲用98%的浓硫酸(密度为1.84g/cm3)配制成浓度为0.5 mol/L的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需
②所取浓硫酸的体积为
③下列操作引起所配溶液浓度偏高的是
A.取浓硫酸时俯视
B.将浓硫酸倒出后,洗涤装置,并将洗涤液倒入烧杯中
C.在烧杯中稀释浓硫酸后,立即转移
D定容时俯视
E颠倒摇匀后发现液面低于刻度线,但未加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室配制 500mL 0.2mol/L 的 NaOH溶液,在下图所示仪器中,配制上述溶液肯定不需要的是____ (填序号),除图中已有仪器外, 配制上述溶液还需要的玻璃仪器是____ 。

具体过程如下:
①计算需要称量 NaOH 固体的质量_____ ;
②用少量蒸馏水洗涤烧杯内壁 2~3 次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
③用托盘天平称量 NaOH 固体;
④将 NaOH 溶液沿玻璃棒注入_____ 中;
⑤将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解,并____________ ;
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将蒸馏水注入容量瓶,液面离刻度线下_____ cm 时,改用_______ 滴加蒸馏水至液面于刻度线相切;
试回答下列问题:
(1)填写上述过程中的空白;
(2)上述过程的正确顺序为___________ (填步骤序号);
(3)使用容量瓶前必须进行的一步操作是____________ ;
(4)经精确测量,最后所得溶液物质的量浓度为 0.192mol/L,原因可能是____________ 。
A、使用滤纸称量 NaOH 固体;
B、未冷却直接转移至容量瓶,立即配好;
C、容量瓶中原来有少量蒸馏水;
D、称量时所用的砝码生锈;
E、溶解 NaOH 后的烧杯未经多次洗涤;
F、定容时俯视刻度。

具体过程如下:
①计算需要称量 NaOH 固体的质量
②用少量蒸馏水洗涤烧杯内壁 2~3 次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
③用托盘天平称量 NaOH 固体;
④将 NaOH 溶液沿玻璃棒注入
⑤将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解,并
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将蒸馏水注入容量瓶,液面离刻度线下
试回答下列问题:
(1)填写上述过程中的空白;
(2)上述过程的正确顺序为
(3)使用容量瓶前必须进行的一步操作是
(4)经精确测量,最后所得溶液物质的量浓度为 0.192mol/L,原因可能是
A、使用滤纸称量 NaOH 固体;
B、未冷却直接转移至容量瓶,立即配好;
C、容量瓶中原来有少量蒸馏水;
D、称量时所用的砝码生锈;
E、溶解 NaOH 后的烧杯未经多次洗涤;
F、定容时俯视刻度。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】I.实验室用密度为1.84g·cm-3,溶质的质量分数为98%的浓硫酸,稀释制250mL物质的量浓度为0.46mol·L-1的硫酸。
(1)98%的浓硫酸的物质的量浓度为___________
(2)现有下列几种规格的仪器,应选用___________ (用序号填空)
①10mL量筒 ②50 mL量筒 ③100mL量筒 ④100mL容量瓶 ⑤250mL容量瓶
II.实验室用氢氧化钠固体配制1.00 mol·L-1 NaOH溶液500 mL,回答下列问题:
(3)关于容量瓶的使用,下列操作正确的是___________ (填字母)。
a.使用前要检验容量瓶是否漏液
b.用蒸馏水洗涤后必须要将容量瓶烘干
c.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
d.为了使所配溶液浓度均匀,定容结束后,要摇匀
e.用500 mL的容量瓶可以直接配制480 mL溶液
f.转移溶液时玻璃棒下端位于刻度线上
(4)请补充完整实验的简要步骤:
①计算;②称量NaOH固体___________ g;③溶解;④冷却并移液;⑤洗涤并转移;⑥___________ ;⑦摇匀。
(5)本实验用到的基本仪器已有烧杯、托盘天平(带砝码)、镊子、量筒、玻璃棒,还缺少的仪器是___________ 、___________ 。
(6)上述实验操作②③都要用到小烧杯,其作用分别是___________ 和___________ 。
(7)过程中,其他操作都是正确的情况下,下列操作会引起浓度偏大的是___________(填字母)。
(1)98%的浓硫酸的物质的量浓度为
(2)现有下列几种规格的仪器,应选用
①10mL量筒 ②50 mL量筒 ③100mL量筒 ④100mL容量瓶 ⑤250mL容量瓶
II.实验室用氢氧化钠固体配制1.00 mol·L-1 NaOH溶液500 mL,回答下列问题:
(3)关于容量瓶的使用,下列操作正确的是
a.使用前要检验容量瓶是否漏液
b.用蒸馏水洗涤后必须要将容量瓶烘干
c.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
d.为了使所配溶液浓度均匀,定容结束后,要摇匀
e.用500 mL的容量瓶可以直接配制480 mL溶液
f.转移溶液时玻璃棒下端位于刻度线上
(4)请补充完整实验的简要步骤:
①计算;②称量NaOH固体
(5)本实验用到的基本仪器已有烧杯、托盘天平(带砝码)、镊子、量筒、玻璃棒,还缺少的仪器是
(6)上述实验操作②③都要用到小烧杯,其作用分别是
(7)过程中,其他操作都是正确的情况下,下列操作会引起浓度偏大的是___________(填字母)。
| A.转移溶液时不慎有少量液体洒到容量瓶外面 |
| B.定容时俯视刻度线 |
| C.未冷却到室温就将溶液转移到容量瓶并定容 |
| D.定容后塞上瓶塞反复颠倒摇匀,静置后,发现液面低于刻度线,再加水至刻度线 |
您最近一年使用:0次



