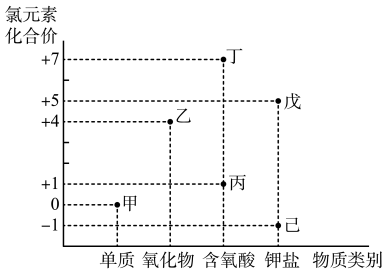
汽车安全气囊系统中有一定比例的叠氮化钠( ),氧化铁、硝酸铵等物质,受到撞击点火器点火引发叠氨化钠迅速分解生成氮气和钠,硝酸铵分解为一氧化二氮和水蒸气。下列说法错误的是
),氧化铁、硝酸铵等物质,受到撞击点火器点火引发叠氨化钠迅速分解生成氮气和钠,硝酸铵分解为一氧化二氮和水蒸气。下列说法错误的是
 ),氧化铁、硝酸铵等物质,受到撞击点火器点火引发叠氨化钠迅速分解生成氮气和钠,硝酸铵分解为一氧化二氮和水蒸气。下列说法错误的是
),氧化铁、硝酸铵等物质,受到撞击点火器点火引发叠氨化钠迅速分解生成氮气和钠,硝酸铵分解为一氧化二氮和水蒸气。下列说法错误的是| A.叠氮化钠的稳定性较弱 |
| B.硝酸铵分解反应中,氧化剂和还原剂的物质的量之比为2∶1 |
| C.金属钠和氧化铁反应生成铁和氧化钠 |
| D.该系统利用了化学反应的物质变化、能量变化和化学反应速率等因素 |
22-23高三上·山东济宁·期末 查看更多[2]
更新时间:2023-01-15 14:59:41
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某离子反应涉及H2O、 、
、 、H+、N2、
、H+、N2、 六种微粒。其中
六种微粒。其中 随反应进行逐渐减小(溶液的总体积不变)。下列判断正确的是
随反应进行逐渐减小(溶液的总体积不变)。下列判断正确的是
 、
、 、H+、N2、
、H+、N2、 六种微粒。其中
六种微粒。其中 随反应进行逐渐减小(溶液的总体积不变)。下列判断正确的是
随反应进行逐渐减小(溶液的总体积不变)。下列判断正确的是A.反应的氧化产物是 | B.反应后溶液的酸性明显增强 |
C.氧化剂与还原剂的物质的量之比为 | D.反应方程式中H2O出现在反应物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的氧化物均是空气污染物,燃油发动机工作时会产生NO,若要将NO转化为 ,从性质考虑下列物质中可以选择与之反应的是
,从性质考虑下列物质中可以选择与之反应的是
 ,从性质考虑下列物质中可以选择与之反应的是
,从性质考虑下列物质中可以选择与之反应的是| A.CO | B.NaClO | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 | B.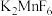 是氧化产物 是氧化产物 |
| C.氧化剂与还原剂物质的量之比为2:3 | D.生成1mol  ,转移4mol电子 ,转移4mol电子 |
您最近一年使用:0次
【推荐2】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多0.7mol,则下列判断正确的是
| A.生成15.68LN2(标准状况) | B.有0.1molKNO3被氧化 |
| C.转移电子的物质的量为0.25mol | D.被氧化的N原子的物质的量为1.5mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】为确定 NaBr 和 NaI 固体混合物样品的组成,称取三份质量均为 35.60 g 的固体溶于水,三份溶液分别与一定体积的 Cl2(气体体积均已折算成标准状况下的体积)充分反应,再将溶液蒸干,称量所 得固体的质量,得到数据如下表:
下列说法不正确的是
| 实验序号 | 1 | 2 | 3 |
| Cl2 体积/L | 2.24 | 4.48 | 6.72 |
| 所得固体质量/g | 22.00 | 17.55 | 17.55 |
| A.实验 1 溶液蒸干所得固体可能是 NaCl、NaBr 和 NaI |
| B.实验 2 和实验 3 溶液蒸干所得固体一定是 NaCl |
| C.原固体混合物中 NaBr 和 NaI 的物质的量之比为 2∶1 |
| D.当 Cl2 体积为 3.36 L 时,所得固体的质量为 17.55 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验相关叙述正确的是
| A.中和滴定实验过程中,眼睛应注视锥形瓶中溶液颜色的变化 |
| B.将钢铁闸门连接电源负极的保护方法称为牺牲阳极的阴极保护法 |
| C.用湿润的pH试纸测电解质稀溶液的pH一定存在实验误差 |
| D.NH4NO3固体溶于水后溶液温度降低,说明盐类的水解都是吸热过程 |
您最近一年使用:0次
【推荐2】在一定温度下,将1molCO2和3molH2充入体积为1L的恒容密闭容器中发生反应并达到平衡:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法
CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法不正确 的是
 CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法
CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法| A.平衡混合气体中C原子的物质的量是1mol |
| B.该反应的反应物的总能量高于生成物的总能量 |
C.该反应的化学平衡常数K= |
| D.其他条件相同时,若起始充入2molCO2和6molH2,达到平衡时CH3OH的物质的量分数大于25% |
您最近一年使用:0次