A、B、C、D、E、F均为36号以前的元素,原子序数依次增大。A元素在p区,其基态原子最外层有1个未成对电子;B、C、D为相邻元素,B的最高价氧化物的水化物可以和B的氢化物发生反应;请回答下列问题:
(1)A基态原子的电子排布式为_______ ,其原子核外占据最高能层电子的电子云轮廓图是_______ 形状。
(2)C基态原子的轨道表示式为_______ 。
(3)B、C、D的第一电离能由小到大的顺序是_______ (填元素符号,下同),电负性由小到大的顺序是_______ 。
(4)E的基态原子价层电子在不同形状的原子轨道中运动的电子数相等,并且D、E形成的简单离子电子层结构相同,E在周期表中的位置_______ ,D、E形成的简单离子半径较小的是_______ (填离子符号)。
(5)F元素的基态原子的M能层全充满;N层没有成对电子,只有1个未成对电子。F的元素符号为_______ ,其基态原子的价层电子排布式为_______ ,在元素周期表中位于_______ 区(填“s”、“p”、“d”或“ds”)。
(1)A基态原子的电子排布式为
(2)C基态原子的轨道表示式为
(3)B、C、D的第一电离能由小到大的顺序是
(4)E的基态原子价层电子在不同形状的原子轨道中运动的电子数相等,并且D、E形成的简单离子电子层结构相同,E在周期表中的位置
(5)F元素的基态原子的M能层全充满;N层没有成对电子,只有1个未成对电子。F的元素符号为
更新时间:2023-01-12 19:03:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】(1)A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,D单质是一种淡黄色固体。请回答:
①C2B2的电子式是___________ ,D、E可形成化合物DE2中,存在下列哪些静电作用力______ 。
a.极性键 b.非极性键 c.范德华力 d.氢键 e.离子键
②B、C、E的离子半径由大到小的顺序为_______________ (用化学式回答),举一个事实证明E和D非金属性的强弱___________________ (用离子反应方程式表示)。
(2)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
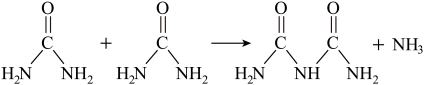
当尿素三聚时,得到两种产物,其中一种为环状结构,请画出其结构式___________ 。
(3)已知某元素的原子序数是33,试推测该元素:
①原子的原子结构示意图______________ 。
②在元素周期表中的位置______________ 。
①C2B2的电子式是
a.极性键 b.非极性键 c.范德华力 d.氢键 e.离子键
②B、C、E的离子半径由大到小的顺序为
(2)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:

当尿素三聚时,得到两种产物,其中一种为环状结构,请画出其结构式
(3)已知某元素的原子序数是33,试推测该元素:
①原子的原子结构示意图
②在元素周期表中的位置
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式______ 。
(2)用电子式表示⑥和⑨形成化合物的过程:______ 。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为______ (用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式______ 。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为______ (用离子符号表示)。

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式
(2)用电子式表示⑥和⑨形成化合物的过程:
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式
(5)⑤、⑥、⑩的离子半径由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表中的一部分。
根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)电负性最强的元素是________ ,第一电离能最小的单质是________ 。
(2)最高价氧化物对应的水化物中,酸性最强的是______ ,呈两性的是______ 。
(3)A分别与E、F、G、H、I形成的化合物中,沸点最高的是________ 。
(4)在B、C、D、G、I中,形成的简单离子半径最大的元素是________ 。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | A | |||||||
2 | E | F | H | J | ||||
3 | B | C | D | G | I |
(1)电负性最强的元素是
(2)最高价氧化物对应的水化物中,酸性最强的是
(3)A分别与E、F、G、H、I形成的化合物中,沸点最高的是
(4)在B、C、D、G、I中,形成的简单离子半径最大的元素是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F六种元素为原子序数依次增大的短周期元素。A为原子半径最小的元素,A和B可形成4原子10电子的分子X;C的最外层电子数是内层的3倍;D原子的最外层电子数是最内层电子数的一半;E是地壳中含量最多的金属元素;F元素的最高正价与最低负价代数和为6。请回答下列问题:(用化学用语填空)
(1)B、C、D、E、F五种元素原子半径由大到小的顺序是________ 。
(2)A和C按原子个数比1:1形成4原子分子Y,Y的结构式是________ 。
(3)B、C两种元素的简单气态氢化物结合质子的能力较强的为________ (填化学式),用一个离子方程式证明:________ 。
(4)D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式________ 。
(5)实验证明,熔融的EF3不导电,其原因是________ 。
(1)B、C、D、E、F五种元素原子半径由大到小的顺序是
(2)A和C按原子个数比1:1形成4原子分子Y,Y的结构式是
(3)B、C两种元素的简单气态氢化物结合质子的能力较强的为
(4)D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式
(5)实验证明,熔融的EF3不导电,其原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F、G、H为八种短周期主族元素,原子序数依次增大。A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、H在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17。D与F同周期。G的单质常用作半导体材料。请回答:
(1)C和H分别与A形成的简单化合物沸点较高的是________ (填化学式),理由是_____________ 。
(2)C、E形成的简单离子半径大小:r(C)______ r(E)(填>、<或=)
(3)请写出F最高价氧化物对应的水化物在水溶液中的电离方程式______________ 。
(4)B与G形成的化合物常用于做耐高温材料,工业可用碳热还原法制取:将G的氧化物与B的单质在1400℃条件下和足量的碳反应,请写出化学反应方程式_____________ 。
(1)C和H分别与A形成的简单化合物沸点较高的是
(2)C、E形成的简单离子半径大小:r(C)
(3)请写出F最高价氧化物对应的水化物在水溶液中的电离方程式
(4)B与G形成的化合物常用于做耐高温材料,工业可用碳热还原法制取:将G的氧化物与B的单质在1400℃条件下和足量的碳反应,请写出化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】W、X、Y、Z、N是原子序数依次增大的5种短周期元素,其元素性质或原子结构如表:
请完成下列空白:
(1)写出各元素的元素符号:W:____ 、X:____ 、Y:____ 、Z:____ 、N:____ 。
(2)X、Y和Z三种元素的原子半径由大到小的顺序:____ (请填元素符号)。
(3)X、Z和N三种元素的电负性由大到小的顺序:____ (请填元素符号)。
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:____ (请填元素符号)。
(5)已知金属性:K>Al,请用一个化学反应方程式表示:____ 。
| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| Z | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| N | 只有一个不成对电子 |
(1)写出各元素的元素符号:W:
(2)X、Y和Z三种元素的原子半径由大到小的顺序:
(3)X、Z和N三种元素的电负性由大到小的顺序:
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:
(5)已知金属性:K>Al,请用一个化学反应方程式表示:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】短周期五种元素 A、B、C、D、E,原子序数依次增大。已知:A 原子的核外电子数与电子层数相等;B 元素原子的核外 p 电子数比 s 电子数少 1 个;C 原子的第一至第四电离能为 I1=738 kJ·mol-1,I2=1 451 kJ·mol-1,I3=7 733 kJ·mol-1,I4=10 540 kJ·mol-1;D 原子核外所有 p 轨道为全充满或半充满;E 元素的族序数与周期序数的差为 4。
(1)写出 C 单质在 B 单质中燃烧的化学方程式:_______________________________________ 。
(2)某同学根据题目信息和掌握的知识分析 C 的核外电子排布为 该同学所画的轨道式违背了
该同学所画的轨道式违背了_______________ 原理(或规则)。
(3)用电子式表示 BA3的形成过程:__________________________ 。
(4)DE3中心原子杂化方式为_______________ ,其空间构型为_______________ 。
(1)写出 C 单质在 B 单质中燃烧的化学方程式:
(2)某同学根据题目信息和掌握的知识分析 C 的核外电子排布为
 该同学所画的轨道式违背了
该同学所画的轨道式违背了(3)用电子式表示 BA3的形成过程:
(4)DE3中心原子杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)GaAs是新型半导体材料,第一电离能As__________ Ga(填“>”或“<”),GaCl3与AsCl3的中心原子的杂化方式分别为______ 、______ ,分别写出一个与它们互为等电子体的分子______ 、________ 。
(2)TiO2离子晶体的其中一种晶胞如图1所示,则Ti、O配位数之比为_________ ;影响离子晶体结构类型的因素有______ 、______ 、键性因素。
(3)基态铜原子的电子排布式是______ 。基态铜原子价电子层排布依据的原理,可用于解释下列事实的是_____ (填标号)。
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(4)铜的堆积方式(如图2)和晶胞结构(如图3)所示。若晶胞顶点A与堆积方式中的A球相对应,则晶胞中x、y、z三点与堆积方式中C球相对应的点是______ 。
已知铜原子的半径为r cm、摩尔质量为Mg/mol、晶体的密度为_________ g/cm3(阿伏伽德罗常数取NA)
(2)TiO2离子晶体的其中一种晶胞如图1所示,则Ti、O配位数之比为

(3)基态铜原子的电子排布式是
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(4)铜的堆积方式(如图2)和晶胞结构(如图3)所示。若晶胞顶点A与堆积方式中的A球相对应,则晶胞中x、y、z三点与堆积方式中C球相对应的点是

已知铜原子的半径为r cm、摩尔质量为Mg/mol、晶体的密度为
您最近一年使用:0次
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p为26号元素,请写出其基态原子电子排布式:___________ 。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_________________ 。
(3)o、p两元素的部分电离能数据如表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是______ 。
(4)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是________ (填图中的序号)。
(5)题给周期表中所列的某主族元素的电离能情况如图所示,则该元素是__________ (填元素符号)。

(1)元素p为26号元素,请写出其基态原子电子排布式:
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(3)o、p两元素的部分电离能数据如表:
| 元素 电离能/kJ·mol-1 | o | p |
| I1 | 717 | 759 |
| I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 |
(4)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(5)题给周期表中所列的某主族元素的电离能情况如图所示,则该元素是

您最近一年使用:0次



