下列说法正确的是
A.因为氧化性:HClO>稀 ,所以非金属性:Cl>S ,所以非金属性:Cl>S |
| B.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强 |
| C.从上到下,卤族元素的非金属性逐渐减弱,所以酸性HCl>HI |
D.离子半径: |
更新时间:2023-01-13 18:00:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】类推的思维方法在化学学习和研究中有时会产生错误的结论,因此类推出的结论最终要经过实践的检验才能决定其正确与否。下列几种类推结论中正确的是
| A.ⅣA CH4的沸点低于SiH4,则ⅦA HF的沸点也低于HCl |
| B.可电解熔融MgCl2来制取金属镁,则也可电解熔融AlCl3来制取金属铝 |
| C.第二周期元素氢化物稳定性顺序是HF>H2O>NH3,则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
| D.晶体中有阴离子必有阳离子,则晶体中有阳离子也必有阴离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列排序正确的是
| A.酸性:H2CO3<C6H5OH<CH3COOH |
| B.碱性:Ba(OH)2<Ca(OH)2<KOH |
| C.熔点:MgBr2<SiCl4<SiO2 |
| D.沸点:PH3<NH3<H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某同学学习元素周期律后,作出以下推测,其中错误的是
| A.Ra是第七周期第IIA族的元素,推测Ra(OH)2碱性比Ba(OH)2强 |
| B.Sb是第四周期第VA族的元素,推测SbH3比NH3稳定 |
| C.Cs的原子半径大于Na的原子半径,推测Cs与水反应比Na与水反应更剧烈 |
| D.Cl的核电荷数比Al大,推测Cl的半径比Al的半径小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺。这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等。该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气。合金中镓(Ga,ⅢA)是关键成分,可阻止铝形成致密的氧化膜。下列关于铝、镓的说法正确的是
| A.铝原子半径比镓原子半径小,所以铝的金属性比镓强 |
| B.铝表面形成致密的氧化膜,所以可以用铝制容器来腌制咸菜 |
| C.Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应 |
| D.铝离子半径比镓离子半径小,所以铝的熔点比镓高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X的简单气态氢化物溶于水呈碱性,基态Y原子无未成对电子,Z的某种氧化物具有漂白性。下列说法正确的是
| A.电负性:W<Z<X |
B.原子半径: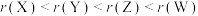 |
| C.最高价氧化物对应水化物的酸性:W<Z |
| D.Y的单质与X、Z、W的单质均能发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验装置或方案能达到实验目的的是
 |  | 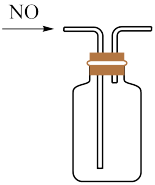 |  |
| A.比较C和Si的非金属性 | B.制备并收集 | C.收集NO气体 | D.比较 和 和 催化效果 催化效果 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】电子层数相同的三种元素 、
、 、
、 ,已知最高价氧化物对应水化物的酸性:
,已知最高价氧化物对应水化物的酸性: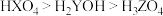 ,则下列判断错误的是
,则下列判断错误的是
 、
、 、
、 ,已知最高价氧化物对应水化物的酸性:
,已知最高价氧化物对应水化物的酸性: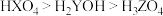 ,则下列判断错误的是
,则下列判断错误的是A.原子半径: |
B.气态氢化物的稳定性: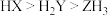 |
C.非金属性: |
D.阴离子的还原性: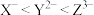 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】X、Y、Z、W为原子序数依次增大的短周期主族元素,其中X、Y相邻,Y是地壳中含量最高的元素,Z的原子半径在短周期元素中最大,W形成的单质可用于自来水消毒。下列说法错误的是
A.最简单氢化物的熔沸点: | B.简单离子半径: |
C. 的最高价氧化物对应的水化物为强酸 的最高价氧化物对应的水化物为强酸 | D.X、Y按原子个数比1∶1组成的化合物为无色气体 |
您最近一年使用:0次



