下列说法错误的是
A. 键的电子云重叠程度比 键的电子云重叠程度比 键大,稳定性强 键大,稳定性强 |
B.N与3个H结合形成 分子,体现了共价键的饱和性 分子,体现了共价键的饱和性 |
C.第三周期主族元素中第一电离能介于 和P之间的有3种 和P之间的有3种 |
| D.短周期主族元素中位于s区的有5种 |
更新时间:2023-02-14 13:43:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.元素周期表中元素排序的依据是原子的核电荷数 |
| B.元素周期表有十六个纵列,也就是十六个族 |
| C.原子的最外层电子数相同的元素,一定属于同一族 |
| D.电子层数相同的粒子,对应元素一定属于同一周期 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】分别处于第二、三周期的主族元素A和B,它们离子的电子层相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B原子核外的电子总数分别为
| A.m+2、10+n | B.m、n |
| C.3、7 | D.m-2、10-n |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一种钠硫电池以钠和硫为电极反应物, 为正极材料,
为正极材料, 陶瓷为电解质隔膜。下列说法正确的是
陶瓷为电解质隔膜。下列说法正确的是
 为正极材料,
为正极材料, 陶瓷为电解质隔膜。下列说法正确的是
陶瓷为电解质隔膜。下列说法正确的是A.电离能大小: | B.半径大小: |
C.电负性大小: | D.酸性强弱: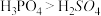 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】摩贝是一家化学品商业信息及行业资讯平台,该平台展示的某物质的结构如图所示:
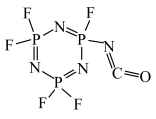
| A.第一电离能:O>N>P |
| B.热稳定性:HF>H2O>PH3 |
| C.所含第二周期元素的简单氢化物均为极性分子 |
D.基态氧原子的价电子轨道表示式若写为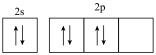 ,则违背了泡利原理 ,则违背了泡利原理 |
您最近一年使用:0次
【推荐3】X、Y、Z、Q、T、W为前36号元素,原子序数依次增大。其中仅X、Y、Z为短周期主族元素,且分占三个周期。基态Y元素原子价层p轨道上的电子数比s轨道多,且第一电离能小于同周期的相邻元素;在同周期元素中,Z的电负性最大;基态W元素原子的4p轨道半充满;Q和T既处于同一周期又位于同一族,且原子序数T比Q多2。下列说法正确的是
| A.基态Y原子核外电子有8种空间运动状态 |
B.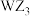 为非极性分子 为非极性分子 |
C.与X形成的简单化合物沸点: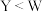 |
D.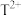 有2个未成对电子 有2个未成对电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】尿素可以减少柴油机尾气氮氧化物的排放,发生反应: ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是
 ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是A. 均为非极性分子 均为非极性分子 | B.标况下,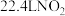 含有电子数 含有电子数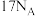 |
C. 中含有 中含有 键数目为 键数目为 | D.反应过程中生成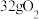 时转移电子数为 时转移电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法中不正确的是
| A.N2分子有一个δ键,两个π键 |
| B.δ键比π键重叠程度大,形成的共价键强 |
C.电子排布图 违背了洪特规则 违背了洪特规则 |
| D.气体单质中,一定有δ键,可能有π键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期元素X、Y、Z、W中,X元素的原子最外层电子排布为ns1,Y元素的原子价电子排布为ns2np2,Z元素的最外层电子数是其电子层数的3倍,W元素原子的M电子层的p能级中有3个未成对电子。
(1)Z原子的电子排布式为_______ ,若X为非金属元素,则按原子轨道的重叠方式,X与Z形成的化合物中的共价键属于_______ 键(填“σ”或“x”)。
(2)当 时,Y在元素周期表的位置为
时,Y在元素周期表的位置为____ ,YZ2属于____ 分子(填“极性”或“非极性”)。
(3)当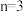 时,YZ2晶体属于
时,YZ2晶体属于_______ 晶体;在Y的含氧酸盐中,Y和Z结合成 四面体,
四面体, 的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为_______ 。

(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(1)Z原子的电子排布式为
(2)当
 时,Y在元素周期表的位置为
时,Y在元素周期表的位置为(3)当
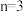 时,YZ2晶体属于
时,YZ2晶体属于 四面体,
四面体, 的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应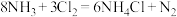 可用于氯气管道的检漏。下列说法正确的是
可用于氯气管道的检漏。下列说法正确的是
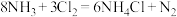 可用于氯气管道的检漏。下列说法正确的是
可用于氯气管道的检漏。下列说法正确的是A.中子数为20的氯原子: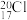 |
| B.N2分子中σ键和π键数目之比为2:1 |
C.NH3分子的电子式: |
D.氯化铵中 的空间构型为正四面体形 的空间构型为正四面体形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一种可吸附甲醇的材料,其化学式为[C(NH2)3]4[B(OCH3)4]3Cl,部分晶体结构如图所示,其中[C(NH2)3]+为平面结构。

| A.元素的电负性:C<N<O |
| B.该化合物中阴阳离子个数比为1:1 |
| C.该晶体中存在N﹣H…O氢键 |
| D.[C(NH2)3]+中C原子的杂化类型是sp3 |
您最近一年使用:0次


 紧邻且等距的Na+有8个
紧邻且等距的Na+有8个 g•cm-3
g•cm-3 的空间构型为正四面体形
的空间构型为正四面体形

