乙烯气相直接水合法过程中会发生乙醇的异构化反应: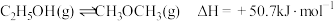 ,该反应的速率方程可表示为
,该反应的速率方程可表示为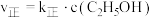 和
和 ,
,
 和只与温度有关。该反应的活化能
和只与温度有关。该反应的活化能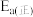
_______ (填“>”“=”或“<”)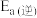 ,已知:
,已知: 时,
时,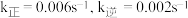 ,该温度下向某恒容密闭容器中充入
,该温度下向某恒容密闭容器中充入 乙醇和
乙醇和 甲醚,此时反应
甲醚,此时反应_______ (填“正向”或“逆向”)进行。
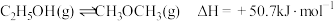 ,该反应的速率方程可表示为
,该反应的速率方程可表示为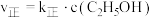 和
和 ,
,
 和只与温度有关。该反应的活化能
和只与温度有关。该反应的活化能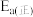
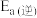 ,已知:
,已知: 时,
时,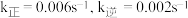 ,该温度下向某恒容密闭容器中充入
,该温度下向某恒容密闭容器中充入 乙醇和
乙醇和 甲醚,此时反应
甲醚,此时反应
2023高三·全国·专题练习 查看更多[1]
(已下线)第七章 化学反应速率与化学平衡 热点强化14 速率常数与化学平衡常数的关系
更新时间:2023-02-11 21:11:15
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】努力实现碳达峰、碳中和展现了我国积极参与和引领全球气候治理的大国担当,其中对于CO2的综合利用是实现碳中和的保证。
I.回收利用CO2解决空间站供氧问题物质转化如图所示:
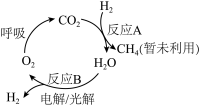
反应A为CO2(g)+4H2(g) CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
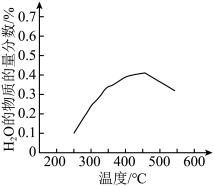
(1)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示。理论上能提高CO2平衡转化率的措施为______ (单选)。
(2)下列能说明反应A已达平衡的是______ (单选)。
(3)空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,可能的原因是______ 。
(4)在容积为1L的密闭容器中充入4molH2(g)和1molCO2(g)发生反应,测得10min时反应达到平衡状态,此时容器内H2O(g)的体积分数为0.25,若此时向容器内额外充入1molH2(g)和0.5molH2O(g),则该平衡将向着______ 方向移动(填“正”或“逆”)。
II.某研究团队利用2CO2(g)+6H2(g) C2H4(g)+4H2O(g)生产乙烯。
C2H4(g)+4H2O(g)生产乙烯。
在三个容积均为1L的密闭容器中以不同的氢碳比[ ]充入H2(g)和CO2(g),在一定条件下CO2(g)的平衡转化率与温度的关系如图所示。
]充入H2(g)和CO2(g),在一定条件下CO2(g)的平衡转化率与温度的关系如图所示。
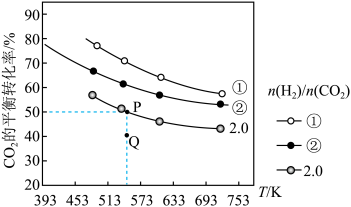
(5)下列说法不正确的是______ (不定项)。
(6)在上述2L的密闭容器中充入2molH2(g)和1molCO2(g)发生反应,10min后到达P点,那么这10min内H2O(g)的反应速率为______ 。
I.回收利用CO2解决空间站供氧问题物质转化如图所示:

反应A为CO2(g)+4H2(g)
 CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。(1)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示。理论上能提高CO2平衡转化率的措施为

| A.升高温度 | B.及时从体系中移走水蒸气 |
| C.恒容条件下向容器中冲入氩气 | D.提高原料气中CO2的比例 |
| A.生成4molH2(g)的同时消耗2mol2H2O(g) |
| B.容器内混合气体的密度保持不变 |
| C.容器内混合气体的平均相对分子质量保持不变 |
| D.容器内CO2与H2物质的量之比保持不变 |
(4)在容积为1L的密闭容器中充入4molH2(g)和1molCO2(g)发生反应,测得10min时反应达到平衡状态,此时容器内H2O(g)的体积分数为0.25,若此时向容器内额外充入1molH2(g)和0.5molH2O(g),则该平衡将向着
II.某研究团队利用2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)生产乙烯。
C2H4(g)+4H2O(g)生产乙烯。在三个容积均为1L的密闭容器中以不同的氢碳比[
 ]充入H2(g)和CO2(g),在一定条件下CO2(g)的平衡转化率与温度的关系如图所示。
]充入H2(g)和CO2(g),在一定条件下CO2(g)的平衡转化率与温度的关系如图所示。
(5)下列说法不正确的是
| A.该反应的正反应活化能E1>逆反应活化能E2 |
| B.氢碳比:①>② |
| C.在氢碳比为2.0时,Q点:v(正)<v(逆) |
| D.该反应发生前后C原子的杂化方式发生改变 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】Ⅰ.在一定温度下,把2 mol N2和6 mol H2通入一个体积不变的密闭容器中(如图)发生以下的反应:

N2(g)+3 H2(g) 2NH3 (g) (正反应为放热反应)
2NH3 (g) (正反应为放热反应)
若反应达到平衡后,测得混和气体为7 mol ,据此回答下列问题:
保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a=1mol ,c=2mol ,则b=____ mol,在此情况下,反应起始时将向_______ 方向进行(填 “正反应”或“逆反应”)
(2)若规定起始时反应向逆反应方向进行,则c的范围是____________ 。
(3)在上述装置中,若需控制平衡后的混和气体的物质的量为6.5 mol,则可采取的措施是___________________________________
Ⅱ.如图所示,温度不变时,把某容器分割成A、B两部分,A容器体积固定不变,B有可移动的活塞,现在A中充入2 mol SO2和1 mol O2,在B中充入2 mol SO3和 1 mol N2,在相同条件下发生可逆反应:2 SO2(g)+O2(g) 2 SO3(g)。根据下列要求填写空白:
2 SO3(g)。根据下列要求填写空白:

(1)固定活塞位置在3处不动,达到平衡时,设A中压强为PA,B中压强为PB,则PA与PB的关系是PA____ PB(填“<”、“=”、“>”)。
(2)若要使A与B中平衡状态相同,可移动活塞的位置应在______ 处。
(3)若活塞右移到5处,达到平衡后,B中SO3为x mol,A中SO3为y mol , 则x和y 的关系是x_____ y(填“<”、“=”、“>”)。

N2(g)+3 H2(g)
 2NH3 (g) (正反应为放热反应)
2NH3 (g) (正反应为放热反应)若反应达到平衡后,测得混和气体为7 mol ,据此回答下列问题:
保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a=1mol ,c=2mol ,则b=
(2)若规定起始时反应向逆反应方向进行,则c的范围是
(3)在上述装置中,若需控制平衡后的混和气体的物质的量为6.5 mol,则可采取的措施是
Ⅱ.如图所示,温度不变时,把某容器分割成A、B两部分,A容器体积固定不变,B有可移动的活塞,现在A中充入2 mol SO2和1 mol O2,在B中充入2 mol SO3和 1 mol N2,在相同条件下发生可逆反应:2 SO2(g)+O2(g)
 2 SO3(g)。根据下列要求填写空白:
2 SO3(g)。根据下列要求填写空白:
(1)固定活塞位置在3处不动,达到平衡时,设A中压强为PA,B中压强为PB,则PA与PB的关系是PA
(2)若要使A与B中平衡状态相同,可移动活塞的位置应在
(3)若活塞右移到5处,达到平衡后,B中SO3为x mol,A中SO3为y mol , 则x和y 的关系是x
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4−(绿色)、Cr2O72−(橙红色)、CrO42−(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+ 与 Al3+ 的化学性质相似,在Cr2(SO4)3 溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________ 。
(2)CrO42− 和 Cr2O72− 在溶液中可相互转化。室温下,初始浓度为1. 0 mol·L−1的Na2CrO4 溶液中c(Cr2O72−) 随c(H+) 的变化如图所示。
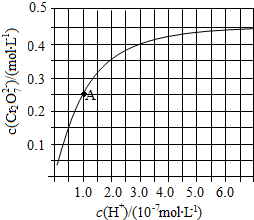
①用离子方程式表示Na2CrO4溶液中的转化反应____________ 。
②由图可知,溶液酸性减小,CrO42− 的平衡转化率__________ (填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的逆反应 的平衡常数为__________ 。
③升高温度,溶液中CrO42−的平衡转化率减小,则该反应的ΔH____ 0(填“大于”“小于”或“等于”)。
(3)+6价铬的化合物毒性较大,常用NaHSO3将废液中的 Cr2O72− 还原成 Cr3+,反应的离子方程式为______________ 。
(1)Cr3+ 与 Al3+ 的化学性质相似,在Cr2(SO4)3 溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是
(2)CrO42− 和 Cr2O72− 在溶液中可相互转化。室温下,初始浓度为1. 0 mol·L−1的Na2CrO4 溶液中c(Cr2O72−) 随c(H+) 的变化如图所示。

①用离子方程式表示Na2CrO4溶液中的转化反应
②由图可知,溶液酸性减小,CrO42− 的平衡转化率
③升高温度,溶液中CrO42−的平衡转化率减小,则该反应的ΔH
(3)+6价铬的化合物毒性较大,常用NaHSO3将废液中的 Cr2O72− 还原成 Cr3+,反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】在一定温度下,向一固定容积的密闭容器中加入1molM和2molN,发生反应:M(g)+2N(g) 3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ
3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ
(1)若维持容器的体积和温度不变,反应从逆反应方向开始,Q和R按一定的物质的量作为起始反应物质,达到平衡时Q仍为1.8mol。则R的起始物质的量n(R)应满足的条件是:n(R)_________ mol。
(2)若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:_______________ 。
(3)若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,M的物质的量浓度为a mol·L-1,现持续增大压强。
①当压强为原来的1.5倍时,平衡时M的物质的量浓度为m mol·L-1,测得m=1.5a;
②当压强为原来的10倍时,平衡时M的物质的量浓度为n mol·L-1,测得n>10a;
试解释形成这种结果的可能的原因:
①1.5倍时:_____________________________________________ ;
②10倍时:_____________________________________________ 。
 3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ
3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ(1)若维持容器的体积和温度不变,反应从逆反应方向开始,Q和R按一定的物质的量作为起始反应物质,达到平衡时Q仍为1.8mol。则R的起始物质的量n(R)应满足的条件是:n(R)
(2)若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:
(3)若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,M的物质的量浓度为a mol·L-1,现持续增大压强。
①当压强为原来的1.5倍时,平衡时M的物质的量浓度为m mol·L-1,测得m=1.5a;
②当压强为原来的10倍时,平衡时M的物质的量浓度为n mol·L-1,测得n>10a;
试解释形成这种结果的可能的原因:
①1.5倍时:
②10倍时:
您最近一年使用:0次



