硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
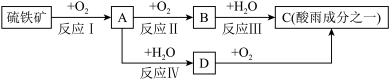
回答下列问题:
(1)硫铁矿中S元素的化合价为_______ 。
(2)为了确定A中S元素的化合价,将其通入新制氯水中,发现溶液褪色,请写出该过程的化学方程式_______ 。
(3)“A→B→C”与“A→D→C”是形成酸雨的两种常见途径,请写出D→C的化学方程式_______ 。
(4)已知反应Ⅲ是放热反应,该反应也是工业制硫酸的主要步骤之一,但在实际工业生产中常用98%的浓硫酸代替水来吸收B气体,其目的是_______ 。
(5)利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫的过程如下图所示:
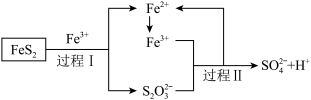
①已知催化脱硫过程的总反应为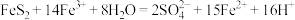 ,则过程Ⅱ反应的离子方程式为
,则过程Ⅱ反应的离子方程式为_______ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀,其原因可能是
在酸性溶液中会形成淡黄色沉淀,其原因可能是_______ (用离子方程式表示)。从氧化还原角度分析,若要制备 应选择
应选择_______ (填字母)。
A. B.
B. C.
C. D.
D.
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
回答下列问题:
(1)硫铁矿中S元素的化合价为
(2)为了确定A中S元素的化合价,将其通入新制氯水中,发现溶液褪色,请写出该过程的化学方程式
(3)“A→B→C”与“A→D→C”是形成酸雨的两种常见途径,请写出D→C的化学方程式
(4)已知反应Ⅲ是放热反应,该反应也是工业制硫酸的主要步骤之一,但在实际工业生产中常用98%的浓硫酸代替水来吸收B气体,其目的是
(5)利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫的过程如下图所示:

①已知催化脱硫过程的总反应为
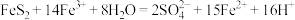 ,则过程Ⅱ反应的离子方程式为
,则过程Ⅱ反应的离子方程式为②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀,其原因可能是
在酸性溶液中会形成淡黄色沉淀,其原因可能是 应选择
应选择A.
 B.
B. C.
C. D.
D.
更新时间:2023-02-16 09:13:59
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某磁性固体A仅含两种元素,为探究A的组成,某研究小组进行如下实验(图中部分产物未标出):
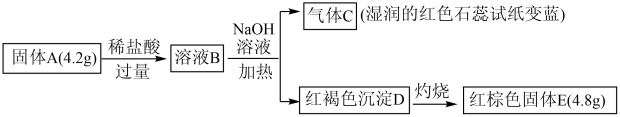
请回答:
(1)组成A的两种元素是_______ ;A的化学式为_______ 。
(2)沉淀D可溶于稀硫酸,发生反应的离子方程式 为_______ ;检验沉淀D溶于过量稀硫酸后溶液中的金属阳离子的实验方案为_______ 。
(3)溶液B与 溶液
溶液共热 产生气体C的离子方程式 为_______ 。

请回答:
(1)组成A的两种元素是
(2)沉淀D可溶于稀硫酸,发生反应的
(3)溶液B与
 溶液
溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】中医认为,明矾[KAl(SO4)2·12H2O]具有解毒杀虫,燥湿止痒,止血止泻,清热消痰的功效。实验室用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制取明矾的流程如下图所示。请回答下列问题:

(1)明矾溶于水后呈________ 性(填“酸”、“碱”或“中”);其原因是______ (用离子程式表示)。
(2)明矾溶于水后所得的溶液中各离子浓度由大到小的顺序是__________ 。
(3)向明矾溶液中逐滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH_____ 7(填“>”、“<”、“=”),离子反应总方程式为_________________
(4)为尽量少引入杂质,流程中的“试剂”应选用______________ (填标号)。
A.NaCl溶液 B.KOH溶液 C.氨水 D.H2SO4溶液
(5)流程图中“沉淀”的化学式为_________________ 。
(6)已知:Kw=l.0×10-14,Al(OH)3 AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于
AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于________________

(1)明矾溶于水后呈
(2)明矾溶于水后所得的溶液中各离子浓度由大到小的顺序是
(3)向明矾溶液中逐滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH
(4)为尽量少引入杂质,流程中的“试剂”应选用
A.NaCl溶液 B.KOH溶液 C.氨水 D.H2SO4溶液
(5)流程图中“沉淀”的化学式为
(6)已知:Kw=l.0×10-14,Al(OH)3
 AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于
AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐(含正盐和酸式盐),A、B、C溶于水后电离可以产生大量下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)气体X为_______ ,沉淀E为_______ ,沉淀D为_______ 。
(2)B在水溶液中的电离方程式为_______ 。
(3)X与C生成E的离子方程式_______ 。
| 阳离子 |  |
| 阴离子 | 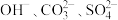 |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)气体X为
(2)B在水溶液中的电离方程式为
(3)X与C生成E的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】晶体硅是一种重要的非金属材料,有科学家认为硅是“21世纪的能源”、“未来的石油”。
(1)工业上生产纯硅的工艺流程如下:

石英砂的主要成分是SiO2,在制备粗硅时,焦炭的作用是__________ (填“氧化剂”或“还原剂”);在该反应中,若消耗了3.0 g SiO2 ,则转移电子的总数为_______________ 。
(2)某实验室利用SiHCl3(沸点33.0 ℃)与过量H2在1 000 ℃~1 100 ℃反应制得纯硅。已知SiHCl3能与H2O强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。

①装置B中的试剂是___________ 。装置C中的烧瓶需要加热,其目的是_________________ 。
②反应一段时间后,装置D中观察到的现象是______________________ ;装置D中发生反应的化学方程式为___________________________________ 。
③为检验产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有______ (填字母)。
a.碘水 b.氯水 c.Na2SO3溶液 d.KSCN溶液
(1)工业上生产纯硅的工艺流程如下:

石英砂的主要成分是SiO2,在制备粗硅时,焦炭的作用是
(2)某实验室利用SiHCl3(沸点33.0 ℃)与过量H2在1 000 ℃~1 100 ℃反应制得纯硅。已知SiHCl3能与H2O强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。

①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为检验产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有
a.碘水 b.氯水 c.Na2SO3溶液 d.KSCN溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】碘是人体生长发育不可缺少的微量元素,海带中富含碘元素,从海带中提取碘的工艺流程如下。回答下列问题:

(1)步骤①中发生反应的离子方程式为_______ ,当生成0.3molI2时,转移电子的物质的量为_______ mol。
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为_______ 。
(3)步骤③中发生反应的化学方程式为_______ 。
(4)步骤⑤的实验操作名称为_______ 。
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为_______ 法。

(1)步骤①中发生反应的离子方程式为
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为
(3)步骤③中发生反应的化学方程式为
(4)步骤⑤的实验操作名称为
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
您最近一年使用:0次
【推荐3】PH3是粮食杀虫处理时常用的熏蒸杀虫剂;水煤气变换时产生的PH3能使催化剂中毒,必须脱除。回答下列问题:
(1)PH3通入 NaClO溶液脱除PH3时,氧化产物是一种含氧酸且反应中氧化剂与还原剂的物质的量之比为4:1,则该含氧酸的化学式为______ 。
(2)已知下列键能数据及P4(白磷)分子结构:
则反应4PH3(g)⇌P4(g)+6H2(g)△H=______ kJ•mol-1;某温度时平衡体系中c(PH3)=0.25mol•L-1,c(H2)=c(P4)=0.50mol•L-1,则平衡常数K=______ 。
(3)文献报道“反应6.25CO2(g)+Fe3O4(s)+3PH3(g)=3FePO4(s)+4.5H2O(g)+6.25C(s)”是铁触媒中毒的主导反应,其平衡常数Kp(Kp为以分压表示的平衡常数)的对数值与温度的关系如图所示:

①该反应的△H______ 0(填“>”“<”或“=”)。
②图中lgKp=______ [列出用分压p(CO2)、p(PH3)、p(H2O)表示的计算式]。
(4)反应(CH3)3AuPH3→(CH3)AuPH3+C2H6的历程如下:
第一步:(CH3)3AuPH3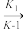 (CH3)3Au+PH3(快反应)
(CH3)3Au+PH3(快反应)
第二步:(CH3)3Au C2H6+CH3Au(慢反应)
C2H6+CH3Au(慢反应)
第三步:CH3Au+PH3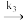 (CH3)AuPH3(快反应)
(CH3)AuPH3(快反应)
①反应的中间产物有PH3、______ 。
②第______ 步(填“一”“二”或“三”)反应的活化能最大。
(5)用Cu2+、Pd2+液相脱除PH3的反应为:PH3+2O2 H3PO4,其他条件相同时溶解在溶液中O2的体积分数、PH3的净化效率与时间的关系如图所示:
H3PO4,其他条件相同时溶解在溶液中O2的体积分数、PH3的净化效率与时间的关系如图所示:

O2的体积分数大,PH3的净化效率高的原因是______ (用碰撞理论等说明)。
(1)PH3通入 NaClO溶液脱除PH3时,氧化产物是一种含氧酸且反应中氧化剂与还原剂的物质的量之比为4:1,则该含氧酸的化学式为
(2)已知下列键能数据及P4(白磷)分子结构:
| 化学键 | P-P | H-H | P-H |  |
| 键能/(kJ•mol-1) | 213 | 436 | 322 |
(3)文献报道“反应6.25CO2(g)+Fe3O4(s)+3PH3(g)=3FePO4(s)+4.5H2O(g)+6.25C(s)”是铁触媒中毒的主导反应,其平衡常数Kp(Kp为以分压表示的平衡常数)的对数值与温度的关系如图所示:

①该反应的△H
②图中lgKp=
(4)反应(CH3)3AuPH3→(CH3)AuPH3+C2H6的历程如下:
第一步:(CH3)3AuPH3
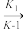 (CH3)3Au+PH3(快反应)
(CH3)3Au+PH3(快反应)第二步:(CH3)3Au
 C2H6+CH3Au(慢反应)
C2H6+CH3Au(慢反应)第三步:CH3Au+PH3
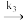 (CH3)AuPH3(快反应)
(CH3)AuPH3(快反应)①反应的中间产物有PH3、
②第
(5)用Cu2+、Pd2+液相脱除PH3的反应为:PH3+2O2
 H3PO4,其他条件相同时溶解在溶液中O2的体积分数、PH3的净化效率与时间的关系如图所示:
H3PO4,其他条件相同时溶解在溶液中O2的体积分数、PH3的净化效率与时间的关系如图所示:
O2的体积分数大,PH3的净化效率高的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】钠是正常生长发育中不可或缺的元素,钠及其化合物的部分转化关系如下。

回答下列问题:
(1)关于Na的叙述中正确的是___________ (填序号)。
①Na在自然界中既有游离态又有化合态 ②少量Na可以保存在冷水里
③Na着火时应用细沙盖灭 ④高压钠灯透雾能力强
(2)物质A为___________ (填颜色)固体;物质B的化学式为___________ 。
(3)物质C转化为D的化学方程式为___________ 。
(4)向足量 溶液中投入一小块Na,反应的实验现象为
溶液中投入一小块Na,反应的实验现象为___________ 。
(5)某研究性学习小组拟用如图装置测定 和
和 混合固体中
混合固体中 的质量分数。
的质量分数。

①正确连接装置后,检查装置气密性。称取5.0g样品于烧瓶中,打开活塞。
②在f处收集产生的气体,最终得到气体的质量为0.8g。
该 和
和 混合固体中
混合固体中 的质量分数为
的质量分数为___________ 。
(6)纯碱是钠的一种重要化合物,向稀盐酸中滴加少量纯碱溶液,发生反应的离子方程式为___________ 。

回答下列问题:
(1)关于Na的叙述中正确的是
①Na在自然界中既有游离态又有化合态 ②少量Na可以保存在冷水里
③Na着火时应用细沙盖灭 ④高压钠灯透雾能力强
(2)物质A为
(3)物质C转化为D的化学方程式为
(4)向足量
 溶液中投入一小块Na,反应的实验现象为
溶液中投入一小块Na,反应的实验现象为(5)某研究性学习小组拟用如图装置测定
 和
和 混合固体中
混合固体中 的质量分数。
的质量分数。
①正确连接装置后,检查装置气密性。称取5.0g样品于烧瓶中,打开活塞。
②在f处收集产生的气体,最终得到气体的质量为0.8g。
该
 和
和 混合固体中
混合固体中 的质量分数为
的质量分数为(6)纯碱是钠的一种重要化合物,向稀盐酸中滴加少量纯碱溶液,发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。

请问答下列问题:
(1)A是____________ ,G是______________ 。(填化学式)
(2)反应①-⑤中,属于氧化还原反应的是________________ (填序号)。
(3)反应⑤的化学方程式为_________________________ 。
甲与B反应的离子方程式___________________________ 。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是___________________ 。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式:____________________ 。
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和 100g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去。(假设过程中液体体积不变)①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。
上述观点是否正确_____________ ,请通过计算对比数据加以说明_____________________ 。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的。试设计简单实验证明烧瓶内溶液中含H2O2,简述实验原理_____________________________ 。

请问答下列问题:
(1)A是
(2)反应①-⑤中,属于氧化还原反应的是
(3)反应⑤的化学方程式为
甲与B反应的离子方程式
(4)在实验室将C溶液滴入F溶液中,观察到的现象是
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式:
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和 100g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去。(假设过程中液体体积不变)①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。
上述观点是否正确
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的。试设计简单实验证明烧瓶内溶液中含H2O2,简述实验原理
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠的四种无色溶液,为了测定四种溶液各是什么?将它们随意编号为 、
、 、
、 、
、 后,按下表进行实验。产生的现象如表所示:
后,按下表进行实验。产生的现象如表所示:
回答下列问题:
(1) 、
、 溶液中分散质的化学式:
溶液中分散质的化学式: :
:_______ ; :
:_______ 。
(2)写出实验顺序①②中有关的离子方程式,不反应的说明理由。
①_______ ;
②_______ 。
(3)写出下列反应的离子方程式。
①碳酸氢钙溶液与过量烧碱溶液混合:_______ ;
②向 溶液逐滴加
溶液逐滴加 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:_______ 。
 、
、 、
、 、
、 后,按下表进行实验。产生的现象如表所示:
后,按下表进行实验。产生的现象如表所示:| 实验顺序 | 实验内容 | 实验现象 |
| ① |  | 没有现象发生 |
| ② |  | 有气体放出 |
| ③ |  | 有沉淀生成 |
| ④ |  | 有沉淀生成 |
(1)
 、
、 溶液中分散质的化学式:
溶液中分散质的化学式: :
: :
:(2)写出实验顺序①②中有关的离子方程式,不反应的说明理由。
①
②
(3)写出下列反应的离子方程式。
①碳酸氢钙溶液与过量烧碱溶液混合:
②向
 溶液逐滴加
溶液逐滴加 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去)。请回答下列问题:
A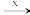 B
B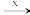 C
C D
D
(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。
①写出B→C的化学方程式_______ 。
②写出实验室制取B的化学方程式_______ 。
③写出Cu与A反应的化学方程式_______ 。
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B_______ ;B→C _______ ;C→D_______ 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式_______ 。
③用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为_______ mol•L-1。
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式_______ 。
②写出工业制取A气体的化学方程式_______ 。
③写出A→B的化学方程式_______ 。
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与SiO2反应的化学方程式_______ 。
②写出A与浓硫酸反应的化学方程式_______ 。
A
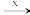 B
B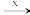 C
C D
D(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。
①写出B→C的化学方程式
②写出实验室制取B的化学方程式
③写出Cu与A反应的化学方程式
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式
③用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式
②写出工业制取A气体的化学方程式
③写出A→B的化学方程式
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与SiO2反应的化学方程式
②写出A与浓硫酸反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】β-MnS作为一种缓冲材料在太阳能电池上有巨大的应用潜力。β-MnS在空气中会慢慢氧化为硫酸锰,加热则生成二氧化硫和四氧化三锰。实验小组在实验室制备硫化锰(β-MnS)的装置如下。
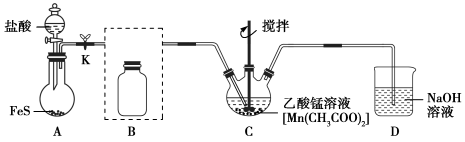
回答下列问题:
(1)检查装置A的气密性的方法是_______ 。
(2)请将除杂装置B补充完整并标明所用试剂________ 。
(3)C中制得β-MnS反应的化学方程式为_______ 。
将C中反应后的混合液经以下操作可得到纯净的β−MnS。

操作1是__ (填名称),洗涤操作中不用水而用H2S溶液的原因是___ ,β-MnS适于在___ (填“高温”或“低温”)的环境下干燥。
(4)某工业废水中含有大量的Mn2+、Hg2+,向此工业废水中加入适量的Na2S,当Mn2+恰好完全沉淀时,废水中Hg2+的浓度为_____ mol·L−1。[已知:Ksp(MnS)=2.5×10−13,Ksp(HgS)=6.4×10−53,当离子的浓度=1.0×10−5mol·L−1时可视为恰好完全沉淀]。
(5)点燃不纯的H2S气体可能会发生爆炸,为了防止意外,可连接一个安全装置,下图中的装置能起到作用的是_______ 。


回答下列问题:
(1)检查装置A的气密性的方法是
(2)请将除杂装置B补充完整并标明所用试剂
(3)C中制得β-MnS反应的化学方程式为
将C中反应后的混合液经以下操作可得到纯净的β−MnS。

操作1是
(4)某工业废水中含有大量的Mn2+、Hg2+,向此工业废水中加入适量的Na2S,当Mn2+恰好完全沉淀时,废水中Hg2+的浓度为
(5)点燃不纯的H2S气体可能会发生爆炸,为了防止意外,可连接一个安全装置,下图中的装置能起到作用的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(反应条件及部分产物已略去):
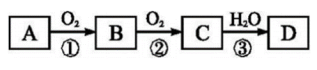
(1)若A是可溶于水的碱性气体。
i.写出反应①的化学方程式_______ 。
ii.实验室可用于检验A的试剂或用品有_______ 。
A.浓硫酸 B.浓盐酸 C.湿润的红色石蕊试纸 D.湿润的蓝色石蕊试纸
(2)若A是一种黄色固体单质,则将B通入 溶液中,充分反应后溶液变为浅绿色,写出反应的离子方程式
溶液中,充分反应后溶液变为浅绿色,写出反应的离子方程式_______ 。写出物质D的一种用途:_______ 。
(3)若A是一种金属单质,C是淡黄色固体。判断物质C中含有的化学键:_______ ,写出反应③的离子方程式为_______ 。将标准状况下 通过足量固体C,反应后测得残留气体在标准状况下体积为2.24L。则反应消耗的固体C的质量为
通过足量固体C,反应后测得残留气体在标准状况下体积为2.24L。则反应消耗的固体C的质量为_______ g。

(1)若A是可溶于水的碱性气体。
i.写出反应①的化学方程式
ii.实验室可用于检验A的试剂或用品有
A.浓硫酸 B.浓盐酸 C.湿润的红色石蕊试纸 D.湿润的蓝色石蕊试纸
(2)若A是一种黄色固体单质,则将B通入
 溶液中,充分反应后溶液变为浅绿色,写出反应的离子方程式
溶液中,充分反应后溶液变为浅绿色,写出反应的离子方程式(3)若A是一种金属单质,C是淡黄色固体。判断物质C中含有的化学键:
 通过足量固体C,反应后测得残留气体在标准状况下体积为2.24L。则反应消耗的固体C的质量为
通过足量固体C,反应后测得残留气体在标准状况下体积为2.24L。则反应消耗的固体C的质量为
您最近一年使用:0次



