如表为元素周期表的一部分。按要求回答下列问题:
(1)元素n在周期表中的位置为______ ,属于副族元素的为______ (用字母表示)。
(2)元素g的原子结构示意图为______ 。
(3)元素b的最高价氧化物的化学式为______ ,其简单氢化物的电子式为______ 。
(4)由a、c两种元素组成的化合物,原子个数比为1:2,其结构式为______ 。
(5)元素b、c、d、e简单离子半径由大到小的顺序是______ (用离子符号表示)。
(6)元素f的最高价氧化物和元素g的最高价氧化物对应的水化物反应的离子反应方程式为______ 。
(7)下列叙述能说明e原子失电子能力比f原子强的是______ (填序号)。
| a | b | c | d | ||||||||||||||
| e | f | g | |||||||||||||||
| h | m | n |
(2)元素g的原子结构示意图为
(3)元素b的最高价氧化物的化学式为
(4)由a、c两种元素组成的化合物,原子个数比为1:2,其结构式为
(5)元素b、c、d、e简单离子半径由大到小的顺序是
(6)元素f的最高价氧化物和元素g的最高价氧化物对应的水化物反应的离子反应方程式为
(7)下列叙述能说明e原子失电子能力比f原子强的是
| A.单质的熔点e比f低 |
| B.单质与盐酸反应e比f反应剧烈 |
| C.最外层电子数e原子的比f原子的少 |
| D.最高价氧化物对应水化物的碱性e比f强 |
更新时间:2023-02-15 09:04:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】下面是某同学学习硫元素的学习方案。
(1)硫元素的原子结构示意图是________________ ,从结构可以知道硫元素在周期表的位置为________________________________ 。
(2)硫元素在自然界中也有以化合态形式存在的,如许多金属矿石是含硫化合物,如胆矾________ 。(填化学式)
(3)设计如下实验探究硫和含硫化合物的相互转化:

①A中在加热时发生反应的化学方程式_____________ ;
②E中反应的离子方程式_______________________________
③G的作用是吸收尾气,写出反应的离子方程式。________________
(4)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑________________
②碳投入热的浓硫酸中溶解________________
③浓硫酸与氧化铜反应________________
④浓硫酸干燥氢气________________
(1)硫元素的原子结构示意图是
(2)硫元素在自然界中也有以化合态形式存在的,如许多金属矿石是含硫化合物,如胆矾
(3)设计如下实验探究硫和含硫化合物的相互转化:

①A中在加热时发生反应的化学方程式
②E中反应的离子方程式
③G的作用是吸收尾气,写出反应的离子方程式。
(4)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表表示的是元素周期表中短周期元素,根据要求回答下列问题:
(1)④⑥元素气态氢化物的稳定性比较______ >_______ (写化学式);
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为______ 、______ 。
(3)用电子式表示⑧和③元素形成A2B型化合物的过程_____________________
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程________________________
| ⑧ | |||||||
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | |||||
(1)④⑥元素气态氢化物的稳定性比较
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为
(3)用电子式表示⑧和③元素形成A2B型化合物的过程
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】(I)如表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素②和④的简单氢化物反应生成化合物的电子式为_______ 。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为_______ 。
(3)元素⑨在周期表中的位置是_______ 。
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:_______ 。
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为_______ (用相应的离子符号表示)。

(1)元素②和④的简单氢化物反应生成化合物的电子式为
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为
(3)元素⑨在周期表中的位置是
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
| 元素代号 | L | M | N | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.099 | 0.114 | 0.104 | 0.066 |
| 主要化合价 | +1 | +3 | +7、-1 | +7、-1 | +6、-2 | -2 |
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E为五种短周期主族元素,且原子序数依次增大,五种元素的原子序数之和为39,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等。
(1) A2C2的结构式为___________ 。
(2)E元素在元素周期表中的位置为___________ 。
(3)C、D、E三种元素的简单离子半径由小到大的顺序为___________ (填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成 ,
, 能与水反应生成A的单质,DA与水反应的化学方程式为
能与水反应生成A的单质,DA与水反应的化学方程式为___________ ;若将1 mol DA和1mol E的单质混合,加入足量的水,充分反应后生成气体的体积为_____ L(标准状况下)。
(5)若要比较D和E的金属性强弱,下列实验方案不可行的是_____ (填标号)。
A.将D的单质置于E的盐溶液中,若D的单质不能置换出E的单质,说明D的金属性弱
B.将少量D、E的单质分别投入水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的碱性,若D的最高价氧化物对应水化物的碱性强,说明D的金属性强
(6)用 和
和 组成以稀硫酸为电解质溶液的质子交换膜燃料电池,结构如图所示:
组成以稀硫酸为电解质溶液的质子交换膜燃料电池,结构如图所示:

①电极N是___________ (填“正极”或“负极”),电极M上的电极反应式为___________ 。
②若该燃料电池消耗11.2 L(标准状况下)BA4,则理论上电路中转移___________ mol电子。
(1) A2C2的结构式为
(2)E元素在元素周期表中的位置为
(3)C、D、E三种元素的简单离子半径由小到大的顺序为
(4)在一定条件下,D元素的单质能与A元素的单质化合生成
 ,
, 能与水反应生成A的单质,DA与水反应的化学方程式为
能与水反应生成A的单质,DA与水反应的化学方程式为(5)若要比较D和E的金属性强弱,下列实验方案不可行的是
A.将D的单质置于E的盐溶液中,若D的单质不能置换出E的单质,说明D的金属性弱
B.将少量D、E的单质分别投入水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的碱性,若D的最高价氧化物对应水化物的碱性强,说明D的金属性强
(6)用
 和
和 组成以稀硫酸为电解质溶液的质子交换膜燃料电池,结构如图所示:
组成以稀硫酸为电解质溶液的质子交换膜燃料电池,结构如图所示:
①电极N是
②若该燃料电池消耗11.2 L(标准状况下)BA4,则理论上电路中转移
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请针对元素①-⑨用相应的化学用语回答下列问题:
(1)化学性质最不活泼的元素是____ (填元素符号),非金属性最强的单质是____ (填化学式)。
(2)③、⑤的原子半径较小的是_____ (填元素符号)。
(3)①、②的最高价氧化物的水化物的酸性较强的是____ (填化学式)。
(4)①的最高价氧化物与⑦的最高价氧化物的熔点较高的是____ (填化学式),原因是_____ 。
(5)⑤与⑥金属性较强的是________ (填元素符号),下列表述能证明这一结论的是____ 。
A.单质的熔沸点:⑤>⑥
B.最高价氧化物的水化物的碱性:⑤>⑥
C.单质与水反应的剧烈程度:⑤>⑥
(6)②的简单氢化物的结构式___ ,它与⑧的气态氢化物反应的化学方程式是___ ,该反应生成物的晶体类型为__ 晶体。
族 周期 | IA | 0 | ||||||
1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)化学性质最不活泼的元素是
(2)③、⑤的原子半径较小的是
(3)①、②的最高价氧化物的水化物的酸性较强的是
(4)①的最高价氧化物与⑦的最高价氧化物的熔点较高的是
(5)⑤与⑥金属性较强的是
A.单质的熔沸点:⑤>⑥
B.最高价氧化物的水化物的碱性:⑤>⑥
C.单质与水反应的剧烈程度:⑤>⑥
(6)②的简单氢化物的结构式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
(1)写出各元素的元素符号:Q_______ 、W_______ 、X_______ 、Y_______ 、Z_______ 。
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是_______ (写化学式)。
(3)金属性Y强于X,用原子结构解释原因:_______ ,失电子能力Y大于X。
(4)下列对于Z及其化合物的推断中,正确的是_______ (填序号)。
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
| 元素 | 信息 |
| Q | 在元素周期表中位于第3周期ⅣA族 |
| W | 最高正化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色反应为紫色 |
| Z | 原子结构示意图为 |
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是
(3)金属性Y强于X,用原子结构解释原因:
(4)下列对于Z及其化合物的推断中,正确的是
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,用化学用语回答下列问题:
(1)①-⑩号元素中元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ (均用化学式表示)。
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为_______ (用离子符号和“>”表示)。
(3)②与④可以形成一种温室气体,用电子式表示其形成过程_______ 。
(4)由①③⑩三种元素形成的一种离子化合物的电子式_______ 。
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 4 |
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为
(3)②与④可以形成一种温室气体,用电子式表示其形成过程
(4)由①③⑩三种元素形成的一种离子化合物的电子式
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)A、B、C三种元素按原子半径由大到小的顺序排列为_____ (用元素符号表示)。
(2)G和H的非金属强弱关系为_____ (用元素符号表示)。
(3)G元素与A元素形成的化合物的电子式是_____ 。高温灼烧该化合物时,火焰呈_____ 色。
(4)上表中其单质能广泛用作半导体材料的元素是_____ 。
周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | E | |||||||
| 3 | A | C | D | F | G | R | ||
| 4 | B | H | ||||||
(1)A、B、C三种元素按原子半径由大到小的顺序排列为
(2)G和H的非金属强弱关系为
(3)G元素与A元素形成的化合物的电子式是
(4)上表中其单质能广泛用作半导体材料的元素是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
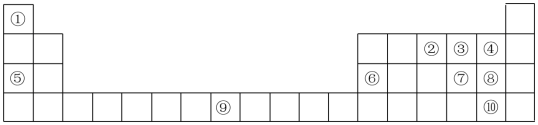
【推荐3】下图为元素周期表的一部分,请参照元①~⑩在表中的位置,回答下列问题:
(1)元素⑩在周期表中的位置是___________ ,⑦的原子结构示意图为___________ 。
(2)④⑤⑥的简单离子半径由大到小的顺序为___________ (用离子符号和“>” 表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是___________ (用化学式表示)。
(4)①和③形成的最简单化合物的电子式为___________ ,② 和⑧形成的化合物中含有化学键类型为___________ 。
(5)用电子式表示⑥和⑨组成的化合物的形成过程:___________ ;⑤的最高价氧化物对应的水化物与⑦的最高价氧化物发生反应的离子方程式为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④⑤⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)①和③形成的最简单化合物的电子式为
(5)用电子式表示⑥和⑨组成的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,针对表中①~⑩元素填空,回答相关问题。
(1)上述元素形成的物质中不存在化学键的是_______ (填元素符号)。
(2)④、⑤、⑨简单离子半径由大到小的顺序_______ (用离子符号表示);②、⑧、⑩最高价氧化物对应水化物的酸性由弱到强_______ (用化学式表示)
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为_______ 。
(4)⑨的低价氧化物和⑩的单质按体积比1:1通入品红溶液中,现象_______ 原因:_______ (用离子方程式表示)
(5)⑥的氧化物可以溶于⑤形成的一种强碱溶液写出该化学方程式_______
(6)证明⑨和⑩两种元素的非金属性强弱,_______ (用离子方程式表示)
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(2)④、⑤、⑨简单离子半径由大到小的顺序
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为
(4)⑨的低价氧化物和⑩的单质按体积比1:1通入品红溶液中,现象
(5)⑥的氧化物可以溶于⑤形成的一种强碱溶液写出该化学方程式
(6)证明⑨和⑩两种元素的非金属性强弱,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表列出了A ~ R 9种元素在周期表中的位置:
请回答下列问题。
(1)这9种元素分别为:A.____ 、B.___ 、C.___ 、D.____ 、E._____ 、F.____ 、G.____ 、H.____ 、R.____ 。其中化学性质最不活泼的是____ (用元素符号作答)。
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_______ 。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为_______ 。(用元素符号表示)
(4)F元素氢化物的化学式是_______ ,该氢化物在常温下与B发生反应的化学方程式是_______ ,所得溶液的pH _______ 7。
(5)H元素与A元素形成的化合物的电子式是___ 。高温灼烧该化合物时,火焰呈___ 色。
(6)G元素最高价氧化物对应的水化物的酸性比H元素最高价氧化物对应的水化物的酸性_____ (“强”或“弱”)。
| 周期 | 族 | ||||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | ||
| 2 | E | F | |||||||
| 3 | A | C | D | G | R | ||||
| 4 | B | H | |||||||
(1)这9种元素分别为:A.
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素与A元素形成的化合物的电子式是
(6)G元素最高价氧化物对应的水化物的酸性比H元素最高价氧化物对应的水化物的酸性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种筒能燃料,分子中含有18个电子,其组成元素与丙相同。
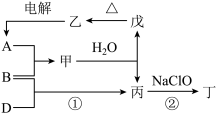
(1)元素X在周期表中的位置是______ ,其简单离子的结构示意图为______ 。
(2)单质B的电子式为______ 。
(3)丙中所含的化学键类型是______ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为______ 。
(5)一定条件下,A与 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为______ 。
| 元素编号 | 元素性质或原子结构信息 |
| X | 第三周期元素中简单离子半径最小的元素 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和所在周期数相等 |

(1)元素X在周期表中的位置是
(2)单质B的电子式为
(3)丙中所含的化学键类型是
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol
 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为(5)一定条件下,A与
 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
您最近一年使用:0次



