为探究某不溶性固体X(仅含四种元素)的成分,设计并完成了如下实验:
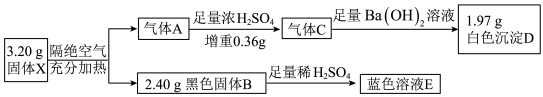
已知气体A是混合物,气体C是纯净物且无色无味。请回答:
(1)盐X中的4种元素是H、O和_______ (填元素符号),
(2)黑色固体B的化学式为_______ 。
(3)该流程中X隔绝空气加热分解的化学方程式为_______ 。
(4)向蓝色溶液E中加入KI溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是CuI,写出该反应的离子方程式_______ 。

已知气体A是混合物,气体C是纯净物且无色无味。请回答:
(1)盐X中的4种元素是H、O和
(2)黑色固体B的化学式为
(3)该流程中X隔绝空气加热分解的化学方程式为
(4)向蓝色溶液E中加入KI溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是CuI,写出该反应的离子方程式
更新时间:2023-03-20 19:04:01
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】某种胃药的有效成分为碳酸钙,测定其中碳酸钙的含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①配制 的稀盐酸和
的稀盐酸和 的
的 溶液各
溶液各
②向一粒研碎后的药片 中加入
中加入 蒸馏水
蒸馏水
③加入 的稀盐酸
的稀盐酸
④用 的
的 溶液仲和过量的稀盐酸,记录所消耗
溶液仲和过量的稀盐酸,记录所消耗 溶液的体积回答下列问题:
溶液的体积回答下列问题:
(1)配制 的稀盐酸用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
的稀盐酸用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有_______ 、_______ 。
(2)配制 的
的 溶液,需称量
溶液,需称量 固体的质量是
固体的质量是_______ g,配制过程中所涉及的下列相关操作正确的是_______ 。
a.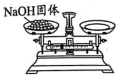 b.
b. 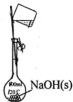 c.
c.  d.
d.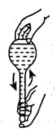
(3)某同学测定消耗的 溶液体积如下,计算这种药片中碳酸钙的质量分数为
溶液体积如下,计算这种药片中碳酸钙的质量分数为_______ 。
①配制
 的稀盐酸和
的稀盐酸和 的
的 溶液各
溶液各
②向一粒研碎后的药片
 中加入
中加入 蒸馏水
蒸馏水③加入
 的稀盐酸
的稀盐酸④用
 的
的 溶液仲和过量的稀盐酸,记录所消耗
溶液仲和过量的稀盐酸,记录所消耗 溶液的体积回答下列问题:
溶液的体积回答下列问题:(1)配制
 的稀盐酸用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
的稀盐酸用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有(2)配制
 的
的 溶液,需称量
溶液,需称量 固体的质量是
固体的质量是a.
 b.
b.  c.
c.  d.
d.
(3)某同学测定消耗的
 溶液体积如下,计算这种药片中碳酸钙的质量分数为
溶液体积如下,计算这种药片中碳酸钙的质量分数为| 测定次数 | 第1次 | 第2次 | 第3次 |
 | 12.90 | 13.10 | 13.00 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】下图是某硫酸试剂瓶标签上的内容:
(1)某化学兴趣小组进行硫酸性质的实验探究时,需要 的稀硫酸,则配制该稀硫酸需要用量筒量取
的稀硫酸,则配制该稀硫酸需要用量筒量取___________  (保留1位小数)该浓硫酸,配制过程中用到的玻璃仪器除了量筒,玻璃棒,烧杯外还需要用到的玻璃仪器有
(保留1位小数)该浓硫酸,配制过程中用到的玻璃仪器除了量筒,玻璃棒,烧杯外还需要用到的玻璃仪器有___________ 。
(2)在下列配制过程示意图中,有错误的是___________ (填序号)。
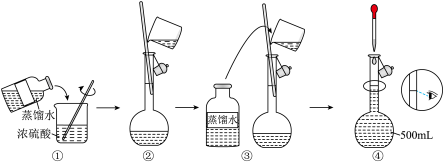
(3)在配制 稀硫酸的过程中,下列情况会引起硫酸的物质的量浓度偏高的是
稀硫酸的过程中,下列情况会引起硫酸的物质的量浓度偏高的是___________ (填序号)。
A.未经冷却趁热将溶液注入容量瓶中进行定容
B.容量瓶洗涤后,未经干燥处理
C.定容时俯视容量瓶刻度线
D.向容量瓶中转移液体时有少量液体溅出
E.用蒸馏水洗涤量筒中的残留液并转移至容量瓶
(4)为中和 溶液后显中性,需要加入
溶液后显中性,需要加入_________  稀硫酸。
稀硫酸。
硫酸化学纯 品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数: 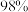 |
(1)某化学兴趣小组进行硫酸性质的实验探究时,需要
 的稀硫酸,则配制该稀硫酸需要用量筒量取
的稀硫酸,则配制该稀硫酸需要用量筒量取 (保留1位小数)该浓硫酸,配制过程中用到的玻璃仪器除了量筒,玻璃棒,烧杯外还需要用到的玻璃仪器有
(保留1位小数)该浓硫酸,配制过程中用到的玻璃仪器除了量筒,玻璃棒,烧杯外还需要用到的玻璃仪器有(2)在下列配制过程示意图中,有错误的是

(3)在配制
 稀硫酸的过程中,下列情况会引起硫酸的物质的量浓度偏高的是
稀硫酸的过程中,下列情况会引起硫酸的物质的量浓度偏高的是A.未经冷却趁热将溶液注入容量瓶中进行定容
B.容量瓶洗涤后,未经干燥处理
C.定容时俯视容量瓶刻度线
D.向容量瓶中转移液体时有少量液体溅出
E.用蒸馏水洗涤量筒中的残留液并转移至容量瓶
(4)为中和
 溶液后显中性,需要加入
溶液后显中性,需要加入 稀硫酸。
稀硫酸。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。___________ 。
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为___________ ,1mol该阴离子中所含的电子总数为___________ mol
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的还原剂为___________ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___________ ?(写出计算过程,保留一位小数,不考虑固体的体积)。
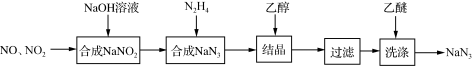
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的还原剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】将 通入微酸性的
通入微酸性的 溶液中,生成
溶液中,生成 和白色沉淀(A)。将白色沉淀(A)与硫酸混合加热最终可制得纳米Cu。
和白色沉淀(A)。将白色沉淀(A)与硫酸混合加热最终可制得纳米Cu。
已知:白色沉淀(A)中含有Cu+及正四面体型离子和三角锥型离子,三种离子物质的量之比为1∶1∶1。
(1)正四面体型结构的离子为___________ (填化学式,下同):三角锥型结构的离子为:___________ 。
(2)写出生成白色沉淀(A)的离子方程式:___________ 。
(3)①理论上纳米Cu的产率为:___________ 。
②若将白色沉淀(A)与硫酸置于密闭容器中反应,则理论上纳米Cu的产率将___________ (填“增大”、“不变”、“减小”),理由为:___________ 。
 通入微酸性的
通入微酸性的 溶液中,生成
溶液中,生成 和白色沉淀(A)。将白色沉淀(A)与硫酸混合加热最终可制得纳米Cu。
和白色沉淀(A)。将白色沉淀(A)与硫酸混合加热最终可制得纳米Cu。已知:白色沉淀(A)中含有Cu+及正四面体型离子和三角锥型离子,三种离子物质的量之比为1∶1∶1。
(1)正四面体型结构的离子为
(2)写出生成白色沉淀(A)的离子方程式:
(3)①理论上纳米Cu的产率为:
②若将白色沉淀(A)与硫酸置于密闭容器中反应,则理论上纳米Cu的产率将
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某课外活动小组甲、乙、丙三位同学进行 胶体的制备实验并检验其性质,实验方案如下:
胶体的制备实验并检验其性质,实验方案如下:
①甲同学的操作:向饱和 溶液中直接加入过量的NaOH溶液。
溶液中直接加入过量的NaOH溶液。
②乙同学的操作:向沸水中滴加饱和 溶液,为了使反应进行充分,长时间煮沸。
溶液,为了使反应进行充分,长时间煮沸。
③丙同学的操作:取一小烧杯,加入40mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
回答下列问题:
(1)你认为哪位同学的制备方法正确:___________ ,生成胶体的化学方程式是___________ 。
(2)甲同学的操作涉及的化学反应方程式为___________ 。
(3)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论:___________ 。
(4) 胶体属于
胶体属于___________ (填“纯净物”“混合物”),向制备的 胶体中逐滴滴加盐酸溶液,先观察到红褐色沉淀,接着沉淀溶解,溶液呈黄色,其离子方程式为
胶体中逐滴滴加盐酸溶液,先观察到红褐色沉淀,接着沉淀溶解,溶液呈黄色,其离子方程式为___________ 。
 胶体的制备实验并检验其性质,实验方案如下:
胶体的制备实验并检验其性质,实验方案如下:①甲同学的操作:向饱和
 溶液中直接加入过量的NaOH溶液。
溶液中直接加入过量的NaOH溶液。②乙同学的操作:向沸水中滴加饱和
 溶液,为了使反应进行充分,长时间煮沸。
溶液,为了使反应进行充分,长时间煮沸。③丙同学的操作:取一小烧杯,加入40mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
 饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
饱和溶液,继续煮沸至混合液呈红褐色,停止加热。回答下列问题:
(1)你认为哪位同学的制备方法正确:
(2)甲同学的操作涉及的化学反应方程式为
(3)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论:
(4)
 胶体属于
胶体属于 胶体中逐滴滴加盐酸溶液,先观察到红褐色沉淀,接着沉淀溶解,溶液呈黄色,其离子方程式为
胶体中逐滴滴加盐酸溶液,先观察到红褐色沉淀,接着沉淀溶解,溶液呈黄色,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某学习小组为研究铁及其化合物的性质,做了以下探究实验并通过下列途径成功制得纳米铁粉和Na2FeO4,已知Na2FeO4能起到净水和杀菌的作用。
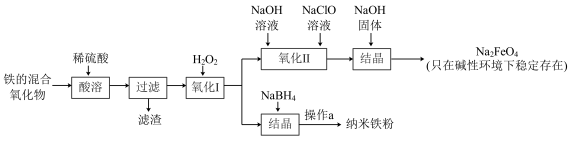
(1)过滤所用到的玻璃仪器有________ ;氧化Ⅰ反应的离子方程式为_________ 。
(2)用实验证明“酸溶”所得的酸性溶液中既含Fe3+,还含Fe2+_______ 。
(3)氧化Ⅱ过程需要高浓度NaClO溶液,可用Cl2与NaOH溶液反应制备:
①Cl2与NaOH溶液反应的还原产物是________ 。
②Na2FeO4中铁元素的化合价为______ ,1mol Na2FeO4与____ mol NaClO氧化消毒能力相当(用得电子数目多少衡量氧化消毒能力强弱)。

(1)过滤所用到的玻璃仪器有
(2)用实验证明“酸溶”所得的酸性溶液中既含Fe3+,还含Fe2+
(3)氧化Ⅱ过程需要高浓度NaClO溶液,可用Cl2与NaOH溶液反应制备:
①Cl2与NaOH溶液反应的还原产物是
②Na2FeO4中铁元素的化合价为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】研究氮的循环和转化对生产、生活有重要的价值。
(1)氨是重要的化工原料,某工厂用氨制硝酸和铵盐的流程如图所示:
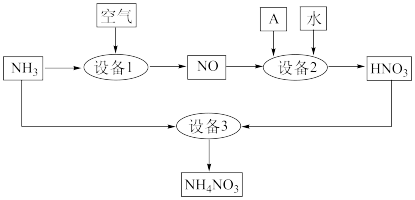
设备1中发生反应的化学方程式为____ ,设备2中通入的物质A是___ 。
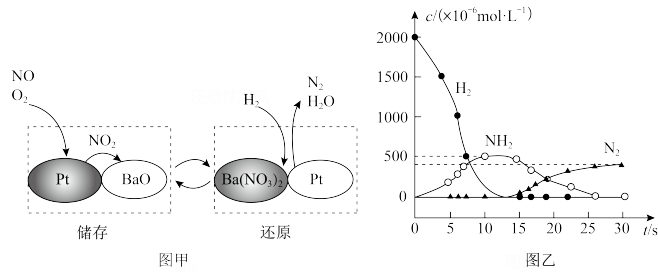
(2)NSR(NOx储存还原),NO储存和还原在不同时段交替进行,如图甲所示。
①NO储存转化为Ba(NO3)2过程中,参加反应NO和O2的物质的量之比为____ 。
②H2还原Ba(NO3)2的过程分两步进行,图乙表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为_____ 。
(3)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:
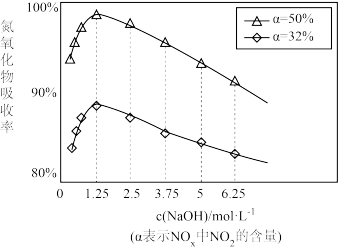
用NaOH溶液吸收氮氧化物的最佳条件为:α=____ ,c(NaOH)=____ 。
②若一定体积的NOx被250mL2mol•L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为_____ 。
(1)氨是重要的化工原料,某工厂用氨制硝酸和铵盐的流程如图所示:

设备1中发生反应的化学方程式为
(2)NSR(NOx储存还原),NO储存和还原在不同时段交替进行,如图甲所示。
①NO储存转化为Ba(NO3)2过程中,参加反应NO和O2的物质的量之比为
②H2还原Ba(NO3)2的过程分两步进行,图乙表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为

(3)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:

用NaOH溶液吸收氮氧化物的最佳条件为:α=
②若一定体积的NOx被250mL2mol•L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】氯气在实验室中制备较为方便,并可用于制备 等一些含氯化合物。
等一些含氯化合物。
二氯化二硫 常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等,
常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等, 沸点为
沸点为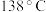 ,遇水会发生化学反应。向熔融的硫中通入氯气即可生成
,遇水会发生化学反应。向熔融的硫中通入氯气即可生成 。实验室用S和
。实验室用S和 制备
制备 的装置如图(部分夹持装置已略去)。
的装置如图(部分夹持装置已略去)。
1.反应前通入 的作用是
的作用是___________ 。
2.装置B和D中的试剂分别是___________。
3.本实验装置有一处不足,若要改进,应将装置___________之间加一个球形干燥管。
4. 遇水会生成
遇水会生成 、一种强酸和一种淡黄色固体单质,该反应的化学方程式为
、一种强酸和一种淡黄色固体单质,该反应的化学方程式为___________ ,反应中每转移 电子,生成的
电子,生成的 的质量为
的质量为___________ g。
 等一些含氯化合物。
等一些含氯化合物。二氯化二硫
 常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等,
常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等, 沸点为
沸点为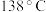 ,遇水会发生化学反应。向熔融的硫中通入氯气即可生成
,遇水会发生化学反应。向熔融的硫中通入氯气即可生成 。实验室用S和
。实验室用S和 制备
制备 的装置如图(部分夹持装置已略去)。
的装置如图(部分夹持装置已略去)。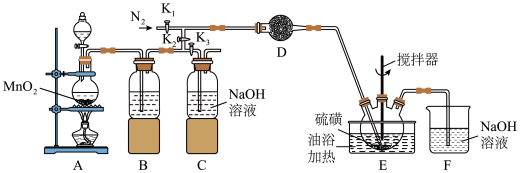
1.反应前通入
 的作用是
的作用是2.装置B和D中的试剂分别是___________。
A.饱和食盐水、无水 | B.浓硫酸、碱石灰 |
C.饱和 溶液、 溶液、 | D.饱和食盐水、无水 |
A. | B.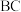 | C.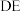 | D. |
 遇水会生成
遇水会生成 、一种强酸和一种淡黄色固体单质,该反应的化学方程式为
、一种强酸和一种淡黄色固体单质,该反应的化学方程式为 电子,生成的
电子,生成的 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。
(1)硝酸工业的尾气(含NO、NO2)可用石灰乳吸收,同时得到用途广泛的Ca(NO2)2,反应为 。部分工业流程如图:
。部分工业流程如图:
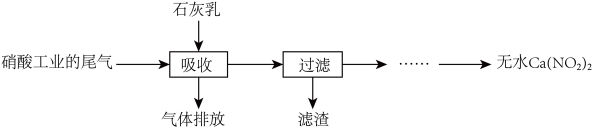
生产中需控制NO和NO2的物质的量之比接近1:1的原因________________ 。
(2)已知Ca(NO2)2溶液遇酸会发生分解,产生NO气体,写出Ca(NO2)2和稀硫酸反应的化学方程式________________ 。
(3)取xg Ca(NO2)2样品加过量的稀硫酸,产生标状下yL气体,则该样品的纯度是________ 。(结果保留3位有效数字)
(1)硝酸工业的尾气(含NO、NO2)可用石灰乳吸收,同时得到用途广泛的Ca(NO2)2,反应为
 。部分工业流程如图:
。部分工业流程如图:
生产中需控制NO和NO2的物质的量之比接近1:1的原因
(2)已知Ca(NO2)2溶液遇酸会发生分解,产生NO气体,写出Ca(NO2)2和稀硫酸反应的化学方程式
(3)取xg Ca(NO2)2样品加过量的稀硫酸,产生标状下yL气体,则该样品的纯度是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐和CO2、H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
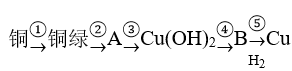
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?____________________ 。
(2)请写出铜绿与盐酸反应的化学方程式___________________________ 。
(3)写出B的化学式______________ 。
(4)上述转化过程中属于化合反应的是_______ (填序号)。
(5)写出反应①的化学方程式____________________________________ 。
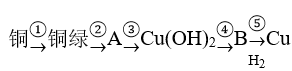
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?
(2)请写出铜绿与盐酸反应的化学方程式
(3)写出B的化学式
(4)上述转化过程中属于化合反应的是
(5)写出反应①的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下图为A-G(初中常见的物质)的转化关系。其中A天然气的主要成分。D为单质。
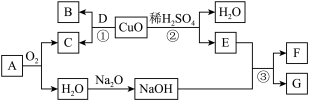
根据以上信息回答下列问题。
(1)写出A的化学式_______ ,其常见用途为_______ (任写一条)。
(2)写出反应①化学方程式_______ ,该反应属于_______ 反应(填基本反应类型)。
(3)反应的②现象为_______ 。
(4)写出反应③的化学方程式_______ 。

根据以上信息回答下列问题。
(1)写出A的化学式
(2)写出反应①化学方程式
(3)反应的②现象为
(4)写出反应③的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某小组设计实验证明乙醇和钠反应产生氢气,并探究氧化铜的还原产物。
已知:① 。
。
②红色粉末 在酸性条件下发生歧化反应:
在酸性条件下发生歧化反应: 。
。
装置如图所示:
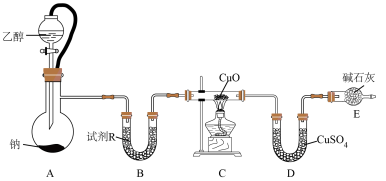
回答下列问题:
(1)试剂R最好选择__________(填字母)。
(2)装置E的作用是__________ 。
(3)实验完毕后,为了探究C中红色粉末是否含有 ,设计下列两种方案:
,设计下列两种方案:
方案1:取少量红色粉末于试管,加入足量溶液M,充分振荡,若溶液变蓝色,则红色粉末一定含 ;
;
方案2:取ag红色粉末,在加热条件下通入足量氢气,充分反应后,冷却、称重,红色固体质量为xg。
①方案1中M可能是__________ 。
A.稀硝酸 B.稀硫酸 C.浓硫酸 D.浓硝酸
②方案2中,当
__________ 时,红色粉末全部是 。
。
(4)分析与讨论。
①CuO被 、
、 、CO等还原可能生成
、CO等还原可能生成 或Cu,生成
或Cu,生成 的可能原因是
的可能原因是__________ 。
A.通入 量不足 B.
量不足 B. 与CuO接触充分
与CuO接触充分
C.温度较低 D.温度过高
②若缺少装置B,C中黑色粉末变红色,D中白色粉末变蓝色,不能肯定A中一定生成了 ,用化学方程式表达其理由
,用化学方程式表达其理由__________ 。
已知:①
 。
。②红色粉末
 在酸性条件下发生歧化反应:
在酸性条件下发生歧化反应: 。
。装置如图所示:

回答下列问题:
(1)试剂R最好选择__________(填字母)。
| A.碱石灰 | B.无水氯化钙 | C.五氧化二磷 | D.硫酸镁 |
(3)实验完毕后,为了探究C中红色粉末是否含有
 ,设计下列两种方案:
,设计下列两种方案:方案1:取少量红色粉末于试管,加入足量溶液M,充分振荡,若溶液变蓝色,则红色粉末一定含
 ;
;方案2:取ag红色粉末,在加热条件下通入足量氢气,充分反应后,冷却、称重,红色固体质量为xg。
①方案1中M可能是
A.稀硝酸 B.稀硫酸 C.浓硫酸 D.浓硝酸
②方案2中,当

 。
。(4)分析与讨论。
①CuO被
 、
、 、CO等还原可能生成
、CO等还原可能生成 或Cu,生成
或Cu,生成 的可能原因是
的可能原因是A.通入
 量不足 B.
量不足 B. 与CuO接触充分
与CuO接触充分C.温度较低 D.温度过高
②若缺少装置B,C中黑色粉末变红色,D中白色粉末变蓝色,不能肯定A中一定生成了
 ,用化学方程式表达其理由
,用化学方程式表达其理由
您最近一年使用:0次



