A、B、C、D、E、F为短周期原子序数依次增大的主族元素,B最外层电子数是内层电子数的3倍,C在短周期元素中原子半径最大,E的最高正价与最低负价代数和为4,A、B常温下能形成两种液态化合物A2B和A2B2,D元素的单质常用来制造太阳能电池。请用化学用语回答下列问题:
(1)D元素在周期表中的位置为_____ ;B、D两种元素的最简单氢化物中,稳定性较强的氢化物的结构式是_____ ,D、E两种元素的最高价氧化物对应的水化物中,酸性较弱的是_____ (填化学式)。
(2)用电子式表示C2E的形成过程____ 。
(3)B、C、E形成的简单离子半径从大到小的顺序为_____ (用离子符号表示)。
(4)写出D的最高价氧化物与C的最高价氧化物对应水化物反应的离子方程式:_____ 。
(5)等物质的量的EB2与F的单质通入品红溶液将失去漂白性,反应的离子方程式为:_____ 。
(6)非金属性强弱大小关系E____ F(填写“大于”或“小于”),下列表述中不能证明这一事实的是_____ (填字母)。
a.E的氢化物比F的氢化物水溶液酸性弱
b.F的氧化物对应的水化物的酸性强于E的氧化物对应的水化物的酸性
c.F的单质能将E的单质从其钠盐溶液中置换出来
d.F的简单阴离子的还原性比E的简单阴离子的还原性弱
e.铁与F的单质反应生成+3价铁,而与E的单质反应生成+2铁
(1)D元素在周期表中的位置为
(2)用电子式表示C2E的形成过程
(3)B、C、E形成的简单离子半径从大到小的顺序为
(4)写出D的最高价氧化物与C的最高价氧化物对应水化物反应的离子方程式:
(5)等物质的量的EB2与F的单质通入品红溶液将失去漂白性,反应的离子方程式为:
(6)非金属性强弱大小关系E
a.E的氢化物比F的氢化物水溶液酸性弱
b.F的氧化物对应的水化物的酸性强于E的氧化物对应的水化物的酸性
c.F的单质能将E的单质从其钠盐溶液中置换出来
d.F的简单阴离子的还原性比E的简单阴离子的还原性弱
e.铁与F的单质反应生成+3价铁,而与E的单质反应生成+2铁
更新时间:2023-03-27 09:47:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有5种短周期元素的原子序数按E、D、B、A、C 的顺序依次增大; A、C 同周期,B、C同主族;A 与B 可形成离子化合物A2B,A2B 中阴阳离子的电子层结构完全相同,且电子总数为30;D 和E可形成4 核10 电子的分子。试回答下列问题:
(1)写出这5种元素的名称: A______ B______ C______ D______ E______
(2)写出下列物质的电子式:
①D 元素形成的单质___________ ②B 与E 形成的四原子化合物________
③A.B、E 形成的化合物__________ ④D、E 形成的简单化合物__________
(3)B、D、E形成的原子个数3:2:4的盐的化学式为_______ ,类别属于______ 化合物(填离子或共价),含有的化学键类型__________ 。
(1)写出这5种元素的名称: A
(2)写出下列物质的电子式:
①D 元素形成的单质
③A.B、E 形成的化合物
(3)B、D、E形成的原子个数3:2:4的盐的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】某污水处理工艺中, 的转化途径如下图所示:
的转化途径如下图所示:

完成下列填空:
(1)上述转化过程_______ (选填“属于”或“不属于”)氮的固定。N原子核外能量最高的电子有_______ 个,这些电子_______ (选填编号)
a.所处的电子亚层相同 b.自旋方向相同
c.占据的轨道相同 d.运动状态相同
(2)从原子结构角度解释NO分子中氮元素化合价呈正价的原因_______ 。
(3) 中氢元素的化合价为
中氢元素的化合价为 价,写出
价,写出 的结构式
的结构式_______ ,其所含共价键的类型为_______ ;若其分子的极性与 相同,则它是
相同,则它是_______ (选填“极性”或“非极性”)分子。
(4)配平离子方程式:_______ 。
_______NO+_______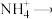 _______
_______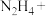 _______
_______ _______
_______
若反应所得的氧化产物比还原产物多1.5mol,则该反应转移的电子为_______ mol。
 的转化途径如下图所示:
的转化途径如下图所示:
完成下列填空:
(1)上述转化过程
a.所处的电子亚层相同 b.自旋方向相同
c.占据的轨道相同 d.运动状态相同
(2)从原子结构角度解释NO分子中氮元素化合价呈正价的原因
(3)
 中氢元素的化合价为
中氢元素的化合价为 价,写出
价,写出 的结构式
的结构式 相同,则它是
相同,则它是(4)配平离子方程式:
_______NO+_______
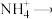 _______
_______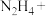 _______
_______ _______
_______
若反应所得的氧化产物比还原产物多1.5mol,则该反应转移的电子为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.如图所示是NH3的两个性质实验

(1)实验一是氨气的喷泉实验,圆底烧瓶中充满干燥的氨气,请写出氨气的电子式_______ ,氨气的结构式_______ ,氨气分子的空间构型是_______ 。
(2)实验开始前,胶头滴管充满水,活塞关闭。请简述引发喷泉的实验操作_______ ,形成喷泉的原理是_______ ,请用化学用语解释喷泉呈红色的原因_______ 。
(3)实验二体现了浓氨水具有的性质是_______ 、_______ 。请写出能够解释形成白烟的化学方程式_______ 。
Ⅱ.下列装置用于实验室中制取干燥氨气的实验



(4)甲、 乙、丙、丁操作是否正确?正确请打“√”,错误请打“×”。错误请简要说明理由。
①用装置甲制备氨气_______
②用装置乙除去氨气中的少量水_______
③用装置丙收集氨气_______
④用装置丁吸收多余的氨气_______

(1)实验一是氨气的喷泉实验,圆底烧瓶中充满干燥的氨气,请写出氨气的电子式
(2)实验开始前,胶头滴管充满水,活塞关闭。请简述引发喷泉的实验操作
(3)实验二体现了浓氨水具有的性质是
Ⅱ.下列装置用于实验室中制取干燥氨气的实验



(4)甲、 乙、丙、丁操作是否正确?正确请打“√”,错误请打“×”。错误请简要说明理由。
①用装置甲制备氨气
②用装置乙除去氨气中的少量水
③用装置丙收集氨气
④用装置丁吸收多余的氨气
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化硫(化学式:SO2)广泛地用于葡萄酒的酿造工艺中,具有抗氧化和杀菌的作用。
(1)实验室常用亚硫酸钠固体和浓硫酸反应制备SO2,其化学方程式为_____________ 。
(2)如图是有关二氧化硫部分性质的实验装置图:
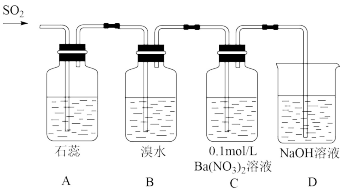
A装置中的现象证明SO2有_____ (填序号),B装置中的现象证明SO2有____ (填序号)。
a、漂白性 b、酸性氧化物性质 c、还原性 d、氧化性
(3)一段时间后C装置中会出现白色沉淀,为确定其成分,某学习小组进行了以下实验探究。
①查阅资料:25℃时,H2SO3电离常数Ka1=1.54×10-2,Ka2=1.02×10-7;Ksp(BaSO3)=5.3×10-7;饱和亚硫酸溶液的pH约为1,其中c(H2SO3)约为1.25mol/L。
小组同学通过计算排除了白色沉淀为BaSO3可能性,计算过程的关键数据如下:
饱和亚硫酸溶液中c(SO2)=_________ (保留2位有效数字);
Q(BaSO3)_______ Ksp(BaSO3) (填“>”“<”或“=”)。
②判断并检验,确定该沉淀为BaSO4
③为进一步探究C装置的溶液中什么微粒将SO2氧化,小组同学提出以下猜想:
猜想a:溶液中有氧气,将SO2氧化,继而生成BaSO4。
猜想b:____________________________________ (用离子方程式表示)
设计实验、验证猜想。
实验过程:
实验1、实验2中煮沸、油覆的目的是_______________________
④实验数据如下:

小组同学通过对比实验1、2、4三组实验的pH变化图像,得出结论:_______________________ 。综合以上pH变化数据,你还可得出什么结论?____________________________ 。
(1)实验室常用亚硫酸钠固体和浓硫酸反应制备SO2,其化学方程式为
(2)如图是有关二氧化硫部分性质的实验装置图:

A装置中的现象证明SO2有
a、漂白性 b、酸性氧化物性质 c、还原性 d、氧化性
(3)一段时间后C装置中会出现白色沉淀,为确定其成分,某学习小组进行了以下实验探究。
①查阅资料:25℃时,H2SO3电离常数Ka1=1.54×10-2,Ka2=1.02×10-7;Ksp(BaSO3)=5.3×10-7;饱和亚硫酸溶液的pH约为1,其中c(H2SO3)约为1.25mol/L。
小组同学通过计算排除了白色沉淀为BaSO3可能性,计算过程的关键数据如下:
饱和亚硫酸溶液中c(SO2)=
Q(BaSO3)
②判断并检验,确定该沉淀为BaSO4
③为进一步探究C装置的溶液中什么微粒将SO2氧化,小组同学提出以下猜想:
猜想a:溶液中有氧气,将SO2氧化,继而生成BaSO4。
猜想b:
设计实验、验证猜想。
实验过程:
实验1 | 实验2 | 实验3 | 实验4 | |
步 骤 | 在a烧杯中加入煮沸的25ml 0.1mol/L BaCl2溶液,再加入食用油覆盖,冷却至室温 | 在b烧杯中加入煮沸的25ml 0.1mol/L Ba(NO3)2溶液,再加入食用油覆盖,冷却至室温 | 在c烧杯中加入未煮沸的25ml 0.1mol/L BaCl2溶液 | 在d烧杯中加入未煮沸的25ml 0.1mol/L Ba(NO3)2溶液 |
| 在a、b、c、d四个烧杯中均放入pH传感器,然后通入纯净的SO2气体 | ||||
④实验数据如下:

小组同学通过对比实验1、2、4三组实验的pH变化图像,得出结论:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】碲(Te)是半导体、红外探测等领域的重要战略元素。从阳极泥或冶炼烟尘中提取的粗二氧化碲中含有SeO2、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。

回答下列问题:
(1)“浸出”步骤中,碲和硒两种元素分别转化为TeCl4和SeCl4。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是_______ 。
(2)粗二氧化碲与浓盐酸反应生成TeCl4的化学方程式为_______ 。
(3)“净化”步骤中产生的滤渣主要含_______ (写化学式)和少量硒单质。
(4)化学反应的吉布斯自由能变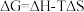 。SO2还原TeCl4和SeCl4的∆G随温度
。SO2还原TeCl4和SeCl4的∆G随温度 的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过
的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过_______ K,该步骤控制在此温度以下的原因是_______ 。

(5)“还原”步骤中产生碲单质的化学方程式为_______ 。
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂 进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是
进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是_______ (填标号)。
A.铁粉 B.氢气 C.硫化钠

回答下列问题:
(1)“浸出”步骤中,碲和硒两种元素分别转化为TeCl4和SeCl4。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
(2)粗二氧化碲与浓盐酸反应生成TeCl4的化学方程式为
(3)“净化”步骤中产生的滤渣主要含
(4)化学反应的吉布斯自由能变
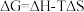 。SO2还原TeCl4和SeCl4的∆G随温度
。SO2还原TeCl4和SeCl4的∆G随温度 的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过
的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过
(5)“还原”步骤中产生碲单质的化学方程式为
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂
 进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是
进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是A.铁粉 B.氢气 C.硫化钠
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭。甲同学用Na2SO4制备SO2,并验证SO2的部分性质。设计了如下实验步骤及装置:
[实验步骤]
I.实验装置的气密性,加入试剂,并按顺序组装仪器。
II.关闭活塞a再打开旋塞b,分次加入酸M。
III.待试管B中充分反应后,打开活塞a,从长颈漏斗加入适量盐酸。
[实验现象]
打开活塞a前,C中溶液有少量固体生成,长导管口有气泡。D中溶液有大量固体生成;当C中长导管口无气泡后,D中液面上气体逐渐变为浅黄绿色。
回答下列问题:
(1)盛放酸M的仪器名称是___________________ 。
(2)查阅资料:①常温常压下,在1L水中大约最多能溶40L SO2,②H2SO3是中强酸。与亚硫酸钠反应制SO2的酸A最好用_________ (填标号)。
a.稀盐酸 b.pH=1的硫酸 c.2mol/L的硝酸 d.12mol/L的硫酸
(3)实验过程中,D中发生反应的离子方程式为_______ 、________________ 。
(4)实验步骤III的目的是__________________________________________________ 。
【问题探究】
(5)乙同学认为:
①甲同学的实验步骤设计不严谨,所以装置C中的少量固体可能是:亚硫酸钡、硫酸钡或亚硫酸钡和硫酸钡。为确定C中固体的成分,乙同学在不改变实验装置的条件下,只对实验步骤加以改进便能准确判断出装置C中的固体的成分。乙同学对实验步骤改进的具体操作是___________________________________ 。
②甲同学的实验装置有明显不足,你认为不足之处是_____________________________ 。

[实验步骤]
I.实验装置的气密性,加入试剂,并按顺序组装仪器。
II.关闭活塞a再打开旋塞b,分次加入酸M。
III.待试管B中充分反应后,打开活塞a,从长颈漏斗加入适量盐酸。
[实验现象]
打开活塞a前,C中溶液有少量固体生成,长导管口有气泡。D中溶液有大量固体生成;当C中长导管口无气泡后,D中液面上气体逐渐变为浅黄绿色。
回答下列问题:
(1)盛放酸M的仪器名称是
(2)查阅资料:①常温常压下,在1L水中大约最多能溶40L SO2,②H2SO3是中强酸。与亚硫酸钠反应制SO2的酸A最好用
a.稀盐酸 b.pH=1的硫酸 c.2mol/L的硝酸 d.12mol/L的硫酸
(3)实验过程中,D中发生反应的离子方程式为
(4)实验步骤III的目的是
【问题探究】
(5)乙同学认为:
①甲同学的实验步骤设计不严谨,所以装置C中的少量固体可能是:亚硫酸钡、硫酸钡或亚硫酸钡和硫酸钡。为确定C中固体的成分,乙同学在不改变实验装置的条件下,只对实验步骤加以改进便能准确判断出装置C中的固体的成分。乙同学对实验步骤改进的具体操作是
②甲同学的实验装置有明显不足,你认为不足之处是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下图所示。
A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。

请填空:
(1)形成单质A的原子的结构示意图为______ ,它的最高化合价为______ 。
(2)B的化学式(分子式)为______ ,B的晶体类型为______ 。B和碳反应生成A和E的化学方程式是______ 。
(3)C的化学式(分子式)为______ ,D的化学式(分子式)为______ 。
A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。

请填空:
(1)形成单质A的原子的结构示意图为
(2)B的化学式(分子式)为
(3)C的化学式(分子式)为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,A是单质,B是A的氧化物。它们有如图反应关系:
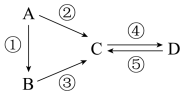
(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18g/mol,D俗称小苏打。则C的化学式为___________ ,写出物质B与 反应的化学方程式
反应的化学方程式___________ ,由D和澄清石灰水可得到C,写出该反应的离子方程式___________ 。
(2)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成___________ ,反应①②③④⑤中,属于氧化还原反应的有___________ (填序号),写出D转化为C的离子方程式___________ 。
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为___________ ;若C、D组成元素相同,则C转化为D的离子方程式为___________ ,在D中滴入氢氧化钠溶液,一段时间内观察到的现象是___________ 。

(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18g/mol,D俗称小苏打。则C的化学式为
 反应的化学方程式
反应的化学方程式(2)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】六氟磷酸锂(LiPF6)具有良好的导电性与电化学稳定性能,常作锂离子电池的电解质。LiPF6极易溶于水,可溶于乙醇等有机溶剂,极易吸水潮解,热稳定性差。实验室制备LiPF6的实验装置如图:
i.在氮气保护的手套箱中,准确称取26.0g干燥LiF固体以及过量PCl5固体,均倒入聚四氟乙烯材质的反应器中,再往其中逐渐加入乙腈,至PCl5充分溶解。
ii.往装置中通一段时间N2,以排出其中空气,关闭K1,加热NaHF2,将生成的HF气体通入反应器中,同时搅拌混合其中的物料。
iii.通过往反应器所处的冷浴槽中调控0~10℃的低温。6~8h后终止反应,继续通N2再关闭加热炉保持通N2一段时间。
iv.打开反应器,对反应后的物料进行过滤,滤液用一个聚乙烯材质的塑料瓶接收,密封后拿出手套箱,置于-18~5℃环境中低温结晶。在氮气保护下,过滤出结晶,经40~50℃真空干燥,最终得到产品140.6g。
回答下列问题:
(1)反应装置选用聚四氟乙烯材质容器,不能用玻璃容器,原因是______ (用化学方程式表示)。
(2)NaHF2加热分解的化学方程式为______ 。
(3)干燥塔的作用为______ 。
(4)NaOH溶液的作用为______ 。
(5)已知合成LiPF6的反应为 ,则生成PF5的化学方程式为
,则生成PF5的化学方程式为______ 。
(6)反应结束后,通入氮气的目的是______ 。
(7)本实验所得六氟磷酸锂的产率为______ %(保留三位有效数字)。

i.在氮气保护的手套箱中,准确称取26.0g干燥LiF固体以及过量PCl5固体,均倒入聚四氟乙烯材质的反应器中,再往其中逐渐加入乙腈,至PCl5充分溶解。
ii.往装置中通一段时间N2,以排出其中空气,关闭K1,加热NaHF2,将生成的HF气体通入反应器中,同时搅拌混合其中的物料。
iii.通过往反应器所处的冷浴槽中调控0~10℃的低温。6~8h后终止反应,继续通N2再关闭加热炉保持通N2一段时间。
iv.打开反应器,对反应后的物料进行过滤,滤液用一个聚乙烯材质的塑料瓶接收,密封后拿出手套箱,置于-18~5℃环境中低温结晶。在氮气保护下,过滤出结晶,经40~50℃真空干燥,最终得到产品140.6g。
回答下列问题:
(1)反应装置选用聚四氟乙烯材质容器,不能用玻璃容器,原因是
(2)NaHF2加热分解的化学方程式为
(3)干燥塔的作用为
(4)NaOH溶液的作用为
(5)已知合成LiPF6的反应为
 ,则生成PF5的化学方程式为
,则生成PF5的化学方程式为(6)反应结束后,通入氮气的目的是
(7)本实验所得六氟磷酸锂的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、Q、R、T、U分别代表原子数依次增大的短周期主族元素,在周期表的短周期在族元素中,X的原子半径最小,X与R的最外层电子数相等;Y的内层电子数是最外层电子数的一半,U的最高化合价和最低化合价的代数和为6;Z与Q相邻,两者原子序数之和为15;R和Q可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
(1)Z元素在周期表中的位置是_______ 。
(2)Q、R、T三种元素的简单离子半径由小到大的顺序为_______ (填离子符号)。
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)下列可以判断R和T的金属性强弱的是_______。
(5)Z元素对应的最高价氧化物对应的水化物的化合物类型是_______ 。(填“离子化合物”或“共价化合物”):Z2X4的电子式是_______ 。
(6)在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6mol/L盐酸100mL,使天平达到平衡。分别向两烧杯加入均不超过5g的镁和T,若要使其充分反应后天平仍然保持平衡,则加入的镁和T的质量之比是_______ 。
(1)Z元素在周期表中的位置是
(2)Q、R、T三种元素的简单离子半径由小到大的顺序为
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为
(4)下列可以判断R和T的金属性强弱的是_______。
| A.单质的熔点:R比T低 |
| B.单质与酸反应时,失电子数R比T少 |
| C.单质与水反应:R比T更易 |
| D.最高价氧化物对应水化物的碱性:R比T强 |
(5)Z元素对应的最高价氧化物对应的水化物的化合物类型是
(6)在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6mol/L盐酸100mL,使天平达到平衡。分别向两烧杯加入均不超过5g的镁和T,若要使其充分反应后天平仍然保持平衡,则加入的镁和T的质量之比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了部分元素在周期表中的位置:

回答下列问题:
(1)写出元素h在元素周期表中的位置:___________ 。
(2)b的气态氢化物的电子式为___________ 。
(3)e、f、j三种元素最高价氧化物对应的水化物的碱性由强到弱依次为___________ (填化学式)。
(4)设计一个实验方案,比较h、k单质氧化性的强弱___________ 。
(5)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。
①预测Ga的化学性质并填写下表:
以上预测都是依据___________ 。
②氮化镓(GaN)材料的研究与应用是目前全球半导体研究的前沿和热点。工业上用含铁酸镓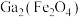 矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的GaN。写出
矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的GaN。写出 用硫酸浸出时发生反应的离子方程式为
用硫酸浸出时发生反应的离子方程式为___________ 。

回答下列问题:
(1)写出元素h在元素周期表中的位置:
(2)b的气态氢化物的电子式为
(3)e、f、j三种元素最高价氧化物对应的水化物的碱性由强到弱依次为
(4)设计一个实验方案,比较h、k单质氧化性的强弱
(5)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。
①预测Ga的化学性质并填写下表:
| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
| Ga能与 | |
| Ga能与 | 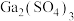 、 、 |
| Ga能与NaOH溶液反应 |
②氮化镓(GaN)材料的研究与应用是目前全球半导体研究的前沿和热点。工业上用含铁酸镓
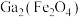 矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的GaN。写出
矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的GaN。写出 用硫酸浸出时发生反应的离子方程式为
用硫酸浸出时发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)化学性质最稳定的元素是_______ (填元素名称),非金属性最强的元素是_______ (填元素符号)。
(2)图中标出的元素的最高价氧化物对应的水化物中,碱性最强的是_______ (用化学式回答),写出该水化物与③的最高价氧化物的水化物反应的离子方程式:_______ 。
(3)①与④可形成的某种化合物,每个分子含有18个电子,该化合物的化学式为:_______ 。
(4)⑤与⑦形成的化合物中化学键类型为_______ ,用电子式表示该化合物的形成过程:_______ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)图中标出的元素的最高价氧化物对应的水化物中,碱性最强的是
(3)①与④可形成的某种化合物,每个分子含有18个电子,该化合物的化学式为:
(4)⑤与⑦形成的化合物中化学键类型为
您最近一年使用:0次



