高锰酸钾是强氧化剂,用途十分广泛。
I.某化学兴趣小组拟以绿色的锰酸钾(K2MnO4)碱性溶液为主要原料在实验室制备KMnO4实验装置(固定和加热装置已省略)如下:
(1)仪器b的名称是_______ ,使用a的优点是_______ ,单向阀(只允许气体从左流向右)可以起到的作用是_______ 。
(2)如图安装好装置后,应先进行的操作是_______ 。
(3)装置B中生成KMnO4的离子方程式为_______ 。
Ⅱ.利用KMnO4标准溶液测定某FeC2O4晶体样品的纯度[样品中含有草酸铵(NH4)2C2O4杂质]。
步骤1:称取m g FeC2O4晶体样品并溶于稀H2SO4中,配成250mL溶液:
步骤2:取上述溶液25.00mL,用cmol/LKMnO4标准溶液滴定至终点:
步骤3:向反应后溶液中加入过量铜粉,充分反应后,过滤、洗涤,将滤液和洗涤液全部收集到锥形瓶中,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗KMnO4溶液VmL。
(4)步骤2中KMnO4溶液除与Fe2+发生反应外,还与H2C2O4发生氧化还原反应,写出其与H2C2O4反应的离子方程式_______ 。
(5)m g FeC2O4晶体样品的纯度为_______ (用含c、V的式子表示,不必化简),若步骤1配制溶液时在空气中放置时间过长,则测定结果将_______ (填 “偏高”、 “偏低“或“无影响”)。
I.某化学兴趣小组拟以绿色的锰酸钾(K2MnO4)碱性溶液为主要原料在实验室制备KMnO4实验装置(固定和加热装置已省略)如下:
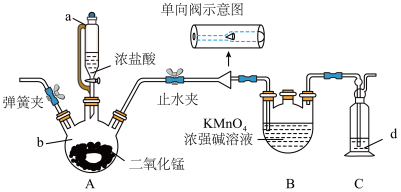
(1)仪器b的名称是
(2)如图安装好装置后,应先进行的操作是
(3)装置B中生成KMnO4的离子方程式为
Ⅱ.利用KMnO4标准溶液测定某FeC2O4晶体样品的纯度[样品中含有草酸铵(NH4)2C2O4杂质]。
步骤1:称取m g FeC2O4晶体样品并溶于稀H2SO4中,配成250mL溶液:
步骤2:取上述溶液25.00mL,用cmol/LKMnO4标准溶液滴定至终点:
步骤3:向反应后溶液中加入过量铜粉,充分反应后,过滤、洗涤,将滤液和洗涤液全部收集到锥形瓶中,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗KMnO4溶液VmL。
(4)步骤2中KMnO4溶液除与Fe2+发生反应外,还与H2C2O4发生氧化还原反应,写出其与H2C2O4反应的离子方程式
(5)m g FeC2O4晶体样品的纯度为
2023·陕西汉中·二模 查看更多[2]
更新时间:2023-04-17 14:05:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.我国的青海省有许多盐湖盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用。粗盐中含Ca2+、Mg2+、SO42-以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯:
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。
(1)以下操作顺序不合理的是_______ 。
A.②⑤④③① B.④⑤②①③
C.⑤②④①③ D.⑤④②①③
(2)步骤①中所用的玻璃仪器有烧杯、______________ 、_____________ 。
(3)通过步骤①中过滤后的滤液,检验SO42-是否除尽的操作方法是__________
Ⅱ.碘是人体所需的必需元素,海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海洋植物中提取碘的流程如下:











 ―→
―→
(1)上述过程灼烧海藻是在____________ (填仪器名称)中进行。
(2)上述步骤②中是加入了氯水,利用氯水中的Cl2把I-氧化为I2,请写出该反应的离子方程式_____________ 。
(3)上述步骤③中加入了CCl4后进行振荡,振荡后静置分层,上层______ 色,下层_______ 色。
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。
(1)以下操作顺序不合理的是
A.②⑤④③① B.④⑤②①③
C.⑤②④①③ D.⑤④②①③
(2)步骤①中所用的玻璃仪器有烧杯、
(3)通过步骤①中过滤后的滤液,检验SO42-是否除尽的操作方法是
Ⅱ.碘是人体所需的必需元素,海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海洋植物中提取碘的流程如下:











 ―→
―→
(1)上述过程灼烧海藻是在
(2)上述步骤②中是加入了氯水,利用氯水中的Cl2把I-氧化为I2,请写出该反应的离子方程式
(3)上述步骤③中加入了CCl4后进行振荡,振荡后静置分层,上层
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.NaClO广泛用作水处理剂及漂白剂。
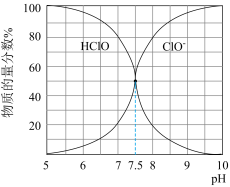
已知:25℃时NaClO溶液中HClO、 物质的量分数随pH的分布如右图所示。
物质的量分数随pH的分布如右图所示。
(1)工业上将 通入
通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于___________ (填“酸”、“盐”、“氧化物”),制备NaClO的化学方程式为___________ 。
②溶液pH=9时,该溶液中主要存在的阴离子有___________ (填化学式)。
Ⅱ. 是一种重要的杀菌消毒剂,其一种生产工艺如下:
是一种重要的杀菌消毒剂,其一种生产工艺如下:
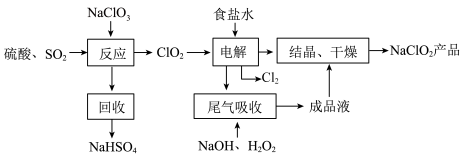
(2)写出“反应”步骤中生成 的化学方程式
的化学方程式___________ 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 ,要加入的试剂分别为
,要加入的试剂分别为___________ ,___________ 。精制时如何证明 已经完全除尽:
已经完全除尽:___________ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,发生如下反应:
,发生如下反应:
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
①配平上述化学方程式。___________
②某容器中发生一个化学反应,其中涉及 、
、 、
、 、
、 、
、 、
、 六种粒子。其中
六种粒子。其中 、
、 的物质的量随时间变化的曲线下图所示。
的物质的量随时间变化的曲线下图所示。

则该反应的离子方程式为:___________ 。
已知:25℃时NaClO溶液中HClO、
 物质的量分数随pH的分布如右图所示。
物质的量分数随pH的分布如右图所示。
(1)工业上将
 通入
通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②溶液pH=9时,该溶液中主要存在的阴离子有
Ⅱ.
 是一种重要的杀菌消毒剂,其一种生产工艺如下:
是一种重要的杀菌消毒剂,其一种生产工艺如下:
(2)写出“反应”步骤中生成
 的化学方程式
的化学方程式(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和
和 ,要加入的试剂分别为
,要加入的试剂分别为 已经完全除尽:
已经完全除尽:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,发生如下反应:
,发生如下反应:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
①配平上述化学方程式。
②某容器中发生一个化学反应,其中涉及
 、
、 、
、 、
、 、
、 、
、 六种粒子。其中
六种粒子。其中 、
、 的物质的量随时间变化的曲线下图所示。
的物质的量随时间变化的曲线下图所示。
则该反应的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】高铁酸钾(K2FeO4)是很好的净水剂,高铁酸钡( BaFeO4)是高能电池阳极的优良材料。已知:K2FeO4为紫色固体,微溶于KOH溶液,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定;在碱性溶液中,NaCl、NaNO3、K2FeO4的溶解性都小于Na2FeO4;BaFeO4难溶于水和碱性溶液。某化学兴趣小组欲制取“84”消毒液,进而制取少量K2FeO4和 BaFeO4。请回答下列问题:
【实验一】选择合适的仪器和试剂制取氯气,进而制备高浓度的“84”消毒液。

(1)选择合适的仪器,导管接口正确的连接顺序为___________ ;所选装置(A或B)中发生反应的离子方程式为______________________ 。
【实验二】用“84”消毒液制取K2FcO4
实验步骤:①用如图所示装置(夹持仪器略去)使反应物充分反应;②用砂芯漏斗对烧杯中的溶液进行抽滤,向滤液中慢慢加入KOH溶液;③再用砂芯漏斗对步骤②的最后反应混合物进行抽滤,并用苯、乙醚洗涤沉淀,真空干燥后得K2FeO4。

(2)写出步骤①中物质在20℃冷水浴中发生反应的化学方程式:______________________ 。
(3)步骤②中能够发生反应的原因是______________________ ,步骤③中不用水,而用苯、乙醚洗涤沉淀的目的是_________________________________ 。
【实验三】将上述产品配成K2FeO4碱性溶液,再慢慢加入Ba(OH)2溶液,抽滤得 BaFeO4。
(4)若投入ag硝酸铁晶体,得到bg高铁酸钡,则高铁酸钡的产率是___________ 。[已知Fe(NO3)3·9H2O的摩尔质量为404g·mol-1, BaFeO4的摩尔质量为257g·mol-1]
【实验四】利用如图所示电解装置也可以制得 BaFeO4。

(5)在___________ (填“阳极区”或“阴极区”)可得到高铁酸钡,阳极的电极反应式为____________ 。
【实验一】选择合适的仪器和试剂制取氯气,进而制备高浓度的“84”消毒液。

(1)选择合适的仪器,导管接口正确的连接顺序为
【实验二】用“84”消毒液制取K2FcO4
实验步骤:①用如图所示装置(夹持仪器略去)使反应物充分反应;②用砂芯漏斗对烧杯中的溶液进行抽滤,向滤液中慢慢加入KOH溶液;③再用砂芯漏斗对步骤②的最后反应混合物进行抽滤,并用苯、乙醚洗涤沉淀,真空干燥后得K2FeO4。

(2)写出步骤①中物质在20℃冷水浴中发生反应的化学方程式:
(3)步骤②中能够发生反应的原因是
【实验三】将上述产品配成K2FeO4碱性溶液,再慢慢加入Ba(OH)2溶液,抽滤得 BaFeO4。
(4)若投入ag硝酸铁晶体,得到bg高铁酸钡,则高铁酸钡的产率是
【实验四】利用如图所示电解装置也可以制得 BaFeO4。

(5)在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铂、镁在现代工业中有着极为重要的应用,某化工厂从含铂废料(主要成分为 ,含少量
,含少量 ,表面沉积着有机物)中回收铂,并获得
,表面沉积着有机物)中回收铂,并获得 的工艺流程如图所示:
的工艺流程如图所示:

该工艺条件下,相关金属离子开始沉淀和完全沉淀时的 如下表:
如下表:
(1)灼烧含铂废料最主要的目的是___________ 。
(2)滤渣1的主要成分为___________ ,“沉铂”得到的沉淀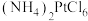 (氯铂酸铵)中铂元素的化合价为
(氯铂酸铵)中铂元素的化合价为___________ 。
(3)“还原”步骤中氯铂酸铵沉淀与 溶液反应的主要离子方程式为
溶液反应的主要离子方程式为___________ 。
(4)“试剂 ”可选用
”可选用___________ , 的调控范围为
的调控范围为___________ 。
a.盐酸 b. 溶液 c.氨水 d.
溶液 c.氨水 d.
(5)“系列操作”中最后的步骤为在 氛围中结晶,原因是
氛围中结晶,原因是___________
(6)某小组为测定 溶液浓度进行以下探究:取
溶液浓度进行以下探究:取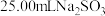 样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用
样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用 标准溶波滴定,达到滴定终点的判断依据是
标准溶波滴定,达到滴定终点的判断依据是___________ 。平行测定三次,平均消耗 标准溶液
标准溶液 ,计算样品溶液中
,计算样品溶液中 的浓度为
的浓度为___________  。
。
 ,含少量
,含少量 ,表面沉积着有机物)中回收铂,并获得
,表面沉积着有机物)中回收铂,并获得 的工艺流程如图所示:
的工艺流程如图所示:
该工艺条件下,相关金属离子开始沉淀和完全沉淀时的
 如下表:
如下表: |  |  | |
| 开始沉淀 | 2.2 | 3.5 | 9.5 |
| 完全沉淀 | 3.2 | 4.7 | 11.1 |
(1)灼烧含铂废料最主要的目的是
(2)滤渣1的主要成分为
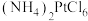 (氯铂酸铵)中铂元素的化合价为
(氯铂酸铵)中铂元素的化合价为(3)“还原”步骤中氯铂酸铵沉淀与
 溶液反应的主要离子方程式为
溶液反应的主要离子方程式为(4)“试剂
 ”可选用
”可选用 的调控范围为
的调控范围为a.盐酸 b.
 溶液 c.氨水 d.
溶液 c.氨水 d.
(5)“系列操作”中最后的步骤为在
 氛围中结晶,原因是
氛围中结晶,原因是(6)某小组为测定
 溶液浓度进行以下探究:取
溶液浓度进行以下探究:取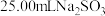 样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用
样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用 标准溶波滴定,达到滴定终点的判断依据是
标准溶波滴定,达到滴定终点的判断依据是 标准溶液
标准溶液 ,计算样品溶液中
,计算样品溶液中 的浓度为
的浓度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碘化钡(BaI2·2H2O)是一种白色粉末,常用于制取其他含碘化合物。一种制备流程如下:

(1)步骤I制FeI2溶液时,提高反应速率的可行措施有____________ (填序号)。
a.铁粉和碘粉用球磨机磨成细粉 b.增大n(铁粉):n(碘)的配料比
c.适当升高反应温度和搅拌速度 d.向反应器中加水至I2全部溶解
(2)步骤II发生反应的化学方程式为____________________________________ ;用pH试纸测定溶液pH的方法是____________________________________ 。
(3)步骤III小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是__________________ ;步骤IV中用到的玻璃仪器____________ 。
(4)从过滤2所得滤液中获得BaI2·2H2O(溶解度曲线如右图所示)的方法是_____________ 。


(1)步骤I制FeI2溶液时,提高反应速率的可行措施有
a.铁粉和碘粉用球磨机磨成细粉 b.增大n(铁粉):n(碘)的配料比
c.适当升高反应温度和搅拌速度 d.向反应器中加水至I2全部溶解
(2)步骤II发生反应的化学方程式为
(3)步骤III小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是
(4)从过滤2所得滤液中获得BaI2·2H2O(溶解度曲线如右图所示)的方法是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。

(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl2
① 写出利用装置Ⅰ制备氯气的离子反应方程式:___________ 。
② 利用上述装置制备NO时,Ⅱ中盛装物质为___________ (写化学式)。
③写出A管的作用___________ 。
(2)利用以下装置在常温常压下制备ClNO

① 装置连接顺序为a→___________ (按气流自左向右方向,用小写字母表示)。
② 为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为___________ 。
③ 装置Ⅸ的作用是___________ 。
④ 装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾气,可将尾气与___________ (气体)同时通入NaOH溶液中。

(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl2
① 写出利用装置Ⅰ制备氯气的离子反应方程式:
② 利用上述装置制备NO时,Ⅱ中盛装物质为
③写出A管的作用
(2)利用以下装置在常温常压下制备ClNO

① 装置连接顺序为a→
② 为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为
③ 装置Ⅸ的作用是
④ 装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾气,可将尾气与
您最近一年使用:0次



