硫、氮是化工生产中的重要非金属元素,铁、铝是生活中重要的金属元素。回答下列相关问题。
(1)(NH4)2Fe(SO4)2•6H2O是一种重要的化工原料,用途十分广泛。一般从废铁屑中回收制备,铁屑经碱溶液洗净之后,用过量硫酸溶解。再加入稍过量硫酸铵饱和溶液,小火下蒸发溶剂直到晶膜出现,______ 、______ 、用少量乙醇洗涤。(填写实验操作)
(2)在400℃时,将一定量的SO2和14molO2充入一个盛有催化剂的10L恒容密闭容器中进行反应:2SO2+O2 2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:
2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:
①2min内平均反应速率:v(O2)=______ 。
②发生反应前容器内压强与发生反应后容器中压强比值为______ 。
(3)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池放电时的总反应式为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH,则该电池放电时负极反应式为______ ,_____ (填“正”或“负”)极附近溶液的碱性增强。
(4)向100mL某硝酸和硫酸的混合稀溶液中加入5.04g铁粉,恰好完全反应,只收集到一种气体,溶液中只存在一种盐,溶液取样加入硫氰化钾无血红色,则原溶液中硫酸的物质的量浓度为______ 。
(5)向某无色溶液中通入过量的HCl,先产生白色沉淀,后白色沉淀溶解,得到无色溶液,向所得无色溶液中再通入NH3至过量,试描述整个过程中的反应现象______ 。
(1)(NH4)2Fe(SO4)2•6H2O是一种重要的化工原料,用途十分广泛。一般从废铁屑中回收制备,铁屑经碱溶液洗净之后,用过量硫酸溶解。再加入稍过量硫酸铵饱和溶液,小火下蒸发溶剂直到晶膜出现,
(2)在400℃时,将一定量的SO2和14molO2充入一个盛有催化剂的10L恒容密闭容器中进行反应:2SO2+O2
 2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:
2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:①2min内平均反应速率:v(O2)=
②发生反应前容器内压强与发生反应后容器中压强比值为
(3)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池放电时的总反应式为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH,则该电池放电时负极反应式为
(4)向100mL某硝酸和硫酸的混合稀溶液中加入5.04g铁粉,恰好完全反应,只收集到一种气体,溶液中只存在一种盐,溶液取样加入硫氰化钾无血红色,则原溶液中硫酸的物质的量浓度为
(5)向某无色溶液中通入过量的HCl,先产生白色沉淀,后白色沉淀溶解,得到无色溶液,向所得无色溶液中再通入NH3至过量,试描述整个过程中的反应现象
更新时间:2023-05-16 07:38:23
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】大气压强对许多物理实验和化学实验有着重要影响,制取氨气并完成喷泉实验。

(1)检验圆底烧瓶中氨气收集满的方法是_________________________________ 。
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是________ ,该实验的原理是________________________________________ 。
(3)如果只提供如图2的装置,请说明引发喷泉的方法:______________________ 。

(1)检验圆底烧瓶中氨气收集满的方法是
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(3)如果只提供如图2的装置,请说明引发喷泉的方法:
您最近一年使用:0次
【推荐2】已知A、B、C、D均为化合物,B、C常温常压下为气体,C气体可使湿润的红色石蕊试纸变蓝色;又知1mol A在200℃时分解仅得1mol B和一定量的水两种产物,A中含有NO 。A、B、C、D间有如图关系:
。A、B、C、D间有如图关系:
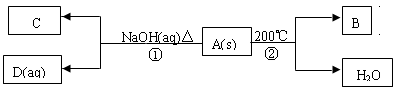
试回答下列问题:
(1)写出A、C的化学式:A_______ ;C_______ 。
(2)写出反应①的离子方程式:_______ 。
(3)写出反应②的化学方程式:_______ 。
 。A、B、C、D间有如图关系:
。A、B、C、D间有如图关系:
试回答下列问题:
(1)写出A、C的化学式:A
(2)写出反应①的离子方程式:
(3)写出反应②的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有害气体。请回答下列问题:
(1)Q在元素周期表中的位置为__________________ 。
(2)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)_______________ 。
(3)Y的气态氢化物能使湿润的红色石蕊试纸变蓝的原因:________________ (用离子方程式表示)。
(4)QM2的电子式为______________ 。
(5)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为______________ 。
(1)Q在元素周期表中的位置为
(2)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)
(3)Y的气态氢化物能使湿润的红色石蕊试纸变蓝的原因:
(4)QM2的电子式为
(5)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
【推荐1】如图是中学化学中常见物质间的反应转化关系图,其中部分产物已略去。常温下, 为固体单质,
为固体单质, 、
、 为液体,其余都为气体。
为液体,其余都为气体。 为化合物,
为化合物, 的浓溶液与
的浓溶液与 在加热条件下反应生成
在加热条件下反应生成 、
、 和
和 。
。 可用作工业上冶炼金属的还原剂。请按要求填空:
可用作工业上冶炼金属的还原剂。请按要求填空:
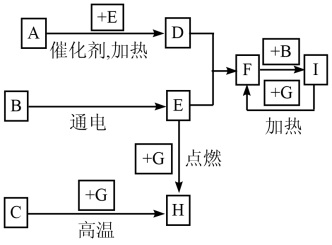
(1)写出下列物质的化学式。
_______ ;
_______ ;
_______ 。
(2)写出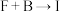 的化学方程式:
的化学方程式:_______ 。
(3)写出 和
和 的浓溶液反应的化学方程式:
的浓溶液反应的化学方程式:_______ 。
 为固体单质,
为固体单质, 、
、 为液体,其余都为气体。
为液体,其余都为气体。 为化合物,
为化合物, 的浓溶液与
的浓溶液与 在加热条件下反应生成
在加热条件下反应生成 、
、 和
和 。
。 可用作工业上冶炼金属的还原剂。请按要求填空:
可用作工业上冶炼金属的还原剂。请按要求填空:
(1)写出下列物质的化学式。



(2)写出
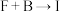 的化学方程式:
的化学方程式:(3)写出
 和
和 的浓溶液反应的化学方程式:
的浓溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】磁性材料FexSy与石墨烯构成的复合材料,用于高性能锂硫电池。某化学小组按如下装置测定该磁性材料FexSy的组成。___________ ,其作用是___________ 。
(2)实验时管式炉中产生的气体能使品红溶液褪色,三颈烧瓶中产生白色沉淀,三颈烧瓶中发生反应的离子方程式是___________ 。
(3)若管式炉内反应的温度为600~700℃,长玻璃管M除了导气外还有的作用是___________ ,若没有长玻璃管会导致测定的y值___________ (填“偏大”“偏小”或“无影响”)。
(4)取2.960g试样放入管式炉充分反应后,再通入O2一段时间,然后将三颈烧瓶中的固体过滤,洗涤,干燥称量得到9.320g,操作过程中,检验沉淀已洗涤干净的方法是___________ 。小组成员提出用浓硝酸代替H2O2,其他小组成员提出反驳意见,反驳的理由是___________ 。
(5)充分反应后,取管式炉中固体溶于足量的稀硫酸中,取少量反应后的溶液,加入___________ (填试剂名称),溶液变红,证明溶液中含有Fe3+;另取少量溶液,加入K3[Fe(CN)6]溶液,没有明显变化,则管式炉中固体的颜色是_______ ,管式炉中发生的化学反应方程式为___________ 。

(2)实验时管式炉中产生的气体能使品红溶液褪色,三颈烧瓶中产生白色沉淀,三颈烧瓶中发生反应的离子方程式是
(3)若管式炉内反应的温度为600~700℃,长玻璃管M除了导气外还有的作用是
(4)取2.960g试样放入管式炉充分反应后,再通入O2一段时间,然后将三颈烧瓶中的固体过滤,洗涤,干燥称量得到9.320g,操作过程中,检验沉淀已洗涤干净的方法是
(5)充分反应后,取管式炉中固体溶于足量的稀硫酸中,取少量反应后的溶液,加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】亚硝酰氯( )是一种黄色气体,沸点为
)是一种黄色气体,沸点为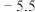 ℃。其液体呈红褐色。遇水发生反应:
℃。其液体呈红褐色。遇水发生反应: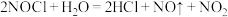 。某化学兴趣小组设计如图装置用
。某化学兴趣小组设计如图装置用 和
和 制备
制备 。回答下列相关问题:
。回答下列相关问题:
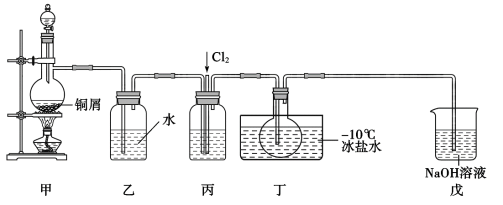
(1)甲装置发生反应的离子方程式为_______ ,装置丙中的液体是浓硫酸。
(2)实验时,先通入 ,待丁中烧瓶内充满黄绿色气体时,再通入
,待丁中烧瓶内充满黄绿色气体时,再通入 ,这样做的目的是
,这样做的目的是_______ 。
(3)装置丁中冰盐水的作用是_______ 。
(4)经分析该套装置设计上有一处明显缺陷,改进方法是_______ 。(用文字描述)
(5)吸收尾气时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。(已知: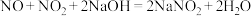 )
)
(6)反应完成后,取烧瓶中所得产物mg溶于水,配制成 溶液,取出
溶液,取出 ,再加入
,再加入

 溶液恰好完全反应,则产物中
溶液恰好完全反应,则产物中 纯度(质量分数)的计算式为
纯度(质量分数)的计算式为_______ 。
 )是一种黄色气体,沸点为
)是一种黄色气体,沸点为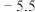 ℃。其液体呈红褐色。遇水发生反应:
℃。其液体呈红褐色。遇水发生反应: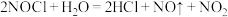 。某化学兴趣小组设计如图装置用
。某化学兴趣小组设计如图装置用 和
和 制备
制备 。回答下列相关问题:
。回答下列相关问题:
(1)甲装置发生反应的离子方程式为
(2)实验时,先通入
 ,待丁中烧瓶内充满黄绿色气体时,再通入
,待丁中烧瓶内充满黄绿色气体时,再通入 ,这样做的目的是
,这样做的目的是(3)装置丁中冰盐水的作用是
(4)经分析该套装置设计上有一处明显缺陷,改进方法是
(5)吸收尾气时,
 发生反应的化学方程式为
发生反应的化学方程式为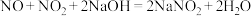 )
)(6)反应完成后,取烧瓶中所得产物mg溶于水,配制成
 溶液,取出
溶液,取出 ,再加入
,再加入

 溶液恰好完全反应,则产物中
溶液恰好完全反应,则产物中 纯度(质量分数)的计算式为
纯度(质量分数)的计算式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】T1℃时,向2.0L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5(g) PCl3(g)+Cl2(g),经一段时间后达到平衡状态。建立平衡过程中时间t与PCl3物质的量的关系如表所示。若升高温度至T2℃,混合气体黄绿色加深。
PCl3(g)+Cl2(g),经一段时间后达到平衡状态。建立平衡过程中时间t与PCl3物质的量的关系如表所示。若升高温度至T2℃,混合气体黄绿色加深。
(1)该反应△H___________ 0(填“>”、“<”或“=”),T1℃时反应在前50 s的平均速率v(PCl3)=___________ ,平衡常数K=___________
(2)下列可用于判断反应达到平衡状态的依据是___________
A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.每生成3molP─Cl键同时生成1molCl─Cl键
(3)T1℃时反应达到平衡后,再向容器中充入0.9mol PCl5、0.1molPCl3和0.1molCl2,再次达到平衡前v(正)___________ v(逆)(填“>”、“<”或“=”),平衡后PCl5体积分数___________ (填“增大”、“减小”或“不变”)。
 PCl3(g)+Cl2(g),经一段时间后达到平衡状态。建立平衡过程中时间t与PCl3物质的量的关系如表所示。若升高温度至T2℃,混合气体黄绿色加深。
PCl3(g)+Cl2(g),经一段时间后达到平衡状态。建立平衡过程中时间t与PCl3物质的量的关系如表所示。若升高温度至T2℃,混合气体黄绿色加深。| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
(1)该反应△H
(2)下列可用于判断反应达到平衡状态的依据是
A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.每生成3molP─Cl键同时生成1molCl─Cl键
(3)T1℃时反应达到平衡后,再向容器中充入0.9mol PCl5、0.1molPCl3和0.1molCl2,再次达到平衡前v(正)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
(1)已知:Ⅰ. ;
;
Ⅱ.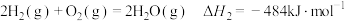 。
。
在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式如下: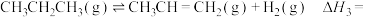
_______  。
。
(2) 时,将
时,将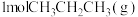 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: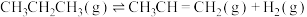 。用压强传感器测出容器内体系压强随时间的变化关系如图a所示:
。用压强传感器测出容器内体系压强随时间的变化关系如图a所示:

①已知: 。
。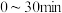 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为_______ kPa·min-1。
② 时,反应的平衡常数
时,反应的平衡常数
_______  (
( 为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。
为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。
③保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是_______ 或_______ ;425℃之后,丙烯产率快速降低的主要原因可能是_______ (任写一点)。
(3)丙烷在有氧气参与的条件下也可发生脱氢反应,即: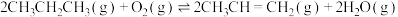 。丙烷的无氧脱氢反应:
。丙烷的无氧脱氢反应: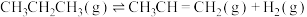 与有氧脱氢反应的压强平衡常数的对数
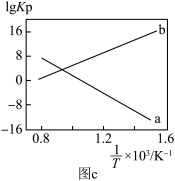
与有氧脱氢反应的压强平衡常数的对数 与温度倒数
与温度倒数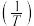 的关系如图c所示。则图中表示有氧脱氢反应的是
的关系如图c所示。则图中表示有氧脱氢反应的是_______ (填“a”或“b”)。
(1)已知:Ⅰ.
 ;
;Ⅱ.
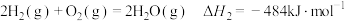 。
。在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式如下:
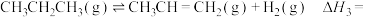
 。
。(2)
 时,将
时,将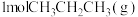 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: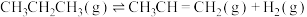 。用压强传感器测出容器内体系压强随时间的变化关系如图a所示:
。用压强传感器测出容器内体系压强随时间的变化关系如图a所示:
①已知:
 。
。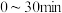 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为②
 时,反应的平衡常数
时,反应的平衡常数
 (
( 为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。
为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。③保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
(3)丙烷在有氧气参与的条件下也可发生脱氢反应,即:
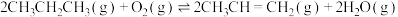 。丙烷的无氧脱氢反应:
。丙烷的无氧脱氢反应: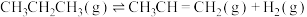 与有氧脱氢反应的压强平衡常数的对数
与有氧脱氢反应的压强平衡常数的对数 与温度倒数
与温度倒数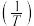 的关系如图c所示。则图中表示有氧脱氢反应的是
的关系如图c所示。则图中表示有氧脱氢反应的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】 .为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
.为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应: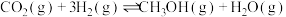 。经测得CH3OH和CO2的物质的量随时间变化如图所示。
。经测得CH3OH和CO2的物质的量随时间变化如图所示。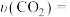
___________ 。
(2)达到平衡时,H2的浓度为___________  。
。
(3)改变条件后,化学反应速率会减小的是___________(填字母)
(4)平衡时,CO2的体积分数为___________ %。
(5)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为 ,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)
,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)
 .利用如图所示原电池的装置使NH3与NO2均转化为N2,既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,请回答下列问题:
.利用如图所示原电池的装置使NH3与NO2均转化为N2,既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,请回答下列问题:___________ (填“A”或“B”),电极B上发生的电极反应为:___________ 。
(7)阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。为使电池持续放电,离子交换膜应为___________ 离子交换膜(填“阳”或“阴”)。
 .为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
.为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应: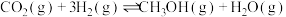 。经测得CH3OH和CO2的物质的量随时间变化如图所示。
。经测得CH3OH和CO2的物质的量随时间变化如图所示。
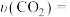
(2)达到平衡时,H2的浓度为
 。
。(3)改变条件后,化学反应速率会减小的是___________(填字母)
| A.降低温度 | B.加入催化剂 |
| C.增大容器容积 | D.恒容下充入He |
(4)平衡时,CO2的体积分数为
(5)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为
 ,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)
,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)A.反应中CO与CH3OH的物质的量之比为 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1molCO,同时生成1molCH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
 .利用如图所示原电池的装置使NH3与NO2均转化为N2,既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,请回答下列问题:
.利用如图所示原电池的装置使NH3与NO2均转化为N2,既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,请回答下列问题: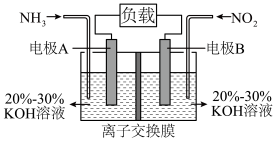
(7)阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。为使电池持续放电,离子交换膜应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g) + 2H2(g) CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=______________
②下列说法正确的是___________ (填字母序号)。
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充人氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g) SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K =
SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K = _________ 。
(3)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H= +131.0kJ/molZiyuanku.com
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= -43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= -178.3kJ/mol
计算①反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=_________ kJ/mol;
②对于可逆反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是_________ 。(填字母)
A.降低体系的温度 B.压缩容器的体积
C.增加CaO的量 D.选用适当的催化剂
(4)甲醇作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为_________________ 。
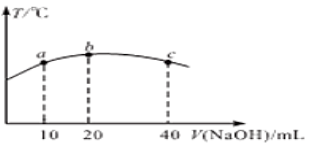
(5)若往20 mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是________ (填标号)
①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
 CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。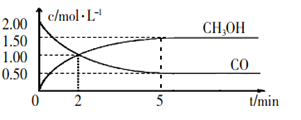
①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=
②下列说法正确的是
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充人氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g)
 SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K =
SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K = (3)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H= +131.0kJ/molZiyuanku.com
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= -43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= -178.3kJ/mol
计算①反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=②对于可逆反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是A.降低体系的温度 B.压缩容器的体积
C.增加CaO的量 D.选用适当的催化剂
(4)甲醇作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为
(5)若往20 mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是
①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】已知:乙二酸(HOOC—COOH,可简写为H2C2O4),俗称草酸。已知:25℃H2C2O4 K1=5.4×10-2,K2=5.4×10-5。
(1)已知:25℃Ka(HF)=3.53×10-4,请写出少量草酸(H2C2O4)与NaF溶液反应的化学方程式:___ 。
(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,,所得溶液中H2C2O4、HC2O 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图一所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图一所示,回答下列问题:___ 。(填“酸性”、“碱性”或“中性”)。
②如果所得溶液溶质为K2C2O4,则该溶液中各离子浓度由大到小顺序为___ 。
③当所得溶液pH=2.7时,溶液中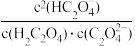 =
=___ 。
(3)已知25℃草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:25℃时向20 mL碳酸钙的饱和溶液中逐滴加入1.0×10-3 mol/L的草酸钾溶液20 mL,(填能或否)___ 产生草酸钙沉淀,理由___ (写出计算过程)。
(4)O2辅助的Al-CO2电池工作原理如图二所示。该电池电容量大,能有效利用CO2电池反应产物Al2(C2O4)3是重要的化工原料。已知:电池正极发生的反应有:O2+e-=O 、2CO2+2O2=C2O
、2CO2+2O2=C2O +2O2,则电池的总反应式为
+2O2,则电池的总反应式为___ ,反应过程中O2作用是___ 。
(1)已知:25℃Ka(HF)=3.53×10-4,请写出少量草酸(H2C2O4)与NaF溶液反应的化学方程式:
(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,,所得溶液中H2C2O4、HC2O
 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图一所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图一所示,回答下列问题: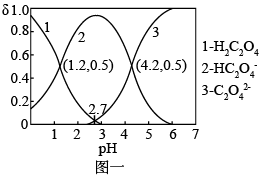
②如果所得溶液溶质为K2C2O4,则该溶液中各离子浓度由大到小顺序为
③当所得溶液pH=2.7时,溶液中
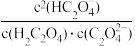 =
=(3)已知25℃草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:25℃时向20 mL碳酸钙的饱和溶液中逐滴加入1.0×10-3 mol/L的草酸钾溶液20 mL,(填能或否)
(4)O2辅助的Al-CO2电池工作原理如图二所示。该电池电容量大,能有效利用CO2电池反应产物Al2(C2O4)3是重要的化工原料。已知:电池正极发生的反应有:O2+e-=O
 、2CO2+2O2=C2O
、2CO2+2O2=C2O +2O2,则电池的总反应式为
+2O2,则电池的总反应式为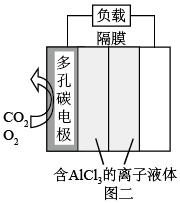
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的价电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物的电子式为___________ 。
(2)已知:① ;△
;△
② ;
;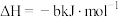
③ ;
; (“•”表示形成共价键所提供的电子)
(“•”表示形成共价键所提供的电子)
写出298 K时,A2与E2反应的热化学方程式___________ 。
(3)在某温度下、容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应: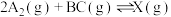 ;
;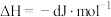 (
(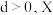 为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则该时间段内A2的平均反应速率为___________ 。
②该温度下此反应的平衡常数K的值为___________ 。
③三个容器中的反应分别达平衡时各组数据关系正确的是___________ (填序号)。
A.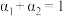 B.
B. C.
C.
D.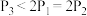 E.
E. F.
F.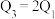
(4)近年来,我国科研人员研制出一种一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为: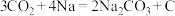 。
。
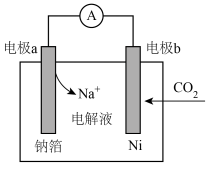
①电极a为___________ 极(填“正”或“负”)。
②电极b发生的电极反应为___________ 。
(1)A、C、D形成的化合物的电子式为
(2)已知:①
 ;△
;△
②
 ;
;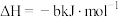
③
 ;
; (“•”表示形成共价键所提供的电子)
(“•”表示形成共价键所提供的电子)写出298 K时,A2与E2反应的热化学方程式
(3)在某温度下、容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:
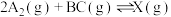 ;
;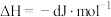 (
(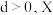 为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |  |  |  |
②该温度下此反应的平衡常数K的值为
③三个容器中的反应分别达平衡时各组数据关系正确的是
A.
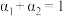 B.
B. C.
C.
D.
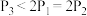 E.
E. F.
F.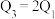
(4)近年来,我国科研人员研制出一种一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为:
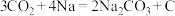 。
。
①电极a为
②电极b发生的电极反应为
您最近一年使用:0次



