设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.100mL  浓硫酸中含有的氧原子数大于 浓硫酸中含有的氧原子数大于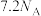 |
B.2mol  与1 mol 与1 mol  充分反应后体系中含有的 充分反应后体系中含有的 分子数为 分子数为 |
C.标准状况下,22.4L  中含有的分子数为 中含有的分子数为 |
D.56g Fe与过量稀硝酸反应,转移的电子数为 |
更新时间:2023-04-27 22:37:22
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏伽德罗常数的值,则下列说法正确的是
A.0.4mol AgNO3受热完全分解(2AgNO3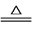 2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA 2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA |
| B.6.4g CaC2中含有的离子总数目为0.3NA |
| C.1 mol FeI2与一定量氯气反应时,若已知有1mol Fe2+被氧化则转移的电子数为3NA |
| D.1mol 苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
A.20g  中含有的原子总数为3NA 中含有的原子总数为3NA |
B.常温下,1mol/L的 溶液中含有的 溶液中含有的 数为2NA 数为2NA |
C.1mol Mg与足量 或 或 反应生成MgO或 反应生成MgO或 ,均失去2NA个电子 ,均失去2NA个电子 |
D.1mol  与1L 4mol/L盐酸反应生成的 与1L 4mol/L盐酸反应生成的 的分子数为2NA 的分子数为2NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】设NA表示阿伏加 德罗常数的数值,下列说法正确的是( )
| A.14g乙烯中含有的原子数目为3NA |
| B.标准状况下,2.24LCHCl3的分子数为0.1NA |
| C.1mol乙醇中含有的碳氢键数目为6NA |
| D.17g羟基(-OH)中含有的电子数目为9NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】下列实验现象或表述正确的是
| A.过量的铁投入一定量的稀硝酸中,充分反应后取适量溶液于试管中,立即滴加KSCN溶液,溶液不显红色 |
| B.向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 |
| C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可 |
| D.FeO投入稀硫酸和稀硝酸中均得到浅绿色溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于水,可溶于氯离子浓度较大的体系,易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,生产CuCl的工艺如下:
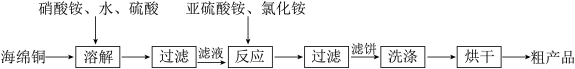
下列说法错误的是

下列说法错误的是
A.“溶解”过程发生氧化还原反应的离子方程式是3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
B.“反应”过程发生反应的离子方程式是Cu2++SO +Cl-+H2O=CuCl↓+SO +Cl-+H2O=CuCl↓+SO +2H+ +2H+ |
| C.“溶解”过程中硫酸可用浓盐酸代替 |
| D.“烘干”需在隔绝空气的环境中进行 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列实验操作现象能得出相应结论的是
选项 | 实验操作 | 现象 | 结论 |
A | CuS溶于浓硝酸 | 有红棕色气泡产生 | CuS能被硝酸氧化 |
B | SO2通入滴有石蕊试液的水中 | 溶液变红但不褪色 | SO2有酸性,无漂白性 |
C | 向Na2CO3中滴入HClO3溶液 | 有气泡产生 | 非金属性Cl>C |
D | 将KI和FeCl3溶液在试管中混 合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列在有关工业生产的主要设备中采取的措施能达到相应目的的是( )
| 选项 | 化学工业 | 主要设备 | 措施 | 目的 |
| A. | 合成氨 | 合成塔 | 500℃左右 | 防止催化剂中毒 |
| B. | 电解食盐水 | 电解槽 | 石棉隔膜 | 防止氯气和氢氧化钠反应 |
| C. | 接触法制硫酸 | 接触室 | 五氧化二钒 | 提高二氧化硫的转化率 |
| D. | 侯式制碱 | 沉淀池 | 先通氨气,再通二氧化碳 | 有利于二氧化碳的吸收 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】用下列两种途径制取H2SO4(某些反应条件和产物已省略),下列有关说法不正确的是
途径①:S H2SO4 途径②:S
H2SO4 途径②:S SO2
SO2 SO3
SO3 H2SO4
H2SO4
途径①:S
 H2SO4 途径②:S
H2SO4 途径②:S SO2
SO2 SO3
SO3 H2SO4
H2SO4| A.途径①中反应仅体现了浓硝酸的强氧化性 |
| B.途径②中可通过控制反应条件,将S直接氧化为SO3 |
| C.由途径①和②分别制取1molH2SO4,理论上均消耗1molS,均共转移6mol电子 |
| D.途径②相较于途径①更能体现“绿色化学”的理念,因为途径②的污染相对于途径①更小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】工业上制硫酸的设备分为三大部分,一是沸腾炉、二是接触室、三是吸收塔。在沸腾炉内二硫化亚铁与氧气发生反应,生成二氧化硫;在接触室内有催化剂存在下SO2进一步与O2化合,生成SO3;SO3流经吸收塔时,采用98.3%的浓硫酸吸收,SO3与水化合形成硫酸。为研究吸收SO3应选用的物质,依照工业上制备硫酸的流程设计了下面的实验装置。

下列有关叙述不正确的是

下列有关叙述不正确的是
| A.本实验中装置甲的作用仅仅是用于干燥气体 |
| B.反应中要求乙反应器内氧气的物质的量要比二氧化硫的物质的量多一倍左右,该装置无法通过现象判断 |
| C.实验时丁装置在反应过程中先出现气泡,不久就出现了白雾,而丙装置一直都没有任何现象,说明浓硫酸的吸收效果比水好 |
| D.该实验装置存在明显的缺陷 |
您最近一年使用:0次



