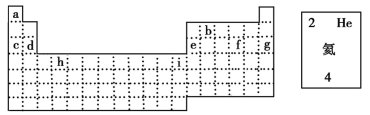
元素周期表的一部分如图所示,其中每一个序号分别代表一种元素。回答下列问题。

(1)地壳中含量最多的金属元素为___________ (填化学式),该元素在元素周期表中的位置为___________ 。
(2)①和②形成的一种常温下极易溶于水且有刺激性气味的气体的电子式为___________ ,该物质___________ (填“属于”或“不属于”)电解质。
(3)③和④相比较,最简单氢化物的稳定性较强的是___________ (填化学式),简单离子半径:⑤___________ (填“>”、“<”或“=”)⑦。
(4)⑤和⑧相比较,金属性较强的是___________ (填元素符号),下列表述中,能证明这一事实的是___________ (填标号)。
A.⑤单质密度比⑧单质的大
B.⑧单质与水反应比⑤单质与水反应剧烈
C.⑤单质的熔点比⑧单质的高

(1)地壳中含量最多的金属元素为
(2)①和②形成的一种常温下极易溶于水且有刺激性气味的气体的电子式为
(3)③和④相比较,最简单氢化物的稳定性较强的是
(4)⑤和⑧相比较,金属性较强的是
A.⑤单质密度比⑧单质的大
B.⑧单质与水反应比⑤单质与水反应剧烈
C.⑤单质的熔点比⑧单质的高
更新时间:2023-05-15 09:29:01
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)A在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程_______ 。
(4)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
完成下列填空:
(1)A在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程
(4)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求完成下列各题:
(1)微粒铵根14N2H4+中的中子数是___________________ ,核外电子数是_____ 。
(2)写出 N2的电子式_________________ ,画出HClO分子的结构式_________________
CO2的电子式________________ ;Na2O2的电子式为___________________
(3)如图是元素周期表的一个方格 ,其中19.00的意义是
,其中19.00的意义是______________
(4) 25℃,101 kPa,1g C2H2气体充分燃烧生成气体CO2和液态H2O,放出125kJ的热量,写出C2H2燃烧热的热化学方程式_________________
(1)微粒铵根14N2H4+中的中子数是
(2)写出 N2的电子式
CO2的电子式
(3)如图是元素周期表的一个方格
 ,其中19.00的意义是
,其中19.00的意义是(4) 25℃,101 kPa,1g C2H2气体充分燃烧生成气体CO2和液态H2O,放出125kJ的热量,写出C2H2燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:

(1)元素⑦的名称为______ ,在周期表中的位置______________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______ ,碱性最强的化合物的电子式是__________ 。
(3)用电子式表示元素④和⑥的化合物的形成过程:____________ ,该化合物属于______ (填“共价”或“离子”)化合物。
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式______ 。
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是_________ (用离子符号表示)

(1)元素⑦的名称为
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④和⑥的化合物的形成过程:
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据①~⑫元素的编号所在周期表中的位置,用相应的元素符号或者化学用语回答有关问题:
(1)能显+1 价,还能显-1 价的元素是___________ 。
(2)最难形成化合物的元素是___________ 。
(3)单质具有半导体性质的元素是___________ 。
(4)任意排放的氧化物溶于雨水形成酸雨的元素是___________ 。
(5)元素⑦氢化物水溶液与 SiO2反应的化学方程式为___________ 。
(6)最新发现的一种单质是由 60 个原子组成球状结构的分子。这种单质叫足球烯,它是由___________ 元素组成的。
(7)第三周期某元素氢化物(组成为 RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为___________ 。
(8)元素⑤与元素⑩形成化合物化学式为___________ ,该化合物在工业上用途是 ___________ (列举一种即可)。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)能显+1 价,还能显-1 价的元素是
(2)最难形成化合物的元素是
(3)单质具有半导体性质的元素是
(4)任意排放的氧化物溶于雨水形成酸雨的元素是
(5)元素⑦氢化物水溶液与 SiO2反应的化学方程式为
(6)最新发现的一种单质是由 60 个原子组成球状结构的分子。这种单质叫足球烯,它是由
(7)第三周期某元素氢化物(组成为 RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为
(8)元素⑤与元素⑩形成化合物化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据表中的①~⑧种元素在周期表中的位置,回答下列问题。
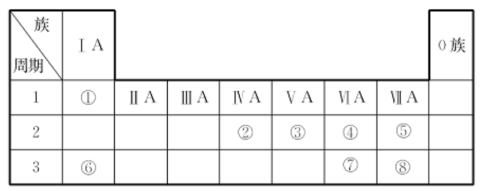
(1)元素⑥、⑦形成的简单的离子,半径大的是_______ (填离子符号)
(2)用电子式表示元素①和⑧的化合物的形成过程:_______ 。
(3)元素②的一种核素可以用来考古,请写该核素的中子数是_______ 。
(4)元素⑤、⑧的简单气态氢化物较稳定的是_______ (填化学式)。

(1)元素⑥、⑦形成的简单的离子,半径大的是
(2)用电子式表示元素①和⑧的化合物的形成过程:
(3)元素②的一种核素可以用来考古,请写该核素的中子数是
(4)元素⑤、⑧的简单气态氢化物较稳定的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】你对以上两组元素原子失电子能力强弱的预测正确吗?你从原子结构的角度对它们失电子能力强弱的解释是否合理?哪些证据支持了你的预测和解释?_______
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】结构决定性质,性质决定用途,试根据元素周期表中第三周期元素相关知识完成下列填空:
(1)原子最外层电子数与次外层电子数相同的元素名称为____________ ,氧化性最弱的简单阳离子是____________ 。
(2)最高正价与最低负价的绝对值相等的元素,其原子的核外电子排布式是____________ ,核外有____________ 种运动状态的电子,有____________ 种不同能量的电子。
(1)原子最外层电子数与次外层电子数相同的元素名称为
(2)最高正价与最低负价的绝对值相等的元素,其原子的核外电子排布式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】元素周期律(表)是认识元素化合物性质的重要理论。
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈
ⅱ.锂和镁的氢氧化物均为中等强度的碱
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物
根据以上事实,可知锂、钠、镁三种元素的金属性强弱关系是___________________ (用“>”“=”或“<”)。
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族。
①碱性:Sr(OH)2_____ Ba (OH)2(填“>”或“<”)。
②用原子结构的观点解释锶的化学性质与钡差异的原因:______________________________
(3)硒(Se)的部分信息如图,且知34Se、35Br位于同一周期。
①Se在元素周期表中的位置是_______________ 。
②H2Se的电子式是______________ 。
③Cl、Se、Br的非金属性强弱的顺序是__________________ ;能证明上述强弱关系的事实是____________________________ (写出一条即可)。
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的。完成下表:
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈
ⅱ.锂和镁的氢氧化物均为中等强度的碱
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物
根据以上事实,可知锂、钠、镁三种元素的金属性强弱关系是
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族。
①碱性:Sr(OH)2
②用原子结构的观点解释锶的化学性质与钡差异的原因:
(3)硒(Se)的部分信息如图,且知34Se、35Br位于同一周期。
| O | |
| S | |
| Se | Br |
②H2Se的电子式是
③Cl、Se、Br的非金属性强弱的顺序是
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的。完成下表:
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | SeO2+2SO2+2H2O=Se+2H2SO4 |
| 2 | ||
| 3 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】开发新型储氢材料是氢能利用的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有__ 个.
②LiBH4由Li+和BH4﹣构成,BH4﹣呈正四面体构型.LiBH4中不存在的作用力有__ (填标号).
A.离子键 B.共价键 C.金属键 D.配位键
③由BH4﹣结构可知Li,B,H元素的电负性由大到小排列顺序为__ .
(2)金属氢化物是具有良好发展前景的储氢材料.
LiH中,离子半径:Li+__ H﹣(填“>”、“=”或“<”).
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有
②LiBH4由Li+和BH4﹣构成,BH4﹣呈正四面体构型.LiBH4中不存在的作用力有
A.离子键 B.共价键 C.金属键 D.配位键
③由BH4﹣结构可知Li,B,H元素的电负性由大到小排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料.
LiH中,离子半径:Li+
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下面为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
(1)①的元素名称为:___________ ,元素④的原子结构示意图为___________ 。
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
(3)②、④组成的能引起温室效应的化合物的电子式为___________ ,其中含有的化学键为___________ 。
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为___________ (用化学式表示)。
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为___________ (用元素符号表示)。
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
| A.②的单质为固体,而③的单质为气体 |
| B.原子半径②比③大 |
| C.②的非金属性比③弱 |
| D.原子序数③比②大 |
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表列出了A—H 八种元素在元素周期表中的相对位置:
(1)请写出下列元素符号: D___________ ,E___________ ,G___________ ;在这八种元素中,化学性质最不活泼的是___________ 。(填写元素符号)
(2)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。(填写元素符号)
(3)F元素氢化物的化学式是___________ ,该氢化物在常温下跟B发生反应的化学方程式是___________ ,所得溶液的PH___________ 7。
(4)G元素跟A元素形成化合物为___________ ,并用电子式表示其形成过程___________ ,高温下灼烧该化合物时,火焰呈___________ 色
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 2 | E | F | ||||||
| 3 | A | C | D | G | H | |||
| 4 | B |
(1)请写出下列元素符号: D
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
(3)F元素氢化物的化学式是
(4)G元素跟A元素形成化合物为
您最近一年使用:0次