下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1)元素①在周期表中的位置是___________ 。
(2)元素③和⑦可形成化合物,用电子式表示其形成过程:___________ 。
(3)比较元素②、③形成离子的半径大小:___________ >___________ 。
(4)元素③、④、⑤组成的单质中,与水反应最剧烈的是___________ ,其离子方程式为:___________ 。
(5)③的最高价氧化物对应的水化物中含有的化学键类型为___________ ,形成化合物的类型为___________ (填“离子化合物”或“共价化合物”)。与⑤的最高价氧化物对应的水化物之间可以发生反应,该反应的离子方程式为___________ 。
(6)某同学将元素⑦的单质与元素③⑧组成的化合物的水溶液反应,写出该反应的离子方程式___________ ,请从原子结构的角度解释该反应能发生的原因:___________ 。
(7)已知硒(34Se)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质是___________ 。
a.Se的最低负化合价为-2价 b.SeO2既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为H2SeO3
族 周期 | IA | 0 | |||||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||||||
| 2 | ① | ② | |||||||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ||||||||
| 4 | ⑧ | ||||||||||||
(2)元素③和⑦可形成化合物,用电子式表示其形成过程:
(3)比较元素②、③形成离子的半径大小:
(4)元素③、④、⑤组成的单质中,与水反应最剧烈的是
(5)③的最高价氧化物对应的水化物中含有的化学键类型为
(6)某同学将元素⑦的单质与元素③⑧组成的化合物的水溶液反应,写出该反应的离子方程式
(7)已知硒(34Se)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质是
a.Se的最低负化合价为-2价 b.SeO2既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为H2SeO3
更新时间:2023-04-28 21:55:01
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
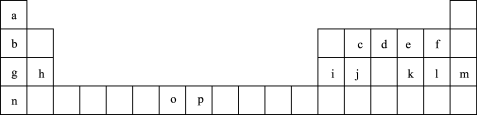
(1)基态o原子的外围电子排布图为_______ ;基态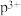 的最外层电子排布式为
的最外层电子排布式为_______ ;n的原子结构示意图为_______ 。表中所列元素的原子中,没有未成对电子的元素有_______ 种。
(2)原子序数为52的元素x在元素周期表中的位置为_______ 。
(3)上表中o、p两个字母表示的元素的第三电离能分别为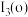 和
和 ,则
,则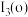
_______  (填“>”或“<”)。理由是
(填“>”或“<”)。理由是_______ 。
(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为_______ (用元素符号表示),第一电离能由大到小排序_______ (用元素符号表示)。

(1)基态o原子的外围电子排布图为
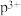 的最外层电子排布式为
的最外层电子排布式为(2)原子序数为52的元素x在元素周期表中的位置为
(3)上表中o、p两个字母表示的元素的第三电离能分别为
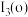 和
和 ,则
,则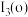
 (填“>”或“<”)。理由是
(填“>”或“<”)。理由是(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是尚未完成的元素周期表,其中a、b、c、d、e、f为元素代号。_______ 。
(2)在上图中标出所有族的序数(示例:IA)_________ 。
(3)在上图中用斜线阴影 标出所有金属元素
标出所有金属元素_______ 。
(4)在元素种类最多的族上方标记★___________ 。
(5)与e原子相邻的四个元素名称是___________ (按原子序数由小到大的顺序)
(6)写出b离子结构示意图___________ 。
(7)b和c两元素的原子以___________ (填化学键类型)形成化合物。
(8)c单质与水反应的现象为:___________ 。
(9)f单质与水反应的化学方程式为:___________ 。
(10)写出c、d元素的最高价氧化物对应的水化物之间发生反应的化学方程式___________ 。

(2)在上图中标出所有族的序数(示例:IA)
(3)在上图中用斜线阴影
 标出所有金属元素
标出所有金属元素(4)在元素种类最多的族上方标记★
(5)与e原子相邻的四个元素名称是
(6)写出b离子结构示意图
(7)b和c两元素的原子以
(8)c单质与水反应的现象为:
(9)f单质与水反应的化学方程式为:
(10)写出c、d元素的最高价氧化物对应的水化物之间发生反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
(1)请写出上述元素d3+的核外电子排布式____________________ ;
(2)请写出e元素的原子电子轨道表示式_____________ ;
(3)ya3分子的电子式________ ,其分子的空间构型是____________ ;
(4)b、e两种元素中,金属性较强的是_______ ,第一电离能大的是___________ (填元素符号);
(5)h的i形成hi2分子杂化类型是____________ ;fh32-的空间构型为_____________ 。
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||
(1)请写出上述元素d3+的核外电子排布式
(2)请写出e元素的原子电子轨道表示式
(3)ya3分子的电子式
(4)b、e两种元素中,金属性较强的是
(5)h的i形成hi2分子杂化类型是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
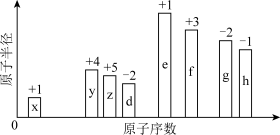
(1)这8种元素中,金属性最强的元素在周期表中的位置是___________ 。
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为___________ (填化学式)。元素z、d、e、f形成的简单离子,半径较大的离子是___________ (填离子符号)。
(3)将化合物eh由固态加热至熔融态,吸收的能量主要用于断裂___________ 键(填“离子”或“共价”)。x与d可形成多种共价分子,其中三原子共价分子的电子式为___________ ;四原子共价分子的结构式为___________ 。
(4)不能作为比较g与h的非金属性强弱的依据是___________。
(5)f的单质与盐酸发生反应的离子方程式为___________ 。

(1)这8种元素中,金属性最强的元素在周期表中的位置是
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为
(3)将化合物eh由固态加热至熔融态,吸收的能量主要用于断裂
(4)不能作为比较g与h的非金属性强弱的依据是___________。
| A.氢化物酸性h强于g |
B.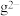 的还原性强于 的还原性强于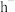 |
| C.与x单质反应,g单质比h单质更困难 |
| D.常温下g单质呈固态,h单质呈气态 |
(5)f的单质与盐酸发生反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】1869年门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。下图为现代元素周期表的一部分,请回答下列问题:
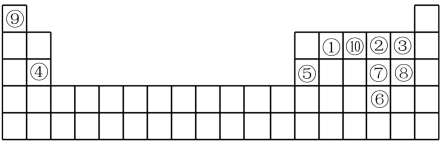
(1)⑤和⑧的最高价氧化物对应的水化物相互反应的离子方程式为:___________ ;
(2)③④⑦⑧的简单离子半径由大到小依次为___________ 。(用离子符号表示)
(3)②与⑨形成 化合物的电子式为
化合物的电子式为___________ 。
(4)由⑧⑨⑩三种元素形成的盐中所含化学键类型有:___________ 。
(5)比较元素③⑦⑧形成的简单气态氢化物的稳定性:___________ (用化学式表示)。

(1)⑤和⑧的最高价氧化物对应的水化物相互反应的离子方程式为:
(2)③④⑦⑧的简单离子半径由大到小依次为
(3)②与⑨形成
 化合物的电子式为
化合物的电子式为(4)由⑧⑨⑩三种元素形成的盐中所含化学键类型有:
(5)比较元素③⑦⑧形成的简单气态氢化物的稳定性:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用下图所示装置(允许加热)验证元素非金属性的变化规律。
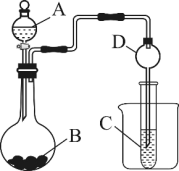
请回答:
(1)仪器A的名称是___________ , 装置D的作用是___________ 。
(2)用药品NaBr、 MnO2、浓盐酸来验证非金属性:Cl>Br,试管C中的现象是___________ ,烧瓶B中发生反应的化学方程式是___________ 。
(3)用药品稀HNO3、碳酸钙、Na2SiO3溶液来验证非金属性:N>C>Si,已知HNO3易挥发,H2SiO3是白色沉淀。该实验装置有一处缺陷, 请写出改进措施___________ ,试管C中的现象是___________ ,发生反应的化学方程式是___________ 。

请回答:
(1)仪器A的名称是
(2)用药品NaBr、 MnO2、浓盐酸来验证非金属性:Cl>Br,试管C中的现象是
(3)用药品稀HNO3、碳酸钙、Na2SiO3溶液来验证非金属性:N>C>Si,已知HNO3易挥发,H2SiO3是白色沉淀。该实验装置有一处缺陷, 请写出改进措施
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、M、W、Q是6种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是_____ 。
(2)X2Q2为______ 化合物(填“离子”或“共价”)。
(3)Z元素的单质是黑火药的主要成分之一,在反应中Z元素的单质表现了_____ 性。
(4)下列能说明M元素比z元素非金属性强的是_____ (填字母标号)。
a.M的气态氢化物的沸点强于Z的
b.M的氧化物对应水化物的酸性强于Z的
c.M的单质与Z的气态氢化物的水溶液反应,使其变浑浊
d.一 定条件下Z、M的单质与Fe反应,产物中铁的价态前者比后者低
(5)科学家们认为存在含氢量最高的化合物WH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式__________ 。
| 元素代号 | X | Y | Z | M | W | Q |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,- 1 | +5,- 3 | -2 |
(1)上述元素中,金属性最强的在周期表中的位置是
(2)X2Q2为
(3)Z元素的单质是黑火药的主要成分之一,在反应中Z元素的单质表现了
(4)下列能说明M元素比z元素非金属性强的是
a.M的气态氢化物的沸点强于Z的
b.M的氧化物对应水化物的酸性强于Z的
c.M的单质与Z的气态氢化物的水溶液反应,使其变浑浊
d.一 定条件下Z、M的单质与Fe反应,产物中铁的价态前者比后者低
(5)科学家们认为存在含氢量最高的化合物WH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,填写下列空格:
(1)比较④⑤⑧的原子半径由大到小依次___________ 。(填元素符号,下同)
(2)元素②与④形成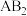 型化合物的电子式为
型化合物的电子式为___________ ,属于___________ 晶体。
(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:___________ ,所得产物中含有的化学键类型有___________ 。
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是___________ 。(填化学式)
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
(2)元素②与④形成
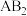 型化合物的电子式为
型化合物的电子式为(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】科学家最近开发了催化剂Mo3S4Fe捕获N2、Na和三甲基硅酰氯[Cl-Si(CH3)3] (用M代表,结构简式如图1)合成[(CH3)3Si]3N (用G代表,结构简式如图2)。
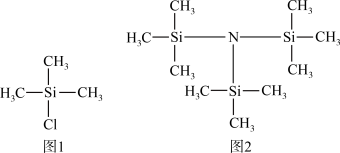
回答下列问题:
(1)基态Mo原子的价层电子排布式为4d55s1,其位于元素周期表_______ 区,最高化合价为_______ 。
(2)1 mol G中采用sp3杂化的原子有_______ mol。已知SiH4中Si—H键的电子云偏向H,G中元素电负性由小到大的顺序为_______ (填元素符号)。在G中Si、N原子构成的立体结构为_______ 。
(3)我国科学家成功研制出超灵敏传感器(MoS2/In2O3)检测气体—NO2。 晶体层状结构如图3所示。
晶体层状结构如图3所示。
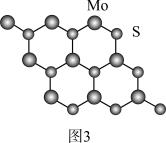
在该结构中Mo原子数、共价键数之比为_______ 。
(4)铵铁蓝广泛用于生产生活中。制备原理如下:
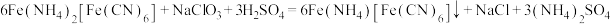
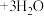
①Fe(NH4)2[Fe(CN)6]中外界的Fe2+比内界的易被氧化,其原因是_______ 。
②1 mol [Fe(CN)6]4-含_______ mol σ键。
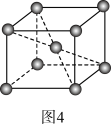
(5)钼晶胞如图4所示。已知两个钼原子最近距离为a cm,设NA为阿伏加德罗常数的值,钼晶体密度为ρ g/cm3。则钼的摩尔质量为_______ g/mol。

回答下列问题:
(1)基态Mo原子的价层电子排布式为4d55s1,其位于元素周期表
(2)1 mol G中采用sp3杂化的原子有
(3)我国科学家成功研制出超灵敏传感器(MoS2/In2O3)检测气体—NO2。
 晶体层状结构如图3所示。
晶体层状结构如图3所示。
在该结构中Mo原子数、共价键数之比为
(4)铵铁蓝广泛用于生产生活中。制备原理如下:
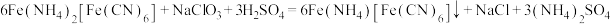
①Fe(NH4)2[Fe(CN)6]中外界的Fe2+比内界的易被氧化,其原因是
②1 mol [Fe(CN)6]4-含
(5)钼晶胞如图4所示。已知两个钼原子最近距离为a cm,设NA为阿伏加德罗常数的值,钼晶体密度为ρ g/cm3。则钼的摩尔质量为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表列出了部分前20号元素的一些性质:
下列问题用元素符号及化学式回答:
(1)②在周期表中的位置是___________ 。
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为___________ 。由①⑨组成的分子中,共含有18e-的化合物结构式为___________ 。
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为___________ 。
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为___________ 。
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 0.37 | 2.27 | 0.74 | 1.52 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +1 | +4 | +5 | +7 | +1 | - | |
| 最低价态 | -1 | - | -2 | - | -4 | -3 | -1 | - | -1 |
(1)②在周期表中的位置是
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】请回答下列问题。
(1)前20号X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为_______ ;若XY2为共价化合物,则其结构式为_______ 。
(2)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是_______ (填“共价化合物”或“离子化合物”),可以证明该判断正确的实验依据是_______ 。
(3)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
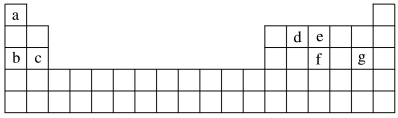
①.元素的原子间最容易形成离子键的是_______ (填字母,下同),容易形成共价键的是_______ 。
Ac和f B.b和g C.d和g D.b和e
②写出a~g七种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式:_______ 。
(1)前20号X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
(2)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是
(3)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:

①.元素的原子间最容易形成离子键的是
Ac和f B.b和g C.d和g D.b和e
②写出a~g七种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。

(1)写出合成NaNO2的化学方程式___________ ,生成1mol NaNO2转移电子___________ mol。
(2)已知NaN3阳离子与阴离子个数比为1∶1,则NaN3中所含的化学键类型为
___________ 、___________ ,1mol该阴离子中所含的电子总数为___________ mol。
(3)上述流程中,操作1的名称为___________ ,试剂1选择___________ 。
(4)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊标准状况下容积为56 L。欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊标准状况下容积为56 L。欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___________ (保留一位小数,不考虑固体的体积)

(1)写出合成NaNO2的化学方程式
(2)已知NaN3阳离子与阴离子个数比为1∶1,则NaN3中所含的化学键类型为

(3)上述流程中,操作1的名称为
(4)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊标准状况下容积为56 L。欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊标准状况下容积为56 L。欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近半年使用:0次



