化合物X由三种元素(其中一种是第四周期元素)组成,某学习小组按如下流程进行实验:
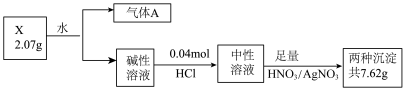
已知:气体A在标准状况下密度为0.714 g∙L-1;碱性溶液焰色试验呈黄色。
请回答:
(1)X的组成元素是___________ (填写元素符号),X的化学式___________ 。
(2)写出X与水反应的化学方程式为___________ 。
(3)两种沉淀中加入1mol/L的适量氨水,一种沉淀溶解请写出相应的化学方程式___________ 。
(4)焰色试验的实验操作___________ 。

已知:气体A在标准状况下密度为0.714 g∙L-1;碱性溶液焰色试验呈黄色。
请回答:
(1)X的组成元素是
(2)写出X与水反应的化学方程式为
(3)两种沉淀中加入1mol/L的适量氨水,一种沉淀溶解请写出相应的化学方程式
(4)焰色试验的实验操作
更新时间:2023-05-04 16:52:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为常见的金属单质,根据下图所示的关系:
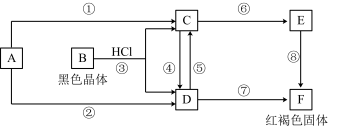
(1)确定A、C、E的化学式:
A.____________ , C.____________ , F.____________ 。
(2)写出反应⑧的化学方程式___________________________________ ,
反应④、⑤的离子方程式______________________ 、______________________ 。

(1)确定A、C、E的化学式:
A.
(2)写出反应⑧的化学方程式
反应④、⑤的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由地壳中含量最多的金属元素组成的单质,反应⑦为置换反应,D为红棕色固体,K是一种红棕色气体,C是一种强酸。

请填写下列空白:
(1)已知M为硝酸亚铁,写出下列物质的化学式:B:___________ E:___________ 。
(2)写出反应④的离子方程式:___________ 。
(3)在反应②、③、⑥、⑧、⑨中既属于化合反应又属于氧化还原反应的___________ (填写序号)。
(4)C的浓溶液可使蓝色的胆矾晶体变为白色粉末,此现象体现了C的___________ 性。
(5)将化合物D与KNO3、KOH高温共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。写出该反应的化学方程式:___________ 。

请填写下列空白:
(1)已知M为硝酸亚铁,写出下列物质的化学式:B:
(2)写出反应④的离子方程式:
(3)在反应②、③、⑥、⑧、⑨中既属于化合反应又属于氧化还原反应的
(4)C的浓溶液可使蓝色的胆矾晶体变为白色粉末,此现象体现了C的
(5)将化合物D与KNO3、KOH高温共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知:单质A为目前人类使用最广泛的金属,氧化物B为具有磁性的黑色晶体,根据下列转化关系填空。
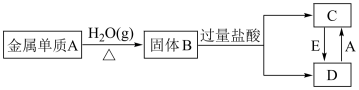
(1)试判断:A的化学式为___________ ,B的名称为___________ 。
(2)若E是一种黄绿色气体单质,该气体是___________ ,在C→D过程中,此气体做___________ 剂。
(3)实验室检验D溶液中的阳离子时,通常可滴加___________ ,可观察到的现象是___________ 。
(4)写出D+A→C的离子方程式___________ 。

(1)试判断:A的化学式为
(2)若E是一种黄绿色气体单质,该气体是
(3)实验室检验D溶液中的阳离子时,通常可滴加
(4)写出D+A→C的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某兴趣小组对化合物X开展探究实验,其中,X由4种元素组成,遇水即分解,混合溶液呈碱性,气体C可使湿润的红色石蕊试纸变蓝色。
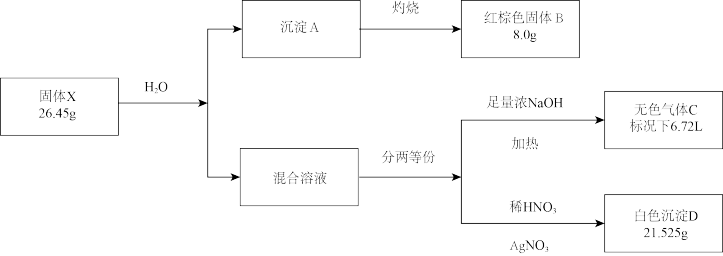
(1)X与水反应的方程式:_______ 。
(2)新制的A略显两性,能溶于强碱NaOH溶液中,化学方程式为_______ 。
(3)下列关于氯化铁的用途及性质说法错误的是_______ 。
A.利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释至所需浓度
B.在印刷制版中用作铜版的腐蚀剂
C.在某些反应中作催化剂
D.在医药上用作伤口的止血剂,它能导致蛋白质的迅速变性,所以用来止血
E.气体C与FeCl3溶液可以制备X
F.Fe(OH)3胶体的制备:向沸水中加入FeCl3的饱和溶液,继续煮沸至溶液呈红褐色,停止加热
G.除去FeCl2中少量FeCl3杂质,可向混合液中加足量铁粉过滤即可

(1)X与水反应的方程式:
(2)新制的A略显两性,能溶于强碱NaOH溶液中,化学方程式为
(3)下列关于氯化铁的用途及性质说法错误的是
A.利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释至所需浓度
B.在印刷制版中用作铜版的腐蚀剂
C.在某些反应中作催化剂
D.在医药上用作伤口的止血剂,它能导致蛋白质的迅速变性,所以用来止血
E.气体C与FeCl3溶液可以制备X
F.Fe(OH)3胶体的制备:向沸水中加入FeCl3的饱和溶液,继续煮沸至溶液呈红褐色,停止加热
G.除去FeCl2中少量FeCl3杂质,可向混合液中加足量铁粉过滤即可
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制备Cl2通常采用如图所示装置:
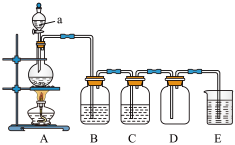
(1)A装置中发生反应的化学方程式是________ ;每生成0.5 mol Cl2,被氧化的物质的物质的量是_____ mol。
(2)仪器a的名称是_________ ;
(3)B装置中所盛的试剂是________________ ;
(4)实验时,通常采用密度为1.19 g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为________ ;
(5)将如图装置代替装置D和E,可进行“氯气与金属钠反应”的实验,以下叙述正确的是________ 。
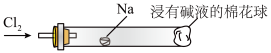
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气
C. 玻璃管中,钠燃烧时会产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
(6)E装置中发生反应的化学方程式是________________ ;为验证E装置反应后的溶液中存在Cl-,正确的操作是_____________ 。

(1)A装置中发生反应的化学方程式是
(2)仪器a的名称是
(3)B装置中所盛的试剂是
(4)实验时,通常采用密度为1.19 g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为
(5)将如图装置代替装置D和E,可进行“氯气与金属钠反应”的实验,以下叙述正确的是

A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气
C. 玻璃管中,钠燃烧时会产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
(6)E装置中发生反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】由难溶性磷酸锂渣(主要成分为Li3PO4)为原料制备电池级Li2CO3的流程如下:

已知:①Li2CO3在不同温度下的溶解度: 0℃ 1.54g,20℃ 1.33g, 90℃ 0.78g。
②碳酸锂:水溶液煮沸时容易发生水解。
(1)溶解除磷。将一定量磷酸锂渣与CaCl2溶液、盐酸中的一种配成悬浊液,加入到三颈烧瓶中(装置如图),一段时间后,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤,得到LiCl溶液。
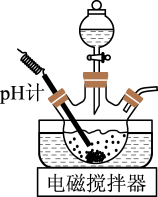
①滴液漏斗中的液体是_______ 。
②Li3PO4转化为LiCl和CaHPO4的离子方程式为_______ 。
(2)除钙。通过离子交换法除去溶液中Ca2+。若要使后续得到的Li2CO3 中不含CaCO3(设沉淀后溶液中Li+浓度为0.1 mol·L-1),需控制除钙后溶液中c(Ca2+)≤_______ 。[Ksp(Li2CO3)=2.5×10-2,Ksp(CaCO3)=2.8×10-9]
(3)制备Li2CO3。向除杂后的LiCl溶液中加入N235萃取剂(50%三辛癸烷基叔胺与50% ,异辛醇的混合液),边搅拌边向混合液中通CO2,过滤洗涤得到Li2CO3。
①方法能制得Li2CO3的原因是_______ 。
②检验滤渣是否洗涤完全的实验方法是_______ 。
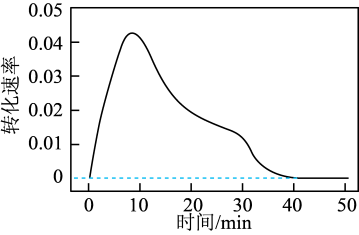
(4)若粗品碳酸锂中含少量难溶性杂质,为获得较高产率的纯Li2CO3,请补充完整实验 方案:向粗品Li2CO3中加水,按一定速率通入CO2,边通边搅拌,_______ 。(已知:①LiHCO3受热易分解;②实验过程中Li2CO3转化速率与时间的关系图如图所示。)

已知:①Li2CO3在不同温度下的溶解度: 0℃ 1.54g,20℃ 1.33g, 90℃ 0.78g。
②碳酸锂:水溶液煮沸时容易发生水解。
(1)溶解除磷。将一定量磷酸锂渣与CaCl2溶液、盐酸中的一种配成悬浊液,加入到三颈烧瓶中(装置如图),一段时间后,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤,得到LiCl溶液。

①滴液漏斗中的液体是
②Li3PO4转化为LiCl和CaHPO4的离子方程式为
(2)除钙。通过离子交换法除去溶液中Ca2+。若要使后续得到的Li2CO3 中不含CaCO3(设沉淀后溶液中Li+浓度为0.1 mol·L-1),需控制除钙后溶液中c(Ca2+)≤
(3)制备Li2CO3。向除杂后的LiCl溶液中加入N235萃取剂(50%三辛癸烷基叔胺与50% ,异辛醇的混合液),边搅拌边向混合液中通CO2,过滤洗涤得到Li2CO3。
①方法能制得Li2CO3的原因是
②检验滤渣是否洗涤完全的实验方法是
(4)若粗品碳酸锂中含少量难溶性杂质,为获得较高产率的纯Li2CO3,请补充完整实验 方案:向粗品Li2CO3中加水,按一定速率通入CO2,边通边搅拌,

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】 和
和 锂离子电池的电极材料,可利用钛铁矿(主要成分为
锂离子电池的电极材料,可利用钛铁矿(主要成分为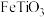 ,还含有少量
,还含有少量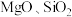 等杂质)来制备,工艺流程如图:
等杂质)来制备,工艺流程如图:
(1)化学上某些盐可写成氧化物的形式,如: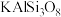 可写成
可写成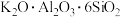 ,则
,则 可写成
可写成____________ 。
(2)“酸浸”后,钛主要以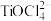 存在,写出相应反应的离子方程式:
存在,写出相应反应的离子方程式:____________ 。
(3)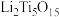 中Ti的化合价为
中Ti的化合价为 ,
,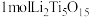 中含有过氧键的数目为
中含有过氧键的数目为____________ 。
(4) 与双氧水、氨水反应40min,控制温度在40℃左右,温度不能高于40℃的原因是
与双氧水、氨水反应40min,控制温度在40℃左右,温度不能高于40℃的原因是____________ 。
(5)向“滤液②”中加入双氧水和磷酸得到 ,写出离子方程式:
,写出离子方程式:____________ 。
(6)在“高温煅烧②”过程中,适当多加草酸的原因为____________ 。
(7)锂离子电池放电时, 由
由 结合
结合 得到,在
得到,在 中,若
中,若 ,材料中
,材料中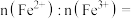
____________ .
 和
和 锂离子电池的电极材料,可利用钛铁矿(主要成分为
锂离子电池的电极材料,可利用钛铁矿(主要成分为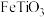 ,还含有少量
,还含有少量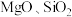 等杂质)来制备,工艺流程如图:
等杂质)来制备,工艺流程如图: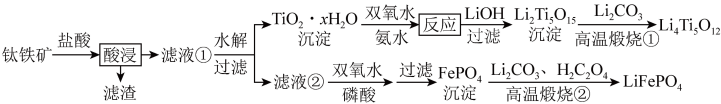
(1)化学上某些盐可写成氧化物的形式,如:
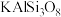 可写成
可写成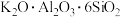 ,则
,则 可写成
可写成(2)“酸浸”后,钛主要以
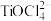 存在,写出相应反应的离子方程式:
存在,写出相应反应的离子方程式:(3)
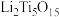 中Ti的化合价为
中Ti的化合价为 ,
,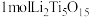 中含有过氧键的数目为
中含有过氧键的数目为(4)
 与双氧水、氨水反应40min,控制温度在40℃左右,温度不能高于40℃的原因是
与双氧水、氨水反应40min,控制温度在40℃左右,温度不能高于40℃的原因是(5)向“滤液②”中加入双氧水和磷酸得到
 ,写出离子方程式:
,写出离子方程式:(6)在“高温煅烧②”过程中,适当多加草酸的原因为
(7)锂离子电池放电时,
 由
由 结合
结合 得到,在
得到,在 中,若
中,若 ,材料中
,材料中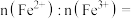
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氨气的用途众多,被广泛应用于化工、轻工、制药、合成纤维等领域,在各个领域都有它的价值体现,某化学兴趣小组利用如图装置制备氨气并探究相关性质。

根据要求回答下列问题:
(1)兴趣小组组装好实验装置后,在加药品前应先进行的操作是_______ 。
(2)A为实验室制备氨气的发生装置,其化学方程式为_______ 。
(3)B中U型干燥管所盛放物质的名称是_______ 。
(4)实验中发现D中无水硫酸铜变蓝,证明_______ ;C中粉末变为红色单质,乙醇在加热和有此单质存在的条件下,可以被空气中的氧气氧化,请写出乙醇发生此反应的化学方程式_______ 。
(5)若将氨气和二氧化硫气体按2:1的体积比同时通入到盛有适量BaCl2溶液的试管中,可观察到_______ 。
(6)从“绿色化学”的角度出发,该装置还存在的缺陷是_______ 。

根据要求回答下列问题:
(1)兴趣小组组装好实验装置后,在加药品前应先进行的操作是
(2)A为实验室制备氨气的发生装置,其化学方程式为
(3)B中U型干燥管所盛放物质的名称是
(4)实验中发现D中无水硫酸铜变蓝,证明
(5)若将氨气和二氧化硫气体按2:1的体积比同时通入到盛有适量BaCl2溶液的试管中,可观察到
(6)从“绿色化学”的角度出发,该装置还存在的缺陷是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有关物质的转化关系如下图所示。A是红棕色固体,B是常见的强酸,C是常见的无色液体。E、F均为无色有刺激性气味的气体,其中E能使品红溶液褪色。G可用作补血剂,I是一种白色固体,在空气中最终变成红褐色。请回答下列问题:

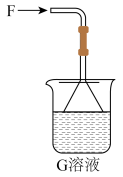
(1)F的电子式为_____ 。
(2)写出反应②的离子方程式,并用单线桥标出电子转移的方向和数目_____ 。
(3)可确定反应②中金属离子已完全反应的试剂为_____ (填化学式)。反应③的装置如上图所示,倒置漏斗的作用是_____ 。
(4)写出反应③的离子方程式:_____ 。


(1)F的电子式为
(2)写出反应②的离子方程式,并用单线桥标出电子转移的方向和数目
(3)可确定反应②中金属离子已完全反应的试剂为
(4)写出反应③的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
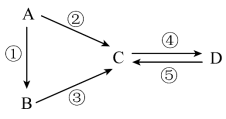
【推荐1】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:___________ 。
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:___________ 。
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某稀溶液含下列离子中的4种,且各种离子的物质的量均为0.01mol
阳离子 K+、Ba2+ 、Fe2+、Al3+、Fe3+
阴离子 OH-、CO32-、Cl-、NO3-、 SO42-
若向原溶液中加入足量的盐酸,只有一种气体生成,且在空气中会迅速变为红棕色。向原溶液中加入Ba(NO3)2后产生沉淀,过滤,加入HNO3酸化的AgNO3后无白色沉淀生成。
(1)溶液中______________ (填“一定”,“一定不”,“可能”)含有CO32-,理由是_____________
(2)将溶液进行焰色反应看到的现象是_____________
(3)写出生成的气体在空气中迅速变为红棕色的化学方程式_____________
(4)原溶液中阴离子为_______________ ,阳离子为_____________
(5)向原溶液中加入足量的盐酸,有无色气体生成的离子方程式为_____________
阳离子 K+、Ba2+ 、Fe2+、Al3+、Fe3+
阴离子 OH-、CO32-、Cl-、NO3-、 SO42-
若向原溶液中加入足量的盐酸,只有一种气体生成,且在空气中会迅速变为红棕色。向原溶液中加入Ba(NO3)2后产生沉淀,过滤,加入HNO3酸化的AgNO3后无白色沉淀生成。
(1)溶液中
(2)将溶液进行焰色反应看到的现象是
(3)写出生成的气体在空气中迅速变为红棕色的化学方程式
(4)原溶液中阴离子为
(5)向原溶液中加入足量的盐酸,有无色气体生成的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】用废易拉罐(主要成分为Al,少量Fe等)制取明矾的实验流程如下:
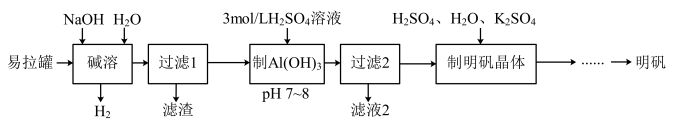
(1)铝位于周期表第________ 周期________ 族。
(2)检验明矾中K+的方案是:用洁净的铂丝蘸取明矾少许,在酒精灯火焰上灼烧,_______ ,说明含有K+。
(3)配制100mL 3mol·L-1H2SO4溶液所需的玻璃仪器有:量筒、烧杯、玻璃棒、______ 和_____ 。
(4)写出“碱溶”时铝转化为偏铝酸钠的离子方程式:___________ 。

(1)铝位于周期表第
(2)检验明矾中K+的方案是:用洁净的铂丝蘸取明矾少许,在酒精灯火焰上灼烧,
(3)配制100mL 3mol·L-1H2SO4溶液所需的玻璃仪器有:量筒、烧杯、玻璃棒、
(4)写出“碱溶”时铝转化为偏铝酸钠的离子方程式:
您最近一年使用:0次



