到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是___________ (填字母)。
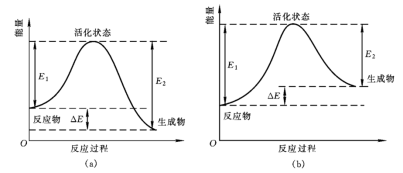
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量___________ kJ。
(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是___________ 。
(4)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
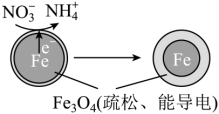
①作负极的物质是___________ 。
②正极的电极反应式是___________ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是
(4)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
更新时间:2023-05-10 13:54:35
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应中均伴随着能量的变化,回答下列问题:
(1)某同学进行如下实验,图①和②中温度计示数降低的是_______ ;
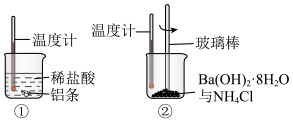
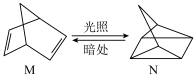
(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是_______ ;
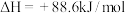
(3)已知 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
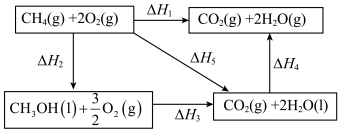
(4)金属Ni可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是_______。
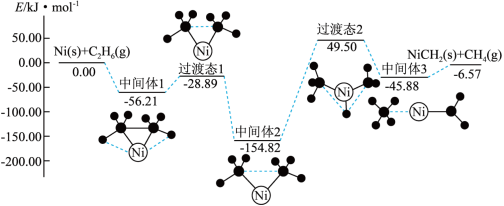
(5) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
_______ kJ/mol。
(6)在25℃、101kPa下,1g乙烷气体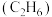 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为_______ 。
(7)中和热的测定实验中,取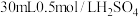 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为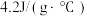 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
_______ kJ/mol。
(1)某同学进行如下实验,图①和②中温度计示数降低的是

(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是

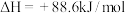
(3)已知
 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
A. | B.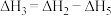 |
C. | D. |
(4)金属Ni可活化
 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是_______。
| A.中间体1→中间体2的过程是放热过程 |
| B.加入催化剂可降低该反应的反应热,加快反应速率 |
C.1molNi和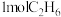 的总能量小于 的总能量小于 和 和 的总能量 的总能量 |
| D.中间体2→中间体3的过程是决速步骤 |
(5)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
| 化学键 |  |  |  | 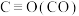 |
| 键能/(kJ/mol) | 413 | 745 | 436 | 1075 |
(6)在25℃、101kPa下,1g乙烷气体
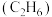 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为(7)中和热的测定实验中,取
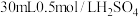 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为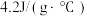 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为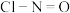 )是有机合成中的重要试剂。它可由
)是有机合成中的重要试剂。它可由 和NO在通常条件下反应制得,反应方程式为
和NO在通常条件下反应制得,反应方程式为 。已知几种化学键的键能数据如下表所示:
。已知几种化学键的键能数据如下表所示:
当 与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为
与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为_______ kJ;
(2)在一个恒容密闭容器中投入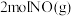 和
和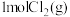 发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
①T1_______ T2(填“>“”<”或”=”);
②温度为T2℃时,起始时容器内的强为p0,则该反应的平衡常数Kp=_____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示
),其工作原理如图所示
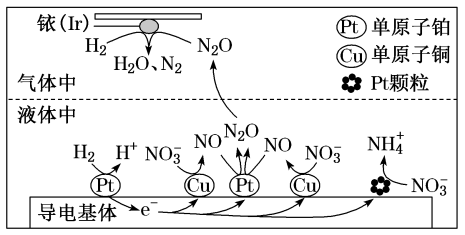
Ir表面发生反应的方程式为_______ ;
II.利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来精炼银,装置如图所示
制成燃料电池,模拟工业电解法来精炼银,装置如图所示
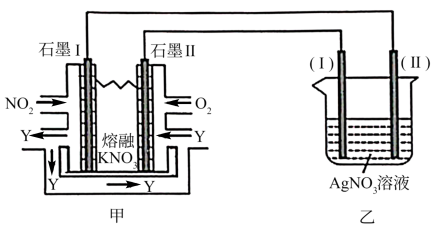
请回答下列问题:
(4)甲池工作时, 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用,则石墨II附近发生的电极反应式为
,可循环使用,则石墨II附近发生的电极反应式为_______ 。
(1)亚硝酸氯(结构式为
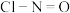 )是有机合成中的重要试剂。它可由
)是有机合成中的重要试剂。它可由 和NO在通常条件下反应制得,反应方程式为
和NO在通常条件下反应制得,反应方程式为 。已知几种化学键的键能数据如下表所示:
。已知几种化学键的键能数据如下表所示:| 化学键 | Cl—Cl | Cl—N | N—O | N—O(NO) |
| 键能(kJ/mol) | 243 | 200 | 607 | 630 |
 与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为
与NO反应生成ClNO的过程中转移了5mol电子,理论上放出的热量为(2)在一个恒容密闭容器中投入
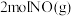 和
和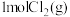 发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示t/min 温度/℃ | 0 | 5 | 8 | 13 |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
②温度为T2℃时,起始时容器内的强为p0,则该反应的平衡常数Kp=
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(
 ),其工作原理如图所示
),其工作原理如图所示
Ir表面发生反应的方程式为
II.利用电化学原理,将
 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来精炼银,装置如图所示
制成燃料电池,模拟工业电解法来精炼银,装置如图所示
请回答下列问题:
(4)甲池工作时,
 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用,则石墨II附近发生的电极反应式为
,可循环使用,则石墨II附近发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】铁是生产生活中应用最广泛的金属,炼铁技术备受关注,已知:
①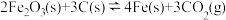
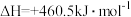
②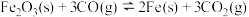
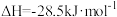
③断裂 气体中的化学键需要吸收1076kJ的能量,断裂
气体中的化学键需要吸收1076kJ的能量,断裂 气体中的化学键需要吸收1490kJ的能量。
气体中的化学键需要吸收1490kJ的能量。
请回答:
(1)断裂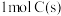 中所有化学键需要吸收的能量为
中所有化学键需要吸收的能量为________ kJ。
(2)T1℃时,向密闭容器中加入一定量的 和C,发生反应①,达到平衡后
和C,发生反应①,达到平衡后 的浓度为
的浓度为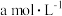 ;其他条件不变,缩小容器体积,再次达到平衡时,
;其他条件不变,缩小容器体积,再次达到平衡时, 的浓度为
的浓度为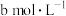 ,则a
,则a________ b(选填“>”“<”或“=”)。
(3)起始温度均为T2℃时,向容积为10L的三个恒容密闭容器中,分别加入一定量的 和CO发生反应②,测得相关数据如表所示:
和CO发生反应②,测得相关数据如表所示:
①T2℃时,容器1中反应的平衡常数K1=_______ 。
②容器2中,5min达到平衡,则0~5min以 表示该反应的速率
表示该反应的速率
___________ 。
③对于三个容器中的反应,下列说法正确的是(填字母)_________ 。
A. B.容器1和容器2中
B.容器1和容器2中 的平衡转化率
的平衡转化率
C.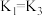 D.平衡时气体压强:
D.平衡时气体压强: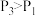
(4)一定条件下,向恒压密闭容器中充入0.5mol 和1.0mol CO,发生反应②,CO和
和1.0mol CO,发生反应②,CO和 的物质的量浓度(c)与时间(t)的关系如图所示:
的物质的量浓度(c)与时间(t)的关系如图所示:
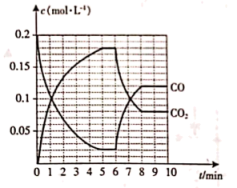
①6min时改变的外界条件为________________ 。
②若在6min时,恒温将容器体积扩大到10L,请在图中画出6~10min 的物质的量浓度随时间变化的曲线
的物质的量浓度随时间变化的曲线_________ 。
①
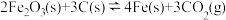
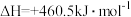
②
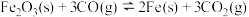
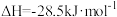
③断裂
 气体中的化学键需要吸收1076kJ的能量,断裂
气体中的化学键需要吸收1076kJ的能量,断裂 气体中的化学键需要吸收1490kJ的能量。
气体中的化学键需要吸收1490kJ的能量。请回答:
(1)断裂
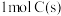 中所有化学键需要吸收的能量为
中所有化学键需要吸收的能量为(2)T1℃时,向密闭容器中加入一定量的
 和C,发生反应①,达到平衡后
和C,发生反应①,达到平衡后 的浓度为
的浓度为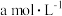 ;其他条件不变,缩小容器体积,再次达到平衡时,
;其他条件不变,缩小容器体积,再次达到平衡时, 的浓度为
的浓度为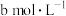 ,则a
,则a(3)起始温度均为T2℃时,向容积为10L的三个恒容密闭容器中,分别加入一定量的
 和CO发生反应②,测得相关数据如表所示:
和CO发生反应②,测得相关数据如表所示:| 编号 | 容器 | 起始时物质的量/mol | 平衡时物质的量/mol | 平衡常数(K) | |
 |  |  | |||
| 1 | 恒温 | 0.5 | 1.5 | 0.8 | K1 |
| 2 | 恒温 | 2 | 3 | M | K2 |
| 3 | 绝热 | 1 | 1.5 | n | K3 |
①T2℃时,容器1中反应的平衡常数K1=
②容器2中,5min达到平衡,则0~5min以
 表示该反应的速率
表示该反应的速率
③对于三个容器中的反应,下列说法正确的是(填字母)
A.
 B.容器1和容器2中
B.容器1和容器2中 的平衡转化率
的平衡转化率
C.
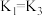 D.平衡时气体压强:
D.平衡时气体压强: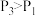
(4)一定条件下,向恒压密闭容器中充入0.5mol
 和1.0mol CO,发生反应②,CO和
和1.0mol CO,发生反应②,CO和 的物质的量浓度(c)与时间(t)的关系如图所示:
的物质的量浓度(c)与时间(t)的关系如图所示:
①6min时改变的外界条件为
②若在6min时,恒温将容器体积扩大到10L,请在图中画出6~10min
 的物质的量浓度随时间变化的曲线
的物质的量浓度随时间变化的曲线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】近年随着现代工业的发展,二氧化氮的排放量大增,二氧化氮对臭氧空洞的形成起着重要作用,同时还是光化学烟雾和酸雨的成因之一。如何实现二氧化氮的转化利用成为了科学家研究的课题。回答下列问题:
(1) 催化
催化 生成
生成 的过程可分为三步:
的过程可分为三步:
第一步: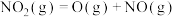 :
:
第三步: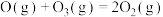 。
。
则第二步的反应方程式为_______ 。
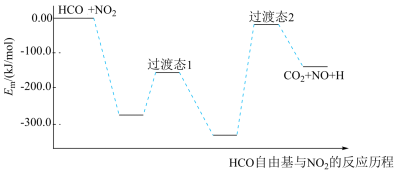
(2)科学家测得HCO自由基还原二氧化氮的反应机理如图所示,两种过渡态物质相比,_______ (填“过渡态1”或“过渡态2”)较稳定,该反应分_______ 步进行,决定该反应速率的是第_______ 步。
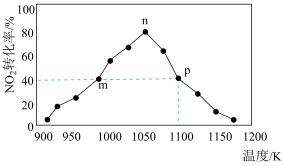
(3)科学家尝试采用焦炭还原法消除二氧化氮污染,反应原理为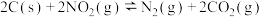 ,在2L恒容密闭容器中加入足量的碳和2mol
,在2L恒容密闭容器中加入足量的碳和2mol  气体,相同时间内测得二氧化氮的转化率随温度变化如图所示,图中m、n、p三点平衡常数由大到小的顺序为
气体,相同时间内测得二氧化氮的转化率随温度变化如图所示,图中m、n、p三点平衡常数由大到小的顺序为_______ ,p点化学反应平衡常数为_______ (计算结果保留两位小数)。
(4)工业上采用CO还原 生成两种大气成分消除污染,若完全还原2mol
生成两种大气成分消除污染,若完全还原2mol  时该反应的正反应活化能为
时该反应的正反应活化能为 ,逆反应活化能为
,逆反应活化能为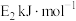 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:_______ 。下列关于该反应的说法正确的是_______ (填选项字母)。
A.恒温恒压下,体系内混合气体密度不随时间变化时,反应达到平衡状态
B.恒温恒容下,平衡后,充入惰性气体, 的平衡转化率增大
的平衡转化率增大
C.恒温恒压下,再按照原比例加入相同量的反应物, 的平衡转化率增大
的平衡转化率增大
D.及时分离出 ,逆反应速率减小,正反应速率增大,平衡正向移动
,逆反应速率减小,正反应速率增大,平衡正向移动
(1)
 催化
催化 生成
生成 的过程可分为三步:
的过程可分为三步:第一步:
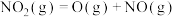 :
:第三步:
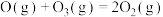 。
。则第二步的反应方程式为
(2)科学家测得HCO自由基还原二氧化氮的反应机理如图所示,两种过渡态物质相比,

(3)科学家尝试采用焦炭还原法消除二氧化氮污染,反应原理为
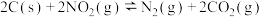 ,在2L恒容密闭容器中加入足量的碳和2mol
,在2L恒容密闭容器中加入足量的碳和2mol  气体,相同时间内测得二氧化氮的转化率随温度变化如图所示,图中m、n、p三点平衡常数由大到小的顺序为
气体,相同时间内测得二氧化氮的转化率随温度变化如图所示,图中m、n、p三点平衡常数由大到小的顺序为
(4)工业上采用CO还原
 生成两种大气成分消除污染,若完全还原2mol
生成两种大气成分消除污染,若完全还原2mol  时该反应的正反应活化能为
时该反应的正反应活化能为 ,逆反应活化能为
,逆反应活化能为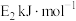 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:A.恒温恒压下,体系内混合气体密度不随时间变化时,反应达到平衡状态
B.恒温恒容下,平衡后,充入惰性气体,
 的平衡转化率增大
的平衡转化率增大C.恒温恒压下,再按照原比例加入相同量的反应物,
 的平衡转化率增大
的平衡转化率增大D.及时分离出
 ,逆反应速率减小,正反应速率增大,平衡正向移动
,逆反应速率减小,正反应速率增大,平衡正向移动
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
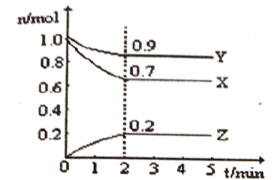
【推荐2】Ⅰ、(1)反应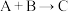 (吸热)分两步进行①
(吸热)分两步进行①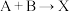 (放热);②
(放热);② (吸热)。下列示意图中,能正确表示总反应过程中能量变化的是
(吸热)。下列示意图中,能正确表示总反应过程中能量变化的是___________ 。
A.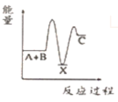 B.
B.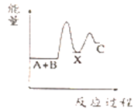
C.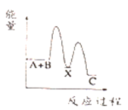 D.
D.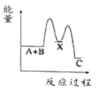
(2)合成氨工业中,合成塔中每产生 ,放出46.1kJ热量,已知(见图):则
,放出46.1kJ热量,已知(见图):则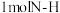 键断裂吸收的能量约等于
键断裂吸收的能量约等于___________ kJ。

Ⅱ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
(1)该反应的化学方程式为___________ ;
(2)混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”)平衡时容器内混合气体密度比起始时___________ (填“大”,“小”或“相等”)
(3)反应开始至2min,开始时的压强与此时体系内压强之比为___________ ;
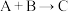 (吸热)分两步进行①
(吸热)分两步进行①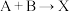 (放热);②
(放热);② (吸热)。下列示意图中,能正确表示总反应过程中能量变化的是
(吸热)。下列示意图中,能正确表示总反应过程中能量变化的是A.
 B.
B.
C.
 D.
D.
(2)合成氨工业中,合成塔中每产生
 ,放出46.1kJ热量,已知(见图):则
,放出46.1kJ热量,已知(见图):则 键断裂吸收的能量约等于
键断裂吸收的能量约等于
Ⅱ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为
(2)混合气体的平均相对分子质量比起始时
(3)反应开始至2min,开始时的压强与此时体系内压强之比为
您最近一年使用:0次
【推荐3】运用化学反应原理研究碳、氮等元素的单质及其化合物的反应有重要意义。
(1)如图表示金刚石、石墨在相关反应过程中的能量变化关系。写出石墨转化为金刚石的热化学方程式:____________________ 。
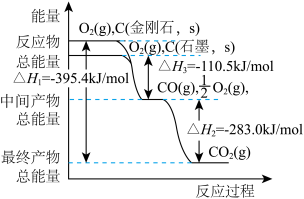
(2)CO与H2可在一定条件下反应生成燃料甲醇:CO(g)+2H2(g) CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。
CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。
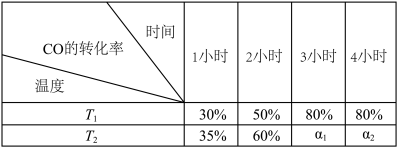
则温度为T1时该反应的平衡常数为____________ 。a1、a2、80%三者的大小关系为______________ 。根据温度为T1时的数据作出的下列判断中正确的是__________ 。
A.反应在2小时的时候混合气体的密度和相对分子质量均比1小时的大
B.反应在3小时的时候,v正(H2)=2v逆(CH3OH)
C.若其他条件不变,再充入6 mol H2,则最多可得到64 g CH3OH
D.其他条件不变,若最初加入的H2为2.4 mol,则达平衡时CO的转化率为50%
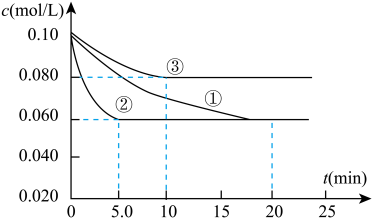
(3)工业中常用以下反应合成氨:N2(g)+3H2(g) 2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:
2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:_______ ;②相对于①条件不同,②的条件是______ ,理由是___________________ 。
(1)如图表示金刚石、石墨在相关反应过程中的能量变化关系。写出石墨转化为金刚石的热化学方程式:

(2)CO与H2可在一定条件下反应生成燃料甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。
CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。
则温度为T1时该反应的平衡常数为
A.反应在2小时的时候混合气体的密度和相对分子质量均比1小时的大
B.反应在3小时的时候,v正(H2)=2v逆(CH3OH)
C.若其他条件不变,再充入6 mol H2,则最多可得到64 g CH3OH
D.其他条件不变,若最初加入的H2为2.4 mol,则达平衡时CO的转化率为50%
(3)工业中常用以下反应合成氨:N2(g)+3H2(g)
 2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:
2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
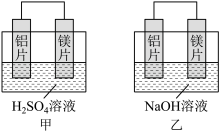
(1)写出甲中正极的电极反应式:_______
(2)乙中负极为_______ , 总反应的离子方程式:_______
(3)由此实验得出的下列结论中,正确的有_______
II.利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:
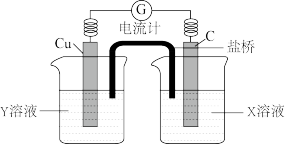
(4)写出电极反应式:正极_______ ;负极_______ 。
(5)图中X溶液是_______ ,Y溶液是_______ 。

(1)写出甲中正极的电极反应式:
(2)乙中负极为
(3)由此实验得出的下列结论中,正确的有_______
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
II.利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:

(4)写出电极反应式:正极
(5)图中X溶液是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(I)某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
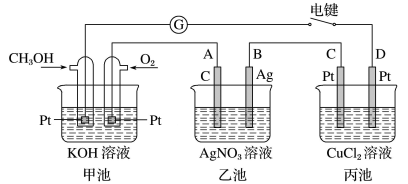
请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”),通入CH3OH电极的电极反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),乙池总反应式为_______ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为_______ mL(标准状况下),丙池中析出_______ g铜。
(II)氯碱工业是高能耗产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。
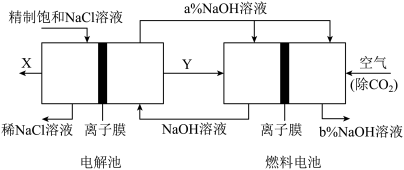
(4)图中X_______ (填化学式)比较图示中a%与b%的大小_______ 。
(5)写出燃料电池中的电极反应式:负极电极反应式_______
(6)当生成的X气体为2mol时,理论上通入空气的体积(标况)为_______ L

请回答下列问题:
(1)甲池为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
(II)氯碱工业是高能耗产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。

(4)图中X
(5)写出燃料电池中的电极反应式:负极电极反应式
(6)当生成的X气体为2mol时,理论上通入空气的体积(标况)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:_______ 。
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为_______ 。
综合上述实验,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(2)采用电化学装置进行验证。
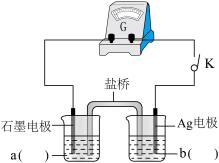
小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为_______ 溶液;b为_______ 溶液;(写a、b化学式)
ii.再向左侧烧杯中滴加较浓的_______ 溶液,产生的现象为_______ 。表明“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为
综合上述实验,证实“Ag++Fe2+
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(2)采用电化学装置进行验证。

小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为
ii.再向左侧烧杯中滴加较浓的
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知原子序数依次增大的前四周期五种常见元素X、Y、Z、W、R,其相关信息如下:X的原子结构中,最外层电子数是内层电子数的2倍;Z形成的多种同素异形体,其中之一是地球生物的“保护伞”;W的一种单质是黄色粉末,难溶于水,易溶于二硫化碳;R单质在氯气中燃烧会产生棕黄色的烟,该烟溶于少量水中显绿色。
(1)X在元素周期表中的位置:______ ,该族元素易形成______ (填写“离子”或“共价”)化合物。
(2)Y的简单氢化物遇到 可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为
可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为________ 。写出该“白烟”的电子式:________ 。
(3)写出Y与Z形成的化合物对环境的影响:__________ (写出一条即可)。
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,其原因是__________ (用离子方程式表示)。
(5)W的简单氢化物与Z的单质在烧碱溶液中可以形成燃料电池(产物中无沉淀生成),写出负极反应式:____________ 。
(6) 投入足量的某浓度的硝酸中,所得气体产物为NO和
投入足量的某浓度的硝酸中,所得气体产物为NO和 的混合物,且体积比为1:1,发生反应的化学方程式为:
的混合物,且体积比为1:1,发生反应的化学方程式为:_____________ 。
(1)X在元素周期表中的位置:
(2)Y的简单氢化物遇到
 可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为
可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为(3)写出Y与Z形成的化合物对环境的影响:
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,其原因是
(5)W的简单氢化物与Z的单质在烧碱溶液中可以形成燃料电池(产物中无沉淀生成),写出负极反应式:
(6)
 投入足量的某浓度的硝酸中,所得气体产物为NO和
投入足量的某浓度的硝酸中,所得气体产物为NO和 的混合物,且体积比为1:1,发生反应的化学方程式为:
的混合物,且体积比为1:1,发生反应的化学方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】一种磁性材料的磨削废料主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍的工艺流程如图,回答下列问题:
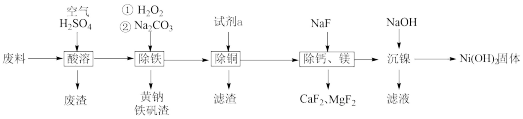
(1)镍元素所在的第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色,下列离子形成的水合离子为无色的是_______(填序号)。
(2)“酸溶”时产生的废渣主要成分为_______ 。
(3)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢通入空气,写出金属镍溶解生成 的离子方程式:
的离子方程式:_______ 。
(4)“除铁”时为了证明添加的 已足量,应选择的试剂是
已足量,应选择的试剂是_______ 。
(5)“除铜”时,试剂a最好选用_______ (填序号),其优点有_______ (至少答两点)。
A. B.
B. C.NaOH D.FeS
C.NaOH D.FeS
(6)“除钙、镁”时,在完全除去钙、镁离子时,溶液中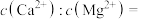
_______ 。
(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下: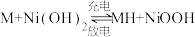 (式中M为储氢合金),写出电池放电过程中正极的电极反应式:
(式中M为储氢合金),写出电池放电过程中正极的电极反应式:_______ ,用该电池及惰性电极电解一定量饱和食盐水,在阴阳两极分别收集到78.4L和33.6L气体(标准状况下),则电池负极质量变化量为_______ 。

| 物质 |  |  | CuS |  |  |
 | 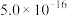 |  | 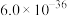 |  | 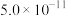 |
(1)镍元素所在的第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色,下列离子形成的水合离子为无色的是_______(填序号)。
A. | B. | C. | D. |
(3)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢通入空气,写出金属镍溶解生成
 的离子方程式:
的离子方程式:(4)“除铁”时为了证明添加的
 已足量,应选择的试剂是
已足量,应选择的试剂是(5)“除铜”时,试剂a最好选用
A.
 B.
B. C.NaOH D.FeS
C.NaOH D.FeS(6)“除钙、镁”时,在完全除去钙、镁离子时,溶液中
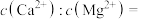
(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:
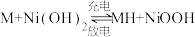 (式中M为储氢合金),写出电池放电过程中正极的电极反应式:
(式中M为储氢合金),写出电池放电过程中正极的电极反应式:
您最近一年使用:0次
【推荐3】研究氮、硫、碳及其化合物的转化对于减少如雾霾、酸雨、酸雾等环境污染问题有重大意义。请回答下列问题:
(1)在一定条件下,CH4可与NO2反应生成对环境无污染的物质。
已知:①CH4的燃烧热:∆H=-890.3 kJ•mol-1②N2(g)+2O2(g)⇌2NO2(g)∆H=+67.0 kJ•mol-1③H2O(g)=H2O(l)∆H=-41.0 kJ•mol-1,则CH4(g)+2NO2 (g) ⇌CO2+2H2O (g)+N2(g)∆H=___ kJ•mol -1。
(2)活性炭也可用于处理汽车尾气中的NO。在2L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成CO2、N2两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
①反应的正反应为________ (填“吸热”或“放热”)反应。
②一定温度下,下列能说明该反应已达到平衡状态的是_______ 。
A. N2与NO 的生成速率相等 B. 混合气体的密度保持不变
C.∆H 保持不变 D. 容器的总压强保持不变
③ 200 ℃时,平衡后向该容器中再充入0.1molNO,再次平衡后,NO的百分含量将______ (填“增大”“减小”或“不变”)。
(3)SO2经催化氧化可制取硫酸,在一定温度下,往一恒容密闭容器中以体积比2∶1,通入SO2和O2,测得容器内总压强在不同温度下与反应时间的关系如图所示。
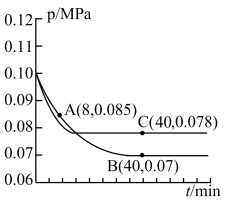
图中C 点时,SO2的转化率为________ 。
②其中C 点的正反应速率υC(正)与A点的逆反应速率υA(逆)的大小关系为:υC(正)____ υA(逆)(填“>”、“<”或“=”)。
(4)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g) ∆H>0,请你分析该设想能否实现?_____ (填“能”或“否”),依据是__________ 。
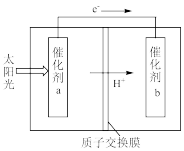
(5)利用人工光合作用,借助太阳能使CO2和H2O转化为HCOOH,如图所示,在催化剂b表面发生的电极反应为:___________ 。
(1)在一定条件下,CH4可与NO2反应生成对环境无污染的物质。
已知:①CH4的燃烧热:∆H=-890.3 kJ•mol-1②N2(g)+2O2(g)⇌2NO2(g)∆H=+67.0 kJ•mol-1③H2O(g)=H2O(l)∆H=-41.0 kJ•mol-1,则CH4(g)+2NO2 (g) ⇌CO2+2H2O (g)+N2(g)∆H=
(2)活性炭也可用于处理汽车尾气中的NO。在2L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成CO2、N2两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
| 温度 | 固体活性炭/mol | NO/mol | N2/mol | CO2/mol |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 |
②一定温度下,下列能说明该反应已达到平衡状态的是
A. N2与NO 的生成速率相等 B. 混合气体的密度保持不变
C.∆H 保持不变 D. 容器的总压强保持不变
③ 200 ℃时,平衡后向该容器中再充入0.1molNO,再次平衡后,NO的百分含量将
(3)SO2经催化氧化可制取硫酸,在一定温度下,往一恒容密闭容器中以体积比2∶1,通入SO2和O2,测得容器内总压强在不同温度下与反应时间的关系如图所示。

图中C 点时,SO2的转化率为
②其中C 点的正反应速率υC(正)与A点的逆反应速率υA(逆)的大小关系为:υC(正)
(4)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g) ∆H>0,请你分析该设想能否实现?
(5)利用人工光合作用,借助太阳能使CO2和H2O转化为HCOOH,如图所示,在催化剂b表面发生的电极反应为:

您最近一年使用:0次



